VDR–SOX2信号与大肠癌进展
酸性肿瘤微环境为恶性肿瘤的发展提供了能量来源。细胞对酸性环境的适应导致了癌症干细胞的出现。维生素D受体(VDR)的表达与大肠癌(CRC)的发生发展密切相关,但其在CRC干细胞中的调控机制尚不清楚。今天给大家带来的发表于“Signal Transduction and Targeted Therapy”,影响因子13.493的文章“VDR–SOX2 signaling promotes colorectal cancer stemness and malignancy in an acidic microenvironment”,详细介绍了VDR–SOX2信号调控大肠癌发展的机制。

我们的研究表明,酸中毒通过下调PPARD的表达降低了VDR的表达。过表达VDR能有效抑制酸中毒细胞的干性和奥沙利铂耐药。VDR核输出信号对酸中毒敏感,VDR从细胞核中输出。此外,染色质免疫沉淀和高通量测序分析显示,VDR通过结合SOX2启动子中的维生素D反应元件转录抑制SOX2,损害肿瘤生长和耐药性。
技术路线

结果:
1)酸中毒抑制VDR表达,VDR表达与恶性大肠癌呈负相关
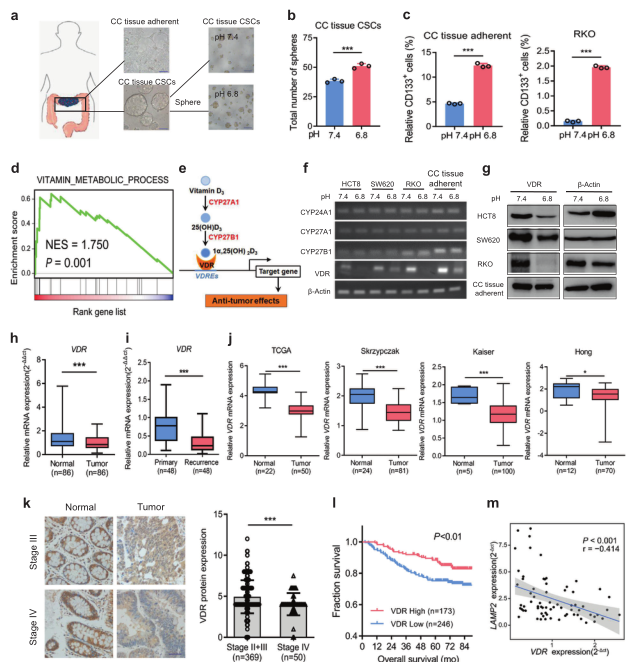
为了研究酸性肿瘤微环境对大肠癌细胞干细胞的影响,我们首先从大肠癌患者的组织样本中分离并鉴定了RKO干细胞样细胞和原代大肠癌细胞、大肠癌干细胞。将细胞培养在不同pH值的培养基中,以评估细胞自我更新的最佳条件。在pH值为6.8的酸性条件下,肿瘤球的数量最大化(图1a、b)。与pH值7.4相比,pH值6.8显著增加了CD133阳性细胞的百分率,促进了CD133、OCT4和SOX2的表达(图1c)。因此,酸性肿瘤微环境可以诱导和维持大肠癌细胞的CSC表型。
为了确定酸性微环境中CSC表型调控的重要途径,我们对pH7.4和6.8培养的RKO细胞进行RNA测序和信号通路富集分析。我们发现脂溶性维生素的代谢过程被酸性条件显著改变(图1d)。维生素D是一种重要的脂溶性维生素,已知维生素D信号通路参与癌细胞分化的调节。因此,我们在pH值为7.4和6.8的条件下测试了维生素D信号通路中具有关键作用的几种蛋白质的表达(图1e),发现各细胞系VDR表达在酸中毒时明显下降(图1f,g)。大肠癌组织与配对相邻组织中VDR的mRNA表达差异显著(图1h)。此外,VDR在复发性大肠癌组织中的表达显著降低(图1i)。TCGA和Skrzypczak,Kaiser和Hong数据库显示,VDR在大肠癌组织中的表达低于正常组织(图1j),VDR在Ⅳ期大肠癌组织中的表达最低(图1k)。我们还研究了VDR表达与预后的关系,结果表明VDR表达低的患者生存时间短(图1l)。LAMP2的表达与肿瘤微环境酸性呈正相关,并且我们发现VDR表达和LAMP2在大肠癌中的表达呈负相关(图1m)。提示酸性肿瘤微环境可抑制VDR的表达,而VDR的表达与大肠癌的恶性程度及复发密切相关。
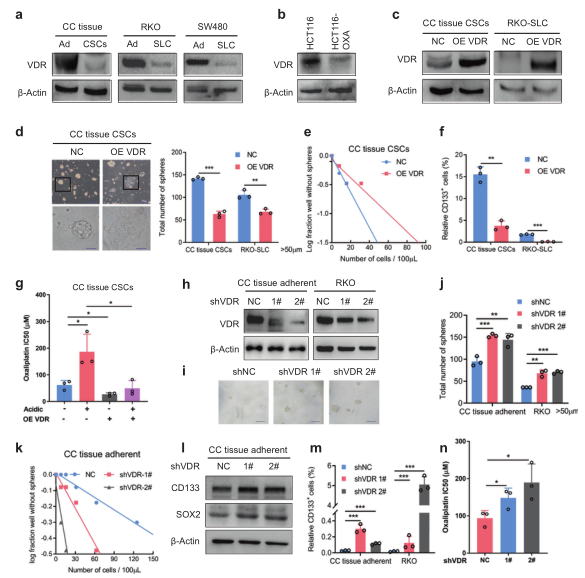
2)VDR损害大肠癌的干细胞和恶性肿瘤
为了研究VDR对大肠癌干细胞表型的影响,我们首先证实了VDR在大肠癌干细胞中的表达低于非干细胞癌细胞(图2a)。此外,在抗奥沙利铂的HCT116细胞中VDR表达降低(图2b)。因此,我们在低VDR表达的大肠癌干细胞中过表达VDR(图2c)。显微成像显示肿瘤球粘附在板的底部,肿瘤球内发生细胞分化(图2d)。VDR过表达显著减少了由CRC干细胞形成的肿瘤球的大小和数量(图2d,e),并显著降低CD133阳性细胞的百分比(图2f)。这些结果表明VDR过表达抑制了大肠癌干细胞的自我更新和诱导细胞分化。此外,VDR的过表达增加了大肠癌干细胞对奥沙利铂的敏感性,并部分减弱了酸性肿瘤微环境介导的耐药促进作用(图2g)。接下来,我们观察到VDR的敲除(图2h)可以提高CRC细胞的自我更新能力(图2i–k),促进干细胞标记物的表达(图2l)。此外,VDR的敲除增加了CD133阳性细胞的百分比(图2m),增强了对奥沙利铂的抵抗力(图2n)。这些结果表明,VDR在酸性肿瘤微环境中抑制CSC表型,提高大肠癌干细胞对药物的敏感性。
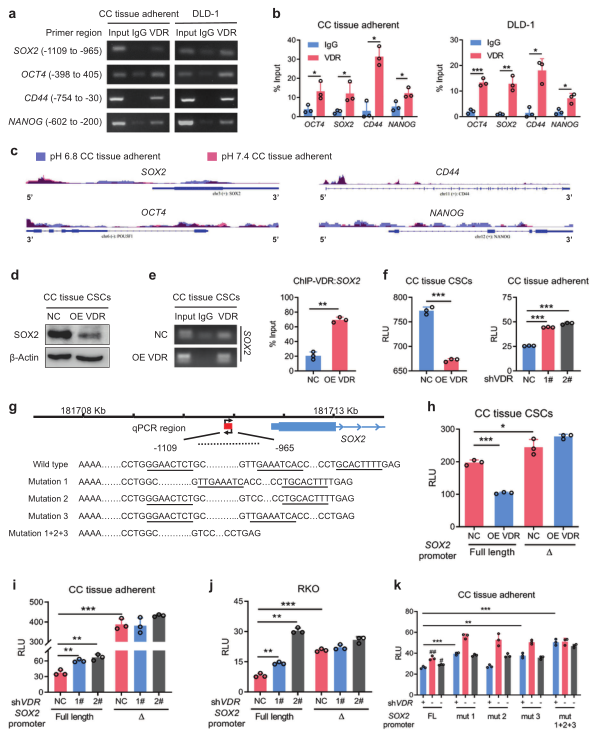
3)VDR通过抑制SOX2启动子的转录活性来下调SOX2的表达
为了阐明VDR如何影响大肠癌的CSC表型和耐药性,我们用染色质免疫沉淀法(ChIP)分析了VDR对干细胞标记物转录的调节作用,发现VDR可与SOX2、OCT4、CD44和NANOG的启动子区结合(图3a、b)。然后,我们利用高通量测序(ATAC-seq)信号分析了在酸性或碱性条件下培养的大肠癌细胞中干性基因的染色质可及性。在酸性条件下,SOX2中的开放染色质优先出现在TSS的上游(图3c),这可能反映了VDR在SOX2启动子区域结合的可能性。我们证实过表达VDR(图3d)会降低SOX2蛋白的表达,并且在过表达VDR的细胞中结合作用增强(图3e)。VDR的过表达抑制了SOX2启动子的转录活性,而VDR的敲除促进了它的转录活性(图3f)。我们进一步删除了SOX2启动子区域的结合序列(图3g),发现VDR对SOX2启动子的抑制作用减弱(图3h–j)。通过生物信息学分析,我们在SOX2启动子中发现了三个VDREs(图3g)。我们对SOX2启动子的转录活性进行了检测和检测。突变1和突变3显著减弱了VDR的抑制作用(图3k)。这些结果表明VDR可能通过抑制SOX2启动子活性来下调SOX2的表达。
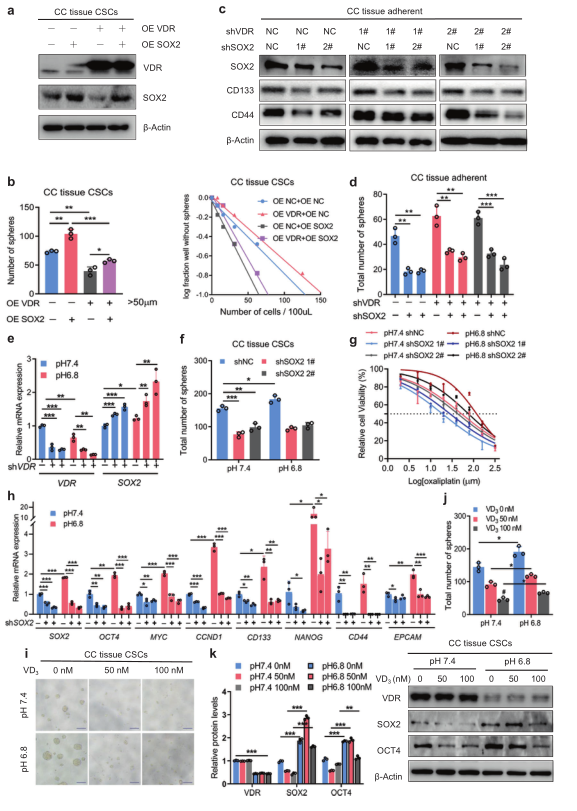
4)酸性肿瘤微环境通过VDR-SOX2轴调控CRC的干细胞特性和耐药
为了证实VDR通过下调SOX2的表达来抑制CRC细胞的恶性表型,我们在过表达VDR的CRC干细胞中过表达SOX2(图4a)。大肠癌干细胞的自我更新能力随着SOX2过表达而增强(图4b)。在低VDR水平的CRC细胞中,SOX2的敲除降低了CD133和CD44的表达(图4c)并降低了自我更新能力(图4d)。我们还分析了酸性和碱性pH中有和没有VDR表达的大肠癌干细胞中SOX2 mRNA。结果表明,在酸性pH条件下,在没有VDR表达的细胞中SOX2 mRNA表达增加(图4e)。与先前的结果一致,在酸性肿瘤微环境中敲除SOX2减弱了结直肠癌干细胞的自我更新能力(图4f),并增强了细胞对奥沙利铂的敏感性(图4g)。在pH6.8时,我们检测了SOX2沉默时干细胞基因网络的mRNA表达。结果表明,当沉默SOX2时,干细胞基因OCT4,MYC和CCND1下调(图4h)。此外,我们发现维生素D的活性形式可以逆转酸性环境介导的自我更新和CD133、SOX2和OCT4在大肠癌干细胞中的表达(图4i,j),提示酸性微环境通过维生素D-VDR信号通路影响大肠癌细胞的干细胞特性。总之,我们的研究结果表明,在酸性肿瘤微环境中VDR的下调减轻了SOX2的转录抑制,导致SOX2表达增加。这些变化促进了大肠癌细胞的干性和耐药性。
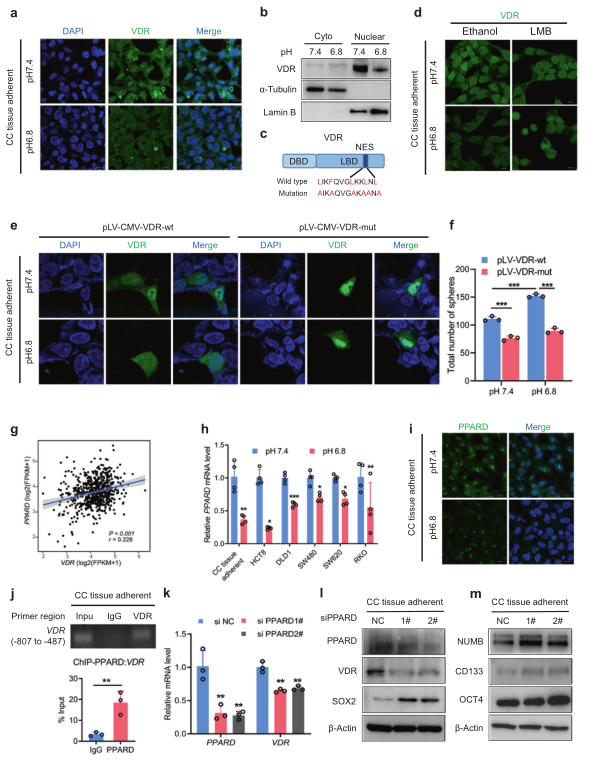
5)酸性微环境抑制核内VDR聚集,通过PPARD抑制VDR表达
VDR调节细胞核中的靶基因。因此,我们检测了VDR在酸性环境中的亚细胞定位。我们发现在酸性条件下,VDR的表达减少,VDR蛋白在细胞核中的积累减少(图5a,b)。进一步的分析表明,在酸性条件下VDR包含核输出信号(NES)(图5c)。LMB与CRM1结合,并抑制其他输出底物的结合。我们在pH7.4和6.8下用LMB处理大肠癌细胞。LMB在pH6.8培养基中阻止了VDR蛋白的核输出(图5d),说明酸性环境下VDR蛋白的核输出依赖于CRM1。为了证实VDR的核输出需要NES,我们用野生型和NES位点突变质粒(图5c)转染CRC细胞,发现VDR的NES突变阻止了VDR在酸性环境下的核输出(图5e)。为了研究核VDR的表达是否使细胞对pH驱动的重编程不敏感,我们用野生型和NES位点突变质粒转染CC组织CSCs,并将其置于酸性条件下。结果表明,VDR的NES突变抑制了大肠癌干细胞在酸性条件下的自我更新(图5f)。这一发现表明,VDR在酸性肿瘤微环境中的核输出是由NES介导的,并且依赖于CRM1。
利用Qiagen数据库,我们预测PPAR家族成员与VDR启动子密切相关。我们首先分析了TCGA数据库中CRC数据中PPARA、PPARD、PPARG和VDR之间的相关性(图5g)。PPARA和PPARD表达与VDR表达呈正相关(图5g)。我们还发现,在酸性条件下,大肠癌细胞中PPARD mRNA和蛋白质水平显著降低(图5h,i),令人惊讶的是,PPARD可以与VDR的启动子结合(图5j),PPARD的敲除降低了VDR的mRNA和蛋白质表达,上调了干细胞标记物的表达(图5k–m)。这些结果表明,酸性肿瘤微环境通过PPARD抑制VDR的表达,诱导VDR蛋白的核输出,抑制VDR的转录调控功能。
6)酸性肿瘤微环境的正常化和VDR表达的诱导抑制了大肠癌的发生和发展
为了确定是否可以通过改变酸性肿瘤微环境和VDR表达来抑制大肠癌的生长,我们将大肠癌细胞注射到裸鼠体内,并给予小鼠水或碳酸氢钠(NaHCO3)溶液。我们发现,VDR过表达后的NaHCO3处理显著抑制了SOX2的表达和肿瘤的发展(图6a),并且NaHCO3处理还有效地减弱了VDR敲除后的SOX2表达和肿瘤形成(图6b)。这些结果表明,降低肿瘤微环境的酸性和诱导VDR的表达可以抑制大肠癌的发展。我们进一步发现,维生素D信号激活和奥沙利铂联合治疗可以抑制患者来源的异种移植物的肿瘤生长(图6c)。PDXs中VDR表达上调,SOX2表达下调(图6d)。这些结果为大肠癌的临床治疗提供了新的理论依据。
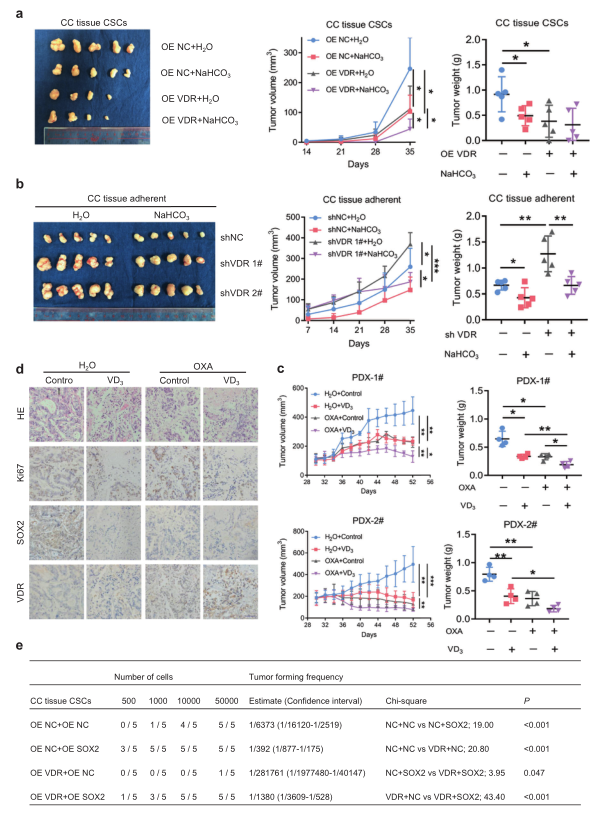
7)VDR表达与SOX2表达呈负相关,有可能用于临床预后预测
我们在体内验证了VDR和SOX2表达对大肠癌干细胞致瘤能力的影响。体内极限稀释实验的结果显示,VDR的过表达显著抑制肿瘤的发生,而SOX2的过表达则减弱了VDR过表达的抑制作用(图6e)。VDR和SOX2高/低表达患者的总生存率(OS)有显著差异。VDR低表达和SOX2高表达的患者预后最差(图7a,b)。VDR和SOX2在III期和IV期标本中的表达水平呈负相关(图7c)。此外,我们评估了65例接受FOLFOX或XELOX方案治疗的晚期大肠癌患者样本中VDR和SOX2的表达。原发性肿瘤中VDR高表达的患者中仅有27.69%对化疗有耐药性,而SOX2高表达的患者对化疗耐药率为72.31%。VDR低表达和SOX2高表达组化疗耐药比例最高(图7d)。这些结果表明,低VDR表达和高SOX2表达都预示着奥沙利铂化疗的耐药性。

结论:这些发现揭示了酸性肿瘤微环境通过调节SOX2的表达而影响大肠癌细胞CSC表型的新机制,并表明VDR表达异常导致维生素D信号的无效激活,导致维生素D在抗肿瘤过程中缺乏作用。






