Cell重磅|国自然/省自然热点:R-loop+相分离—MYC凝聚体阻止R-loop衍生的异常RNA泄漏,促进肿瘤免疫逃逸
简介
针对转录延伸紊乱,MYC癌蛋白多聚化并发生相变。在此,作者证明MYC在内含RNA积累时,从DNA上的经典位置重新定位到新生RNA上。在结合RNA后,MYC形成多聚体,使核小体(RNA外切酶)及其靶向复合物在双链RNA和R-loop周围集中。MYC具有四个RNA结合区域(RBRI–IV)。RBRIII促进MYC多聚化,并招募小体到R-loop上。RBRIII对转录激活和胰腺肿瘤细胞在体外增殖不是必需的,但在体内维持肿瘤生长是必不可少的。通过RBRIII,MYC抑制R-loop衍生的RNA-DNA杂合物的积累,并阻止它们通过TLR3模式识别受体激活先天性免疫激酶TBK1。数据表明,MYC的相变是一种RNA驱动的应激反应,它抑制免疫原性RNA-DNA杂合物的积累。该研究于2026年1月发表在《Cell》,IF:42.5。
技术路线
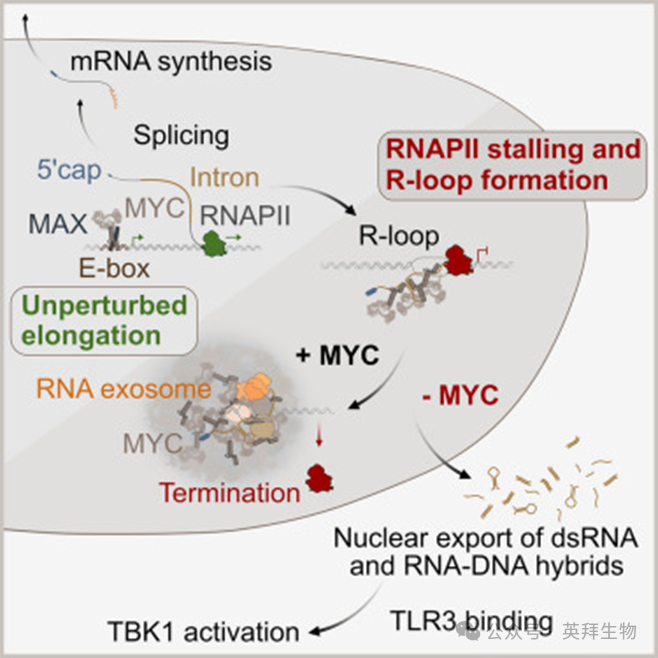
主要研究结果
1.MYC结合新生RNA
为研究细胞内MYC是否与RNA结合,作者在表达高水平MYC的K562慢性髓系白血病细胞中进行了交联免疫沉淀(CLIP)实验。从UV交联细胞中进行的MYC免疫沉淀(IP)的SDS-PAGE凝胶经染色后显示RNA阳性,且该信号对RNase I处理敏感(图1A)。作为对照的非特异性 IgG 免疫沉淀以及未进行 UV 交联的 MYC 免疫沉淀均未检测到 RNA,证明该信号具有特异性。对免疫沉淀RNA进行单端增强CLIP(seCLIP)测序分析,使用Skipper算法在MYC-IP中鉴定出11,077个可重复富集窗口,而IgG对照仅有72个可重复富集窗口。(图1B)。热图以及对对单个基因位点的检查进一步证实了MYC信号的特异性(图1C和1D)。约70%的MYC结合位点位于内含子RNA中,约10%位于剪接位点附近,表明MYC结合新生或未加工的转录本,这与MYCN的发现一致(图1E)。将MYC结合窗口数按不同 RNA 特征对应的总窗口数进行归一化后可见,MYC RNA结合在不同序列元件上分布均匀(图S1A)。而之前分析中未被识别的远端启动子区域的MYC RNA结合位点,主要是因为之前使用了更适合识别染色质上短结合位点的MACS2算法。MYC结合位点的分布与其他内含子结合蛋白相似(图S1B)。许多内含子包含多个MYC结合窗口,表明单个内含子可能被多个MYC分子结合(图S1C)。GO分析未MYC结合基因具有特定功能类别的富集。使用Skipper或PureCLIP算法对MYC结合的RNA窗口进行de novo motif分析,显示几个富含UG的基序有富集(图S1D),与MYCN RNA结合特征类似。MYC的RNA结合位点并未富集DNA上MYC/MAX复合体偏好的E-box序列。与MYC ChIP-seq数据的比较显示,同时存在三类基因:仅在启动子处被MYC结合、仅在新生RNA上被MYC结合,以及同时在DNA和RNA上被MYC结合。定量分析进一步显示,每条mRNA上结合的MYC量与其启动子处结合的MYC量并不相关(图S1E),提示MYC对启动子DNA的结合与对新生RNA的结合是彼此独立的。还在可被多西环素诱导表达外源MYC的U2OS细胞(U2OS^MYC-Tet-On细胞)中进行了seCLIP实验。U2OS细胞表达1.8×10^5个内源性MYC分子,这与增殖中的非转化细胞相当,低于许多肿瘤细胞系。乙醇处理的U2OS^MYC-Tet-On细胞中,内源性MYC对RNA的总体结合模式与K562细胞非常相似:Skipper鉴定出3,220个可重复富集窗口,且MYC结合主要位于内含子中(图S1F和S1G)。
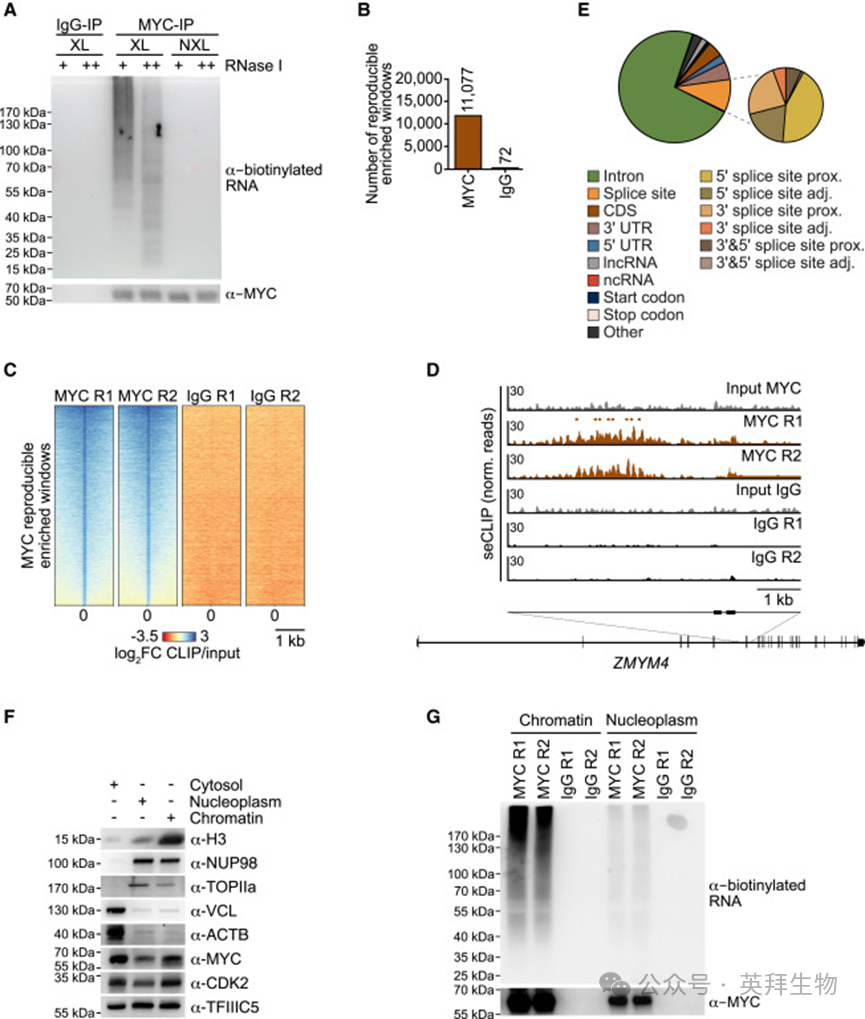
图1:MYC与新生RNA结合
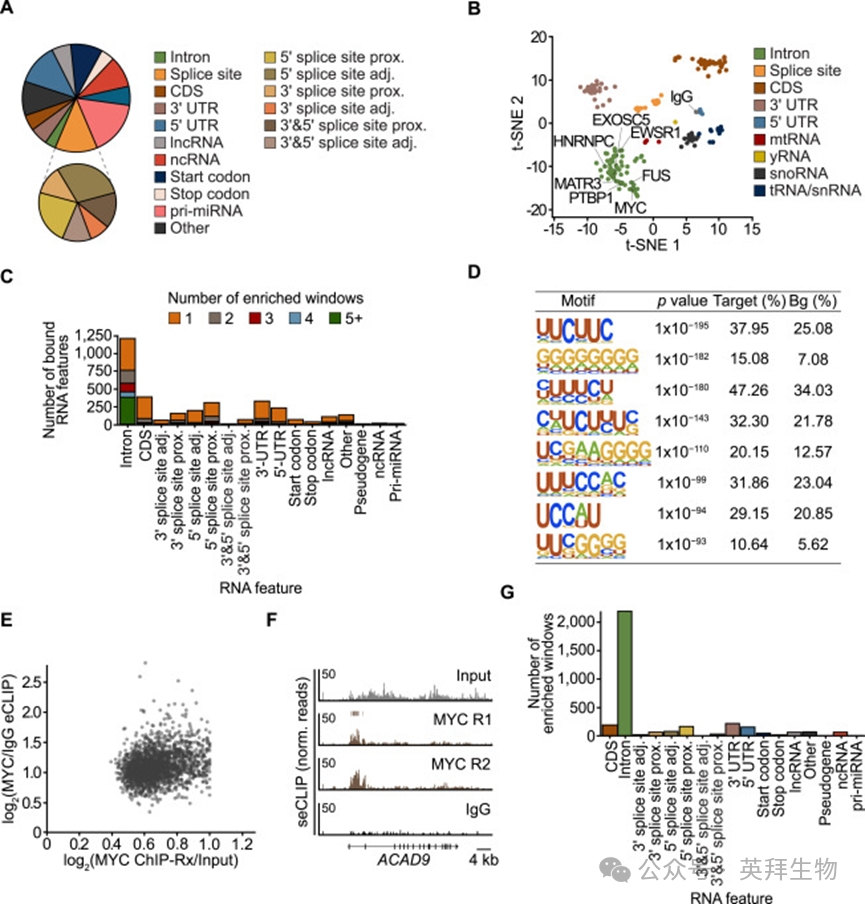
附图1:MYC RNA结合的特征
将U2OS细胞分为染色质、核质和胞质组分后进行eCLIP实验,结果显示MYC同时存在于染色质相关组分和核质组分中(图1F)。MYC和其他可溶性核蛋白也在胞质中被检测到,可能是由于分离过程中的泄漏。MYC结合的RNA几乎只在染色质组分中发现(图1G和S2A)。与总MYC一样,染色质结合的MYC主要与内含子RNA结合(图S2B)。为检验MYC是在转录过程中还是转录后立即结合RNA,对用NVP-2(一种特异性抑制CDK9从而阻断RNAPII暂停释放的抑制剂)处理1小时的细胞进行eCLIP实验。由于MYC mRNA高度不稳定,在经多西环素处理24小时的U2OS^MYC-Tet-On细胞中完成该实验。在这些条件下,U2OS^MYC-Tet-On细胞每个细胞表达约3×10^6个MYC分子,约为结肠癌和胶质母细胞瘤细胞中MYC水平的3倍。CLIP实验显示,在多西环素诱导后,MYC对RNA的结合随MYC蛋白水平同步升高(图S2C和S2D)。在低水平和高水平MYC表达下,MYC与RNA的总体结合模式非常相似(图S2E),但Skipper分析显示,MYC在RNA上的总体结合位点数增加了两倍。虽然低水平和高水平MYC下与内含子的结合基本保守,但高水平MYC下与外显子的结合增强(图S2F和S2G)。用NVP-2抑制CDK9 1小时导致MYC的RNA结合显著减少(图2A),而总MYC水平不受影响(图S2H和S2I)。对于每种RNA,MYC结合的减少与RNA丰度的减少成正比,并且这种下降在内含子中比在外显子中更明显,提示该效应与RNA加工有关(图2B和2C)。据此得出结论,MYC在转录过程中或转录刚结束后结合染色质相关的新生RNA。
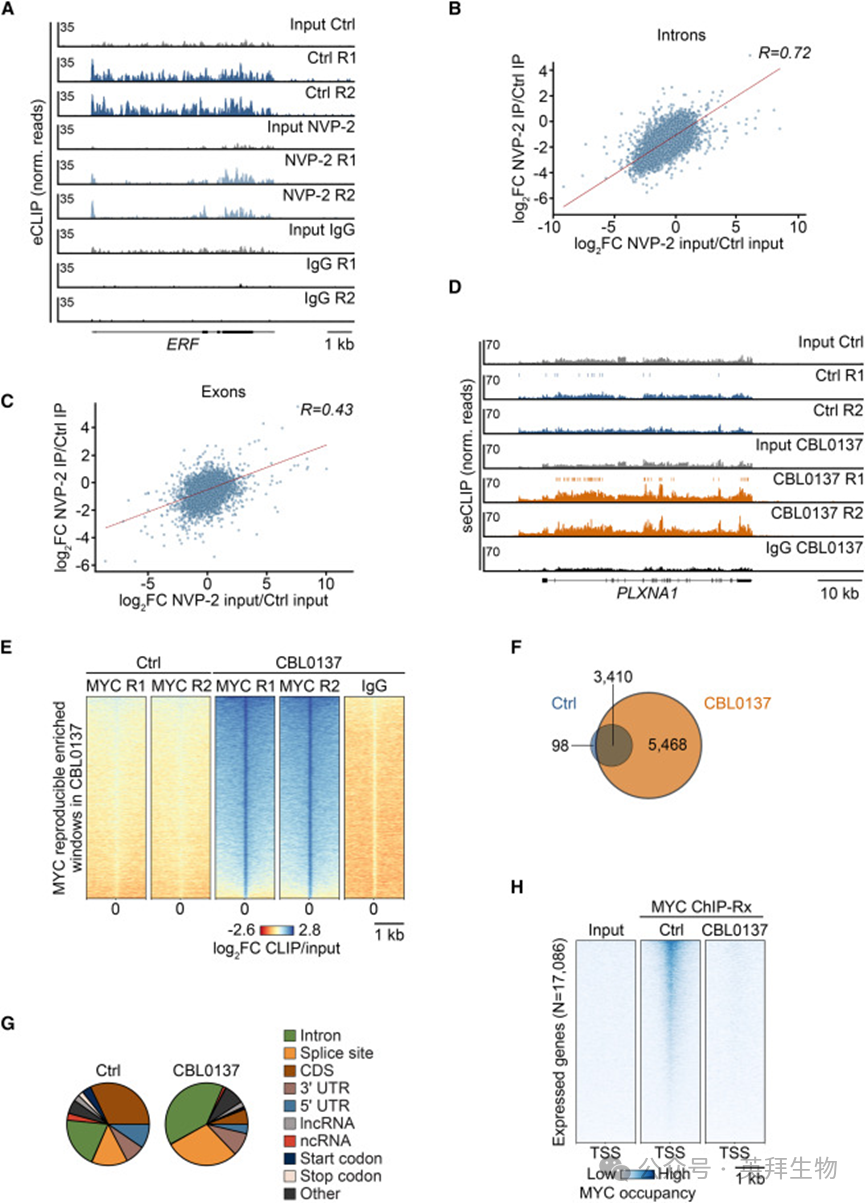
图2:MYC的RNA和DNA结合池处于动态平衡
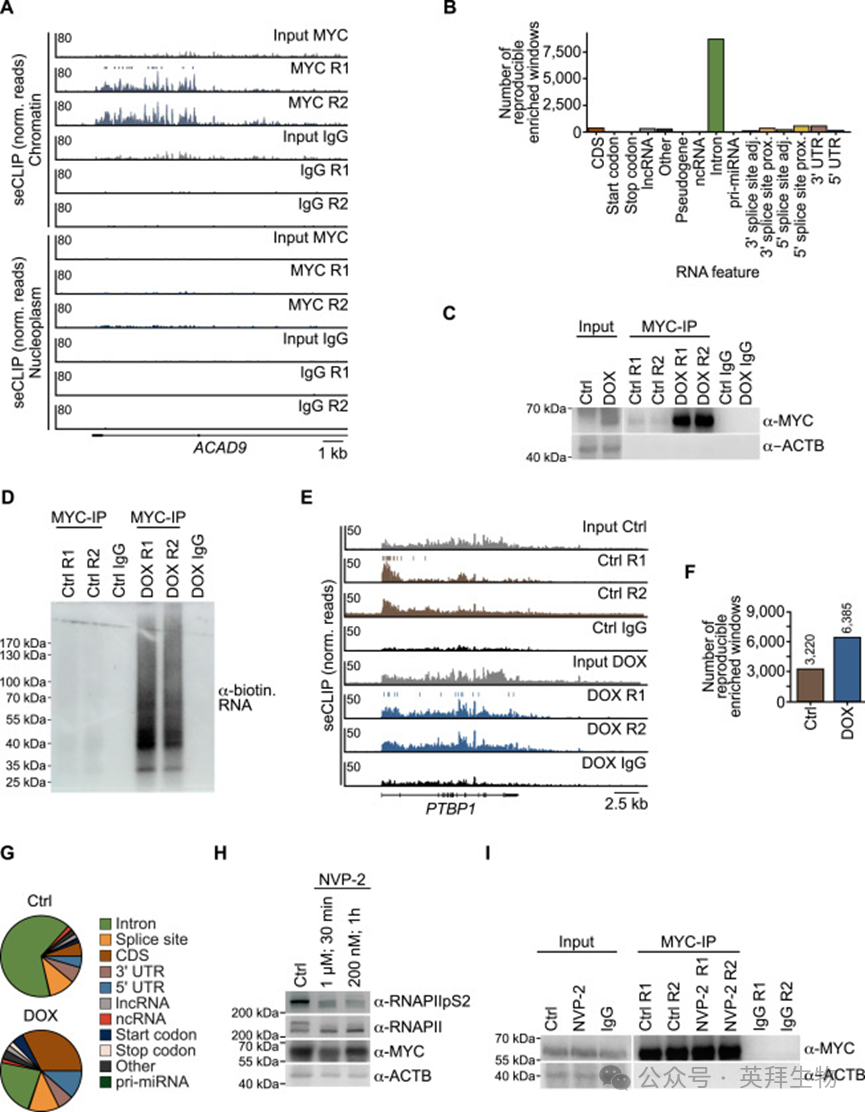
附图2:对MYC RNA结合的进一步表征
2.MYC蛋白在DNA结合态与RNA结合态之间处于动态平衡
针对FACT组蛋白伴侣或剪接体的SF3B1亚基的抑制,MYC蛋白会发生相变并形成多聚,这促使作者研究抑制FACT或剪接体是否会影响MYC在RNA结合态与DNA结合态之间的分布。为此,作者对多西环素处理的U2OS^MYC-Tet-On细胞进行了MYC和RNAPII的平行染色质免疫沉淀测序(ChIP-seq)及seCLIP测序,这些细胞用FACT抑制剂CBL0137处理。暴露于CBL0137显著增加了MYC RNA结合位点的总数以及MYC与许多个体位点的结合(图2D-2F)。CBL0137特异性结合位点的大多数是内含子,提示FACT阻断增加了MYC在未加工转录本上的占据(图2G)。相应地,CBL0137处理导致seCLIP实验的input中出现的内含子RNA数量相对增加(图S3A)。ChIP-Rx测序显示,CBL0137导致启动子附近的RNAPII染色质占据显著下降,并且基因体内Ser2位点磷酸化的延伸型RNAPII(RNAPIIpS2)减少,这很可能同时源于转录终止和RNAPII 降解,提示在CBL0137处理细胞中,MYC结合的是从RNAPII上释放出来的新生RNA(图S3B和S3C)。
MYC对多个含 E-box 的启动子的结合会因 FACT 抑制而下降。经多西环素处理的U2OS^MYC-Tet-On细胞的ChIP-Rx测序显示,FACT抑制导致活性启动子上的染色质结合型MYC几乎完全损失(图2H)。类似地,用pladeniolide B(PlaB)抑制剪接体因子SF3B1也导致MYC从活性启动子全局性地重新分布到内含子RNA上(图S3D和S3E),且许多RNA结合位点靠近剪接位点(图S3F)。由于剪接体抑制延迟了转录延伸(表现为启动子近端RNAPII相对延伸型RNAPII的比例增加,图S3B和S3C),并导致未加工RNA的积累,推测MYC RNA结合的增加是由于内含子RNA的积累所致。为验证这一点,使用小干扰RNA(siRNA)来耗竭核外切体(负责降解内含子RNA)的核心亚基EXOSC5。seCLIP实验显示,EXOSC5的耗竭导致MYC RNA结合增加(图S3G和S3H),这一变化与多种内含子RNA总量升高相一致。针对MYC的siRNA对照实验进一步证实了该信号的特异性(图S3G和S3H)。综上,内含子RNA的积累使MYC从DNA结合态转变为RNA结合态。
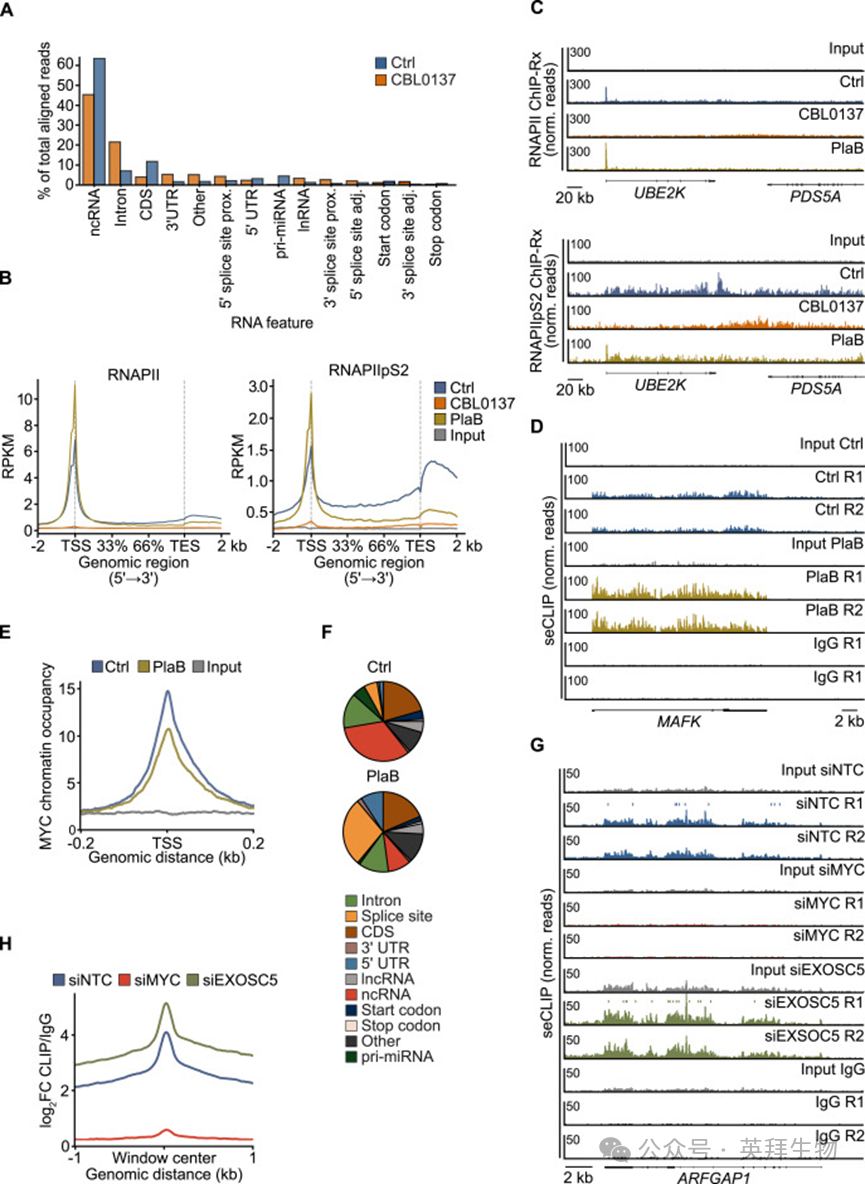
附图3:CBL0137和PlaB依赖性转录延伸和MYC RNA结合的变化
3.MYC多聚体在R-loop和dsRNA周围富集RNA降解因子
在FACT抑制前短时间内用CDK9抑制剂NVP-2阻断新生转录,会在MYC水平未变的情况下减少MYC多聚体数量,提示多聚体形成于新生RNA周围。(图S4A)。因此检测了MYC是否与RNA代谢或降解因子相关(图3A)。对U2OS细胞中的MYC进行免疫沉淀时,可共沉淀出MAX以及总RNAPII和延伸型RNAPIIpS2(图3A)。与对照IP相比,抗MYC的IP还含有EXOSC10(外切酶体的催化亚基)、ZCCHC8(NEXT复合物的支架亚基)、参与m6A代谢的YTHDC1、RBM15和METTL3,以及RNA结合蛋白FUS、HNRNPC和STRBP(图3A)。上述实验中作者在裂解液中加入了RNase抑制剂。用降解DNA和RNA的Benzonase处理细胞裂解液,对MYC与多个RNA降解因子的相互作用没有影响,排除了这些相互作用是通过RNA间接介导的可能性(图S4B)。反向IP实验证实了MYC与几个RNA加工因子的相互作用(图S4C)。用MG-132或CBL0137(两者均诱导MYC多聚化)处理细胞,引起了共沉淀蛋白量的变化,这些变化与MYC多聚体形成的动力学相关,表明这些相互作用发生在MYC多聚体中(图S4D)。对经多西环素处理并暴露于CBL0137的U2OS^MYC-Tet-On细胞进行定量免疫荧光分析显示,多种参与RNA代谢和降解的因子在MYC多聚体中富集(图3B)。平均而言,约10%的总MYC蛋白集中于foci中,而共定位蛋白的比例始终低于MYC,范围从1.6%(MTR4)到8.8%(EXOSC10)(图S4E)。相比之下,能够结合新生mRNA的ARS2,integrator与restrictor转录终止复合体的INTS11和ZC3H4亚基,切割与加尾特异性复合体的CPSF3亚基,以及RNAPII暂停释放的负调控因子Hexim1,均未定位于MYC多聚体中(图S4F)。
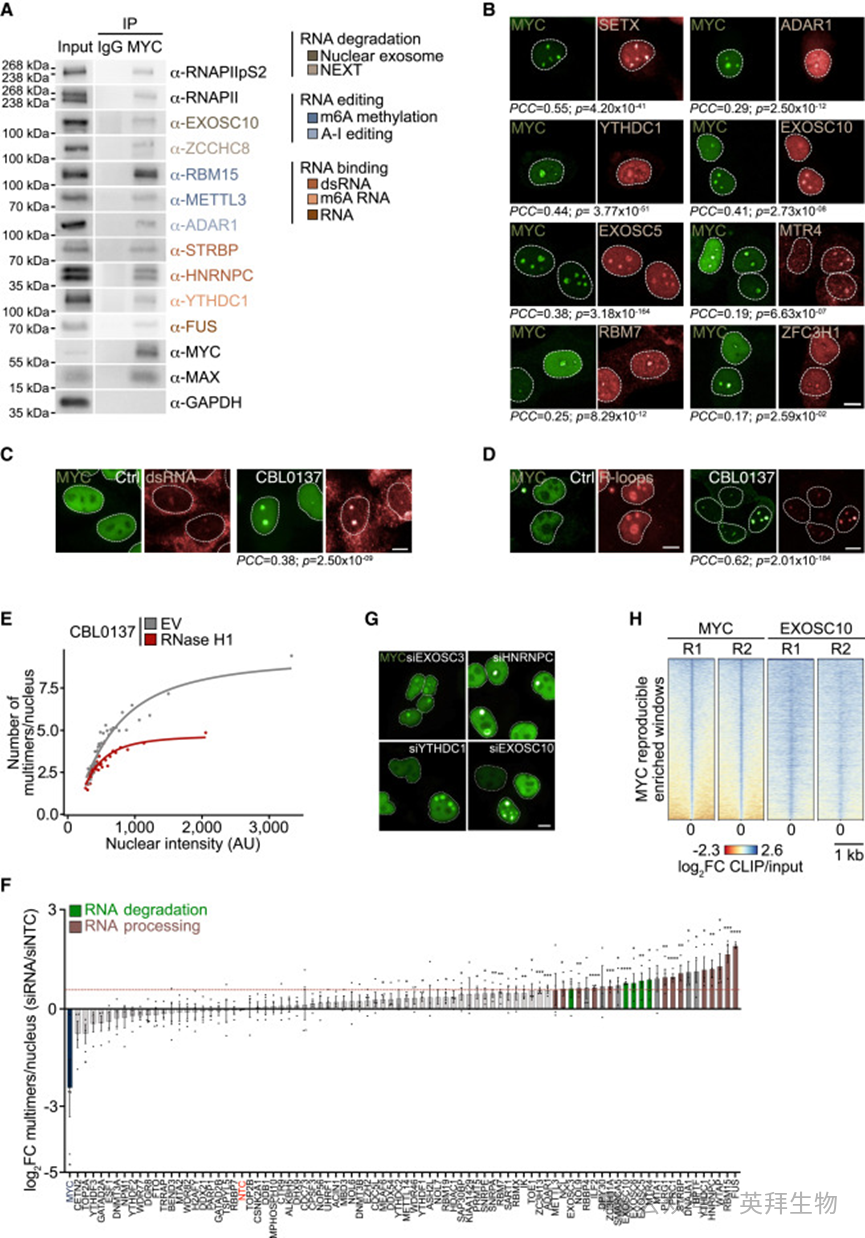
图3:MYC多聚体是RNA降解和加工因子的中心
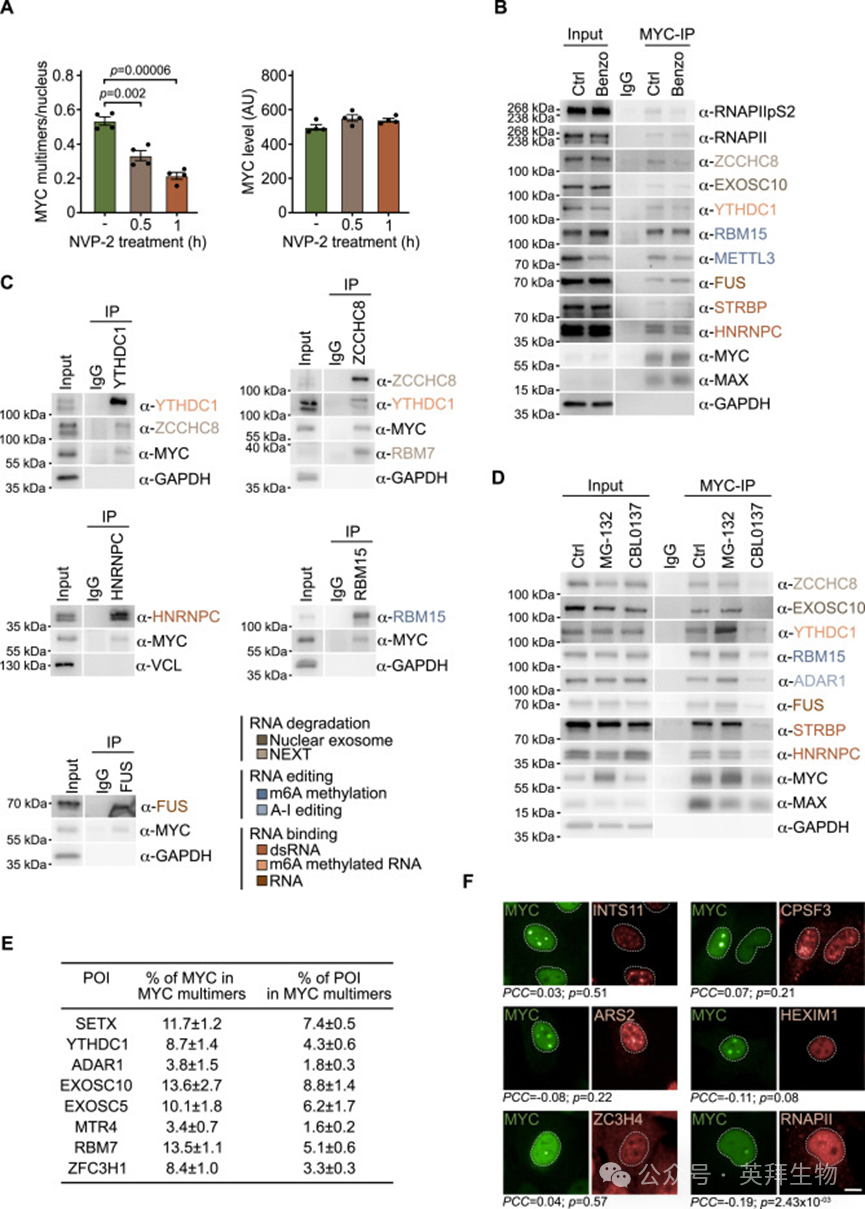
附图4:对MYC蛋白相互作用的进一步分析
为判断MYC多聚体内是否存在特定RNA结构,用识别双链RNA(dsRNA) 的单克隆抗体J2染色细胞。同时使用稳定表达了RNaseH1的RNA-DNA杂合体结合结构域(HBD)并连接抗体标签,另以携带HBD三个位点突变的WKK突变体作为特异性对照(图S5A)。在四环素处理的U2OS^MYC-Tet-On细胞中,CBL0137存在时,dsRNA和R-loop都集中在MYC多聚体中(图3C和3D)。一致地,RNA-DNA免疫沉淀(IP)后进行cDNA转换(DRIPc)测序(用于绘制全基因组R-loop分布),显示在对照细胞中MYC结合RNA处没有R-loop的显著富集,而在CBL0137处理细胞中识别的R-loop与MYC RNA结合位点重叠(图S5B-S5D)。为确定R-loop或R-loop介导的转录-复制冲突是否对MYC多聚体化是必需的,在U2OS^MYC-Tet-On细胞中稳定表达融合了核定位信号的RNase H1,并证实该酶定位于细胞核(图S5E)。对MYC水平和多聚体焦点数量的测量显示,RNase H1的表达减弱了CBL0137响应下的MYC多聚体化(图S5F)。对超过3,000个细胞中MYC免疫荧光信号和多聚体焦点数量的独立定量显示,去除R-loop会在不依赖MYC水平的情况下降低MYC多聚化(图3E)。得出结论,MYC多聚体是可在R-loop和dsRNA附近富集RNA降解过程的“枢纽”,且R-loop可促进MYC的多聚化。
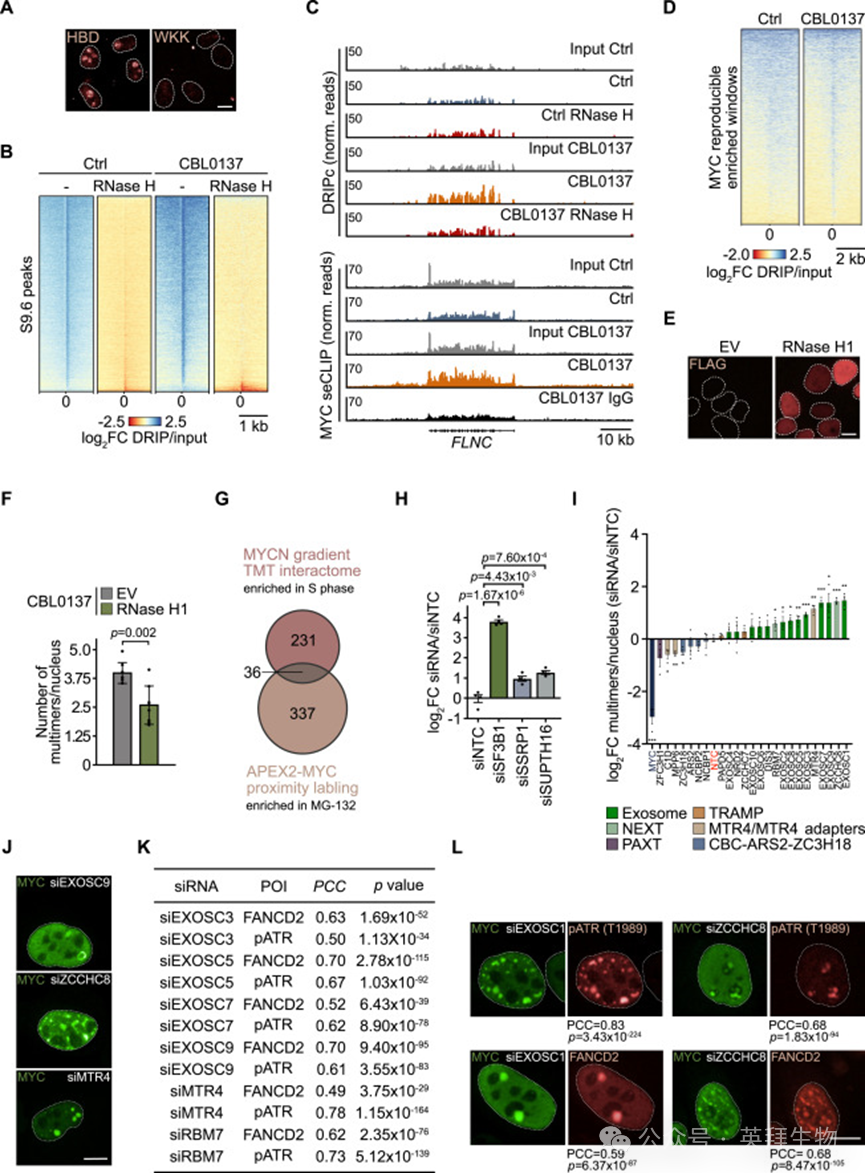
附图5:MYC多聚体背景下R-loop的分析
4.未降解的新生RNA可驱动MYC多聚化
为明确驱动MYC多聚化的关键因子,筛选了84条针对MYC多聚体互作组中蛋白或RNA结合MYCN所涉及蛋白的siRNA(图S5G)。在已用多西环素处理的U2OS^MYC-Tet-On细胞中转染特异性siRNA,以尽量减少对MYC表达本身的影响,并检测其对MYC多聚体形成的作用。针对FACT复合体两个亚基SUPTH16和SSRP1的siRNA,以及针对剪接体亚基SF3B1的siRNA,均可促进MYC多聚化,这与CBL0137或pladienolideB的作用一致(图S5H)。筛选结果显示,针对RNA加工和降解因子的siRNA会在未受应激的细胞中诱导MYC多聚化(图3F和3G)。第二轮siRNA筛选进一步耗竭了核外切体及其靶向复合体TRAMP、NEXT和PAXT的亚基,以及ARS2等其他因子;结果显示,耗竭外切体及其将外切体导向非poly(A)RNA的NEXT复合体亚基会触发MYC多聚化,而其他因子的耗竭影响较弱或无明显影响(图S5I和S5J)。FACT抑制时,MYC会在停滞复制叉附近多聚化;同样地,耗竭多个外切体亚基、NEXT亚基ZCCHC8及其他RNA降解因子时也会出现类似现象(图S5L和S5L)。值得注意的是,MYC的RNA结合位点与EXOSC10的结合位点存在显著重叠(图3H)。综上,未能降解新生RNA或异常RNA会稳定MYC多聚体。
5.MYC是一种多价RNA结合蛋白
为炎症MYC是否直接与RNA结合,作者纯化了重组的全长(FL)MYC蛋白(图S6A)。将MYC与两条与seCLIP实验中被MYC强烈结合的内含子RNA位点相对应的单链RNA寡核苷酸(PTDSS2和ANKRD11)孵育后,揭示PTDSS2RNA和ANKRD11RNA具有相似的亲和力和表观Kd值,分别为0.22±0.04μM和0.72±0.16μM。后者包含上述PureCLIP分析中鉴定出的UUAGUAG基序(图S6B)。这些值与近期发表的MYC对G富集RNA序列的亲和力相似。与多项研究一致,MYC对E-box的高亲和力结合需要与MAX形成异源二聚体,因此MYC对含有共识E-box序列的单链DNA或双链DNA均未表现出高亲和力(图S6C)。MYC对RNA-DNA杂合体和dsRNA的亲和力也较低(图S6C)。MYC在细胞中与这些结构共定位,可能部分依赖于其与NEXT复合体的MTR4解旋酶或senataxin的结合(图3B)
为鉴定介导RNA结合的残基,使用覆盖整个MYC序列、彼此重叠且长度为25个氨基酸的肽库进行分析。结果鉴定出四个RNA结合区域(命名为“RBRI–IV”),其中围绕MYC盒IV的RBRIII显示出最强的结合(图4A)。RBRIV包含结合DNA的碱性区域,其中含有一个富含精氨酸的RNA结合基序,可增强MYC与启动子的相互作用。为确定MYC RNA结合的其他作用,进行了荧光各向异性实验,发现包含氨基酸1-163和304-354的重组蛋白对ssRNA表现出显著的亲和力,表观Kd值分别为1.94 ± 0.24和1.92 ± 0.24 μM(图4D,S6D)。由于RBR与参与蛋白质修饰和周转的序列重叠,在U2OS细胞中稳定表达了多个突变等位基因,其中这些结构域中的碱性残基被丙氨酸替换(图S6E),这些细胞的内源性MYC基因已用生长素诱导型降解子标记(U2OS^MYC-AID细胞)。所有位于氨基端的替换突变体表达水平都显著低于野生型MYC(WT^MYC),阻碍了在细胞中的进一步分析(图S6F和S6G)。相比之下,一个在RBRIII中带有六个丙氨酸替换(K316A,K317A,R331A,R334A,R340A,和 K341A)的突变等位基因的表达水平与WT^MYC相同(图4B,4C,S6F)。体外结合实验证实这些突变消除了RNA结合(图4D),因此用该等位基因(RBRIII^MUT MYC)进行后续实验。RBRIII^MUT MYC保留了MYC Box IV中的HCF-1结合位点和核定位信号中的三个碱性氨基酸(K323,R324,K326),并且完全定位于细胞核(图4B,S6H)。eCLIP测序显示,与WT^MYC相比,RBRIII^MUT MYC结合新生RNA的能力显著受损,这在多个单个RNA上均可见,并反映在表达RBRIII^MUT MYC并用CBL0137处理的细胞中RNA结合位点总数的减少(图4E和4F)。在平行的ChIP-Rx测序实验中,在未应激细胞中,RBRIII^MUT MYC与启动子近端染色质的结合与WT^MYC几乎无区别(图4G,4H,4I)。WT^MYC和RBRIII^MUT MYC的染色质结合位点均在作为MYC/MAX复合物DNA结合基序的E-box序列中高度富集(图S6I)。与WT^MYC不同,RBRIII^MUT MYC在CBL0137处理后部分保留在染色质上,表明MYC从DNA重新定位到新生RNA需要一个完整的RBRIII(图4H和4I)。RBRIII^MUT MYC在细胞内形成多聚体的能力受损,表明MYC多聚体是在RNA周围形成的(图4J,4K,S6J)。在体外,荧光标记的RNA被重组MYC蛋白形成的液滴招募(图S7A),用ssRNA寡核苷酸孵育以RNase敏感的方式增强了MYC多聚化(图S7B)。对U2OS细胞施加CBL0137后,RBRIII^MUT MYC与EXOSC10的共定位能力相较WT^MYC明显受损(图4K,4L)。近邻连接实验(PLA)显示,内源性MYC可促进EXOSC10向R-loop募集(图S7C),而RBRIIIMUTMYC在将EXOSC10募集到R-loop上的能力方面受损(图4M,4N)
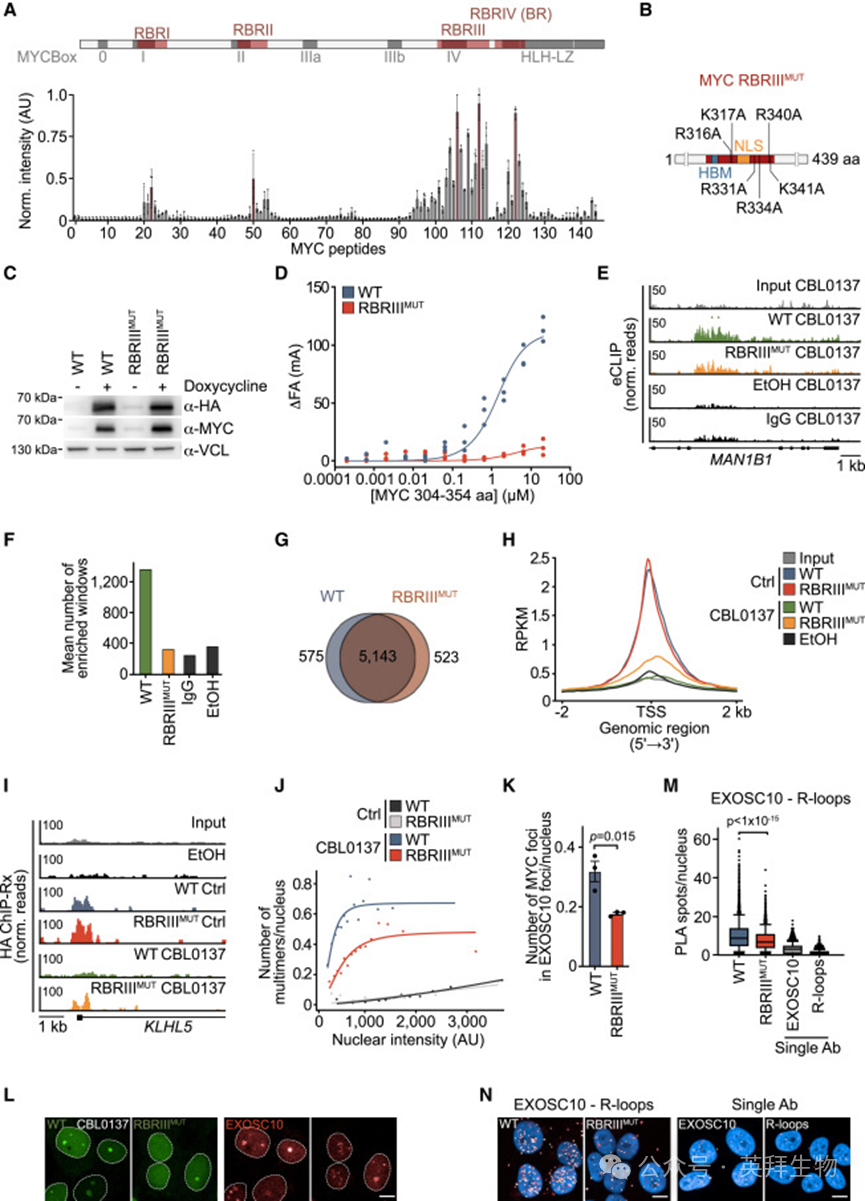
图4:MYC是一种多价RNA结合蛋白
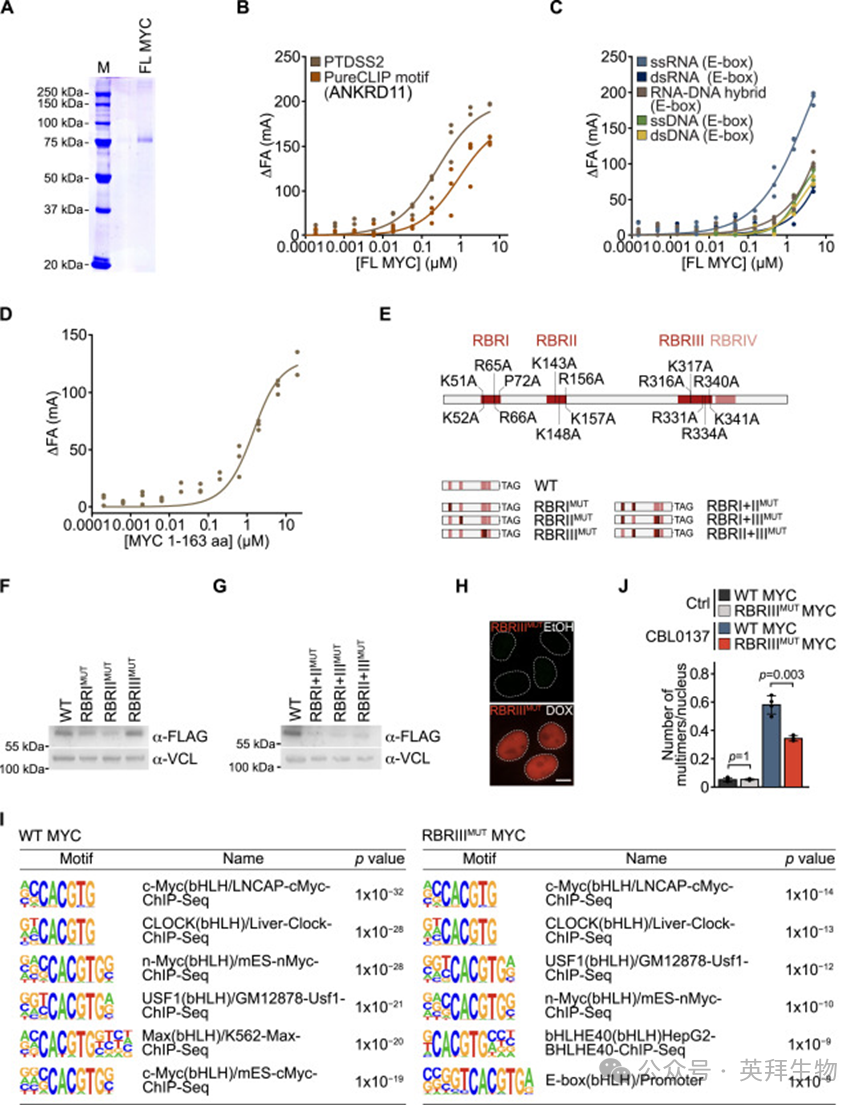
附图6:体外和细胞中MYC多聚化及RNA结合的进一步表征
6. MYC的RBRIII是抑制先天免疫信号所必需的
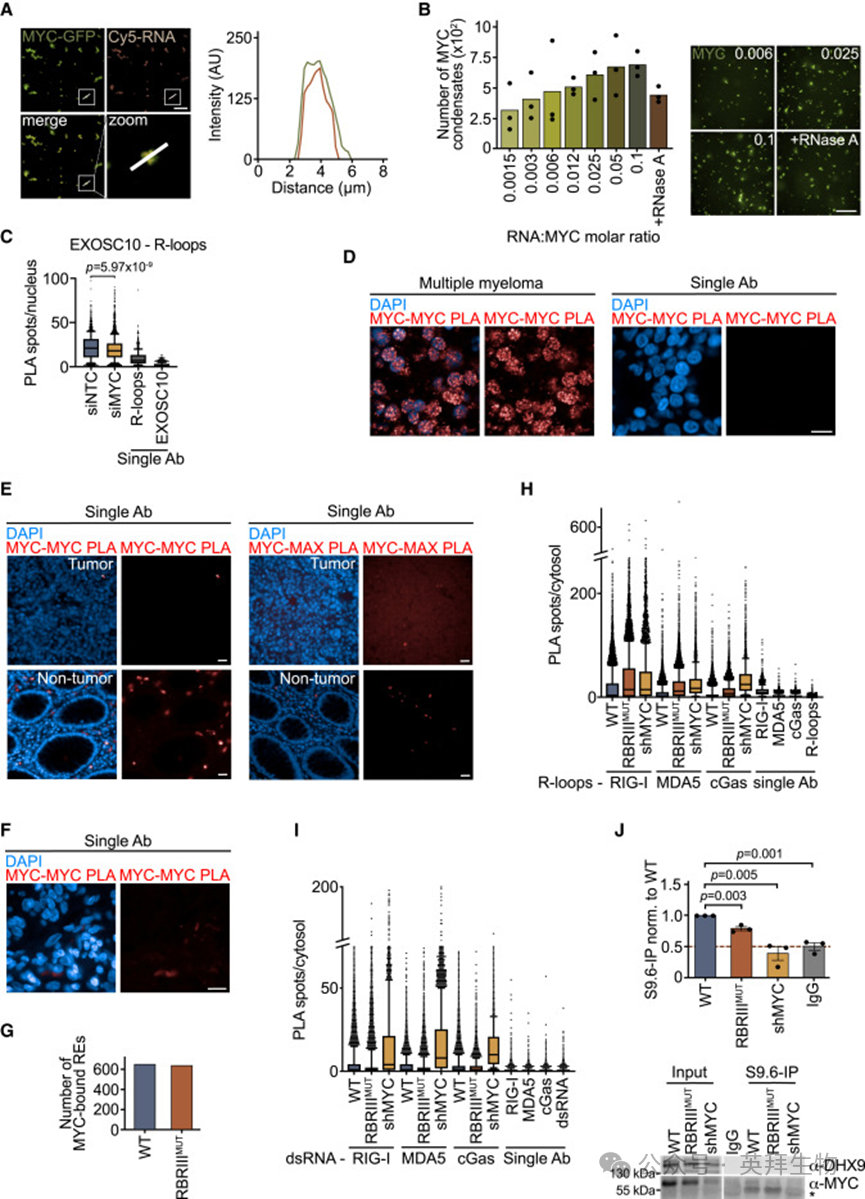
在应激反应下,MYC多聚体在正常和肿瘤细胞系以及人类多发性骨髓瘤患者样本中积累(图S7D)。在人类结肠肿瘤和邻近正常组织中进行的MYC-MYC和MYC-MAX PLA(图5A和S7E)显示,MYC/MAX异二聚体在正常组织和肿瘤组织中的水平相似。相比之下,正常组织中几乎检测不到MYC多聚体,但在肿瘤中其水平显著增加。还在人胰腺癌组织样本中检测到MYC多聚体(图5B和S7F)。
为探索通过RBRIII的RNA结合和寡聚体的形成是否赋予肿瘤细胞选择优势,在表达四环素诱导性短发夹RNA(shRNA)靶向内源性MYC的胰腺KPC细胞中表达了WT^MYC和RBRIII^MUT MYC。免疫印迹证实了在添加四环素后内源性MYC的耗竭,并显示WT^MYC和RBRIII^MUT MYC的表达水平相同(图5C)。与U2OS细胞中的观察结果一致,eCLIP实验表明RBRIII^MUT MYC在结合新生和内含子RNA方面受损(图5D和5E),而平行的ChIP-Rx测序实验表明其与启动子近端染色质的结合与WTMYC几乎相同(图5F、5G和5H)。WT^MYC和RBRIII^MUT MYC的表达刺激了KPC细胞在培养中的增殖(图5I)。接下来,将稳定表达萤火虫荧光素酶的原位移植肿瘤细胞移植到C57BL/6同源小鼠中。7天后,添加四环素以耗竭内源性MYC并诱导WT^MYC和RBRIII^MUT MYC的表达。在这些实验中,表达WT^MY的肿瘤在28天内平均体积增加了24倍,而表达RBRIII^MUT MYC的肿瘤在同一时期体积减少了94%(图5J和5K),证明RBRIII在体外基本不是必需的,但在体内防止肿瘤消退是必需的。
为解释这一表型,对用多西环素处理48小时后的细胞进行了RNA测序,结果显示WT^MYC和RBRIII^MUT MYC在激活经典MYC靶基因集和细胞周期进展相关的E2F依赖基因方面没有显著差异(图5L)。相比之下,虽然WT^MYC还抑制了由多种转录因子驱动的先天免疫信号基因,包括NF-kB/RelA、视黄酸受体和干扰素调节因子(Irf1),但RBRIII^MUT MYC在抑制这些基因集方面存在缺陷(图5L)。由于NF-kB和IRF依赖性转录均被TBK1激活,基因表达差异可能反映了RBRIII^MUT MYC无法抑制TBK1活性。这一假设得到了强烈支持,因为RBRIII^MUT MYC无法抑制TBK1的自磷酸化,也不能抑制其下游靶标P62磷酸化和LC3脂化(图5C)。
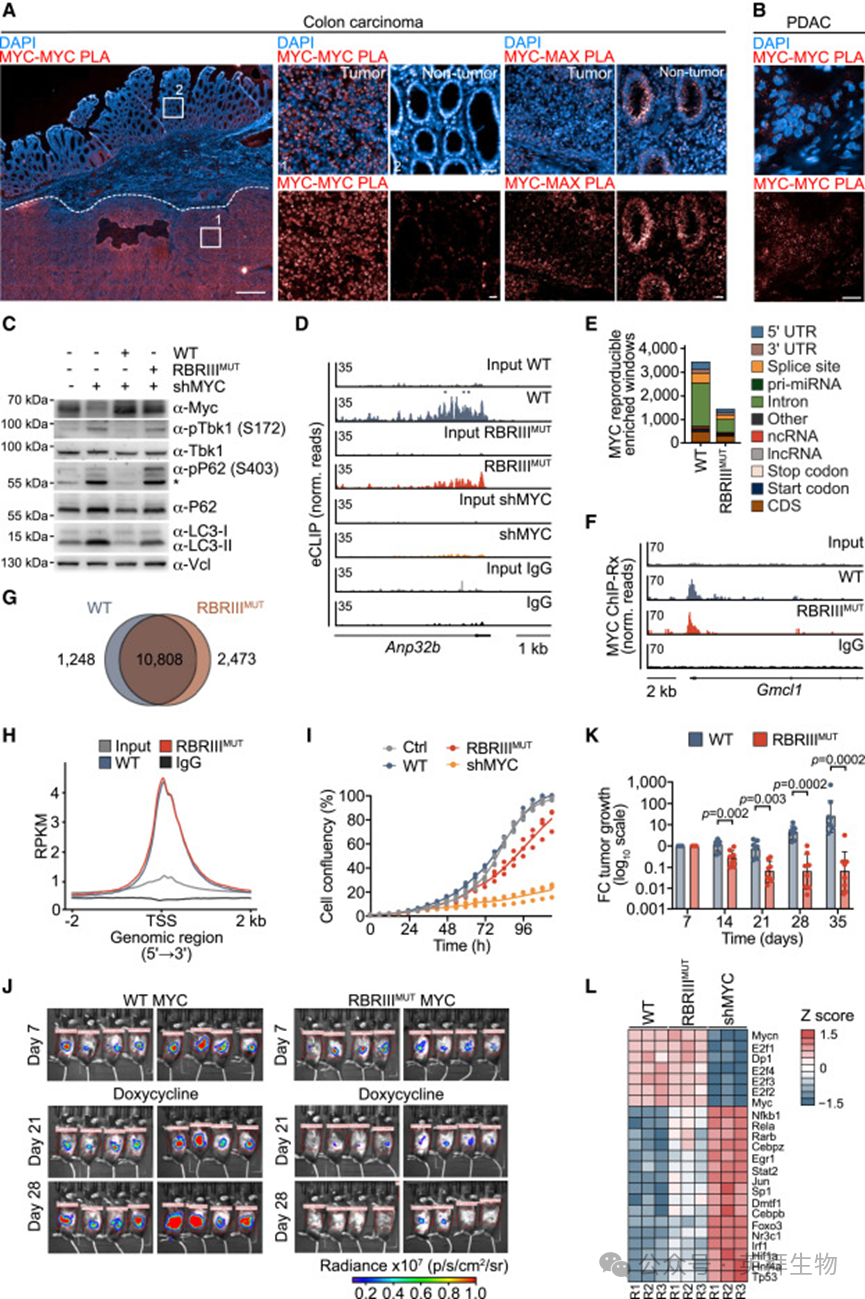
图5:MYC的RNA结合抑制了PDAC细胞中的先天性免疫信号通路,并在体内促进肿瘤生长
附图7:对MYC RBR突变体的进一步表征
7. MYC的RBRIII对R-loop结合及DNA/RNA杂交体抑制是必需的
TBK1的激活依赖于MYC的耗竭,这取决于模式识别受体TLR3,后者能结合dsRNA和R-loop衍生的RNA-DNA杂合体。检测TRIF1(一种底物适配蛋白)与TLR3接近程度的PLA实验显示,在MYC耗竭细胞中存在强烈信号,该信号在表达WT^MYC后被抑制,但RBRIII^MUT MYC的抑制作用要弱得多(图6A)。seCLIP实验表明,TLR3结合了编码RNA和多种非编码RNA,并且在MYC耗竭后,多种RNA类别的富集RNA数目增加(图6B和图6C)。MYC耗竭还增加了通过DRIPc测序确定的结合到R-loop上的TLR3结合RNA的数量(图6D)。PLA实验显示,RBRIII^MUT MYC与WT^MYC一样,抑制了dsRNA加载到TLR3上(图6E),这与eCLIP测序评估的WT^MYC或RBRIII^MUT MYC结合重复元件的数量未受影响一致(图S7G)。与WT^MYC不同,RBRIII^MUT MYC无法阻止RNA-DNA杂合体在TLR3上的积累(图6F),这表明RBRIII在R-loop代谢中发挥作用。与RIG-I、MDA5和cGAS模式识别受体相关的PLA实验显示类似但较弱的效果(图S7H和图S7I)。
与WT^MYC相比,RBRIII^MUT MYC在KPC细胞中与R-loop的邻近性和相互作用减少(图7A和S7J),这促使作者在MYC耗竭细胞和表达WT^MYC或RBRIII^MUT MYC的细胞中绘制R-loop图谱。这些实验鉴定了4,912个R-loop区域,其中501个位于有MYC结合RNA的基因中(图7B)。这些R-loop中的大多数位于内含子中(图7C)。对501个MYC RNA结合基因内的DRIPc信号的定量表明,表达RBRIII^MUT MYC的细胞中R-loop中含有的RNA量显著高于表达WT^MYC的细胞(图7D)。RBRIII^MUT MYC相对于WT^MYC没有改变这些R-loop所宿主基因的表达,表明R-loop数量的增加独立于宿主基因的表达差异(图7E)。RBRIII^MUT MYC与R-loop中含有的RNA结合的数量显著低于WT^MYC(图7F)。对单个基因的检查发现,有几个MYC结合的R-loop在表达RBRIII^MUT MYC的细胞中积累,但在表达WT^MYC的细胞中不积累,并且这些R-loop中含有的RNA在MYC耗竭时被TLR3结合(图7G)。MYC结合的R-loop中的RNA水平在EXOSC10耗竭时显著增加,与所有含R-loop的基因相比,在MYC结合基因上的增加更为明显(图7G和7H)。虽然表达WT^MYC的KPC细胞在多个基因上表现出低基线水平的R-loop,在EXOSC10耗竭时增强,但表达RBRIII^MUT MYC的KPC细胞显示出高基线水平的R-loop,这些R-loop在EXOSC10耗竭时没有进一步增强,这表明MYC和EXOSC10协同抑制R-loop的积累(图7I和7J)。总的来说,上述数据显示,MYC通过RBRIII招募RNA外切体,以抑制双链RNA和R-loop衍生的RNA-DNA杂合体在TLR3上的负载。
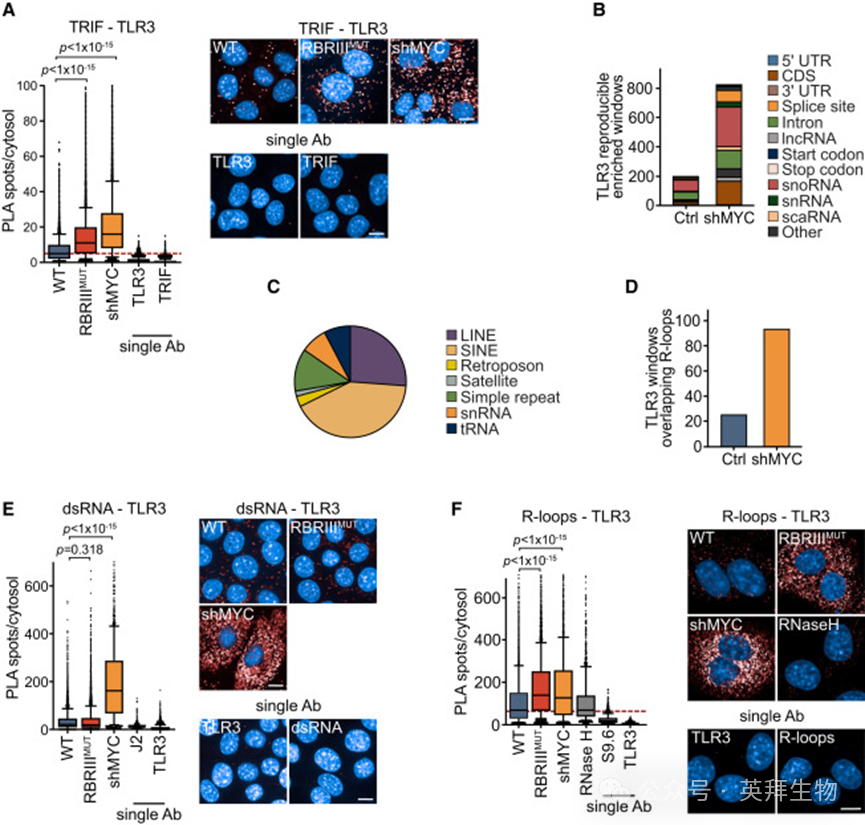
图6:MYC RNA结合抑制了RNA-DNA杂合体在TLR3上的积累
先前的研究表明,在MYC耗竭的细胞中,TLR3被dsRNA和来源于核内R-loop的RNA-DNA杂交体激活。为检测RBRIII^MUT MYC是否影响这些TLR3配体的积累,首先使用针对S9.6抗体(识别RNA-DNA杂交体)的斑点印迹评估了总RNA-DNA杂交体水平。在表达RBRIII^MUT MYC的细胞中,总RNA-DNA杂交体水平升高(图S7I)。为确定这些杂交体的基因组来源,进行DNA-RNA杂交免疫沉淀,随后进行测序(DRIPc-seq),并加入果蝇S2细胞作为spike-in对照。DRIPc-seq显示,在表达RBRIII^MUT MYC的细胞中,R-loop水平在数千个基因上显著增加(图7A-7C)。这些基因在先天免疫应答通路中富集(图7D)。在WT^MYC和RBRIII^MUT MYC细胞中,通过S9.6 PLA测量的R-loop水平与MYC结合RNA的水平相关(图7E,7F)。此外,在表达RBRIII^MUT MYC的细胞中,通过S9.6 PLA测量的R-loop与TLR3的共定位显著增加,并且该信号对RNase H处理敏感(图7G,7H)。相比之下,在WT^MYC细胞中,TLR3与dsRNA(通过J2抗体检测)的共定位增加,但在RBRIII^MUT MYC细胞中没有(图7I,7J)。此外,在表达RBRIII^MUT MYC的细胞中,TLR3与R-loop的结合增加,但TLR3与dsRNA的结合没有增加,这可以通过使用RNase H或RNase III处理来区分(图7K,7L)。这些数据表明,在表达WT^MYC的细胞中,MYC抑制dsRNA在TLR3上的积累,而在表达RBRIII^MUT MYC的细胞中,该功能得以保留;然而,表达RBRIII^MUT MYC的细胞无法抑制R-loop衍生的RNA-DNA杂交体在TLR3上的积累。因此得出结论,MYC通过其RBRIII与RNA的结合来抑制R-loop衍生的RNA-DNA杂交体在TLR3上的积累,从而防止先天免疫信号的激活。
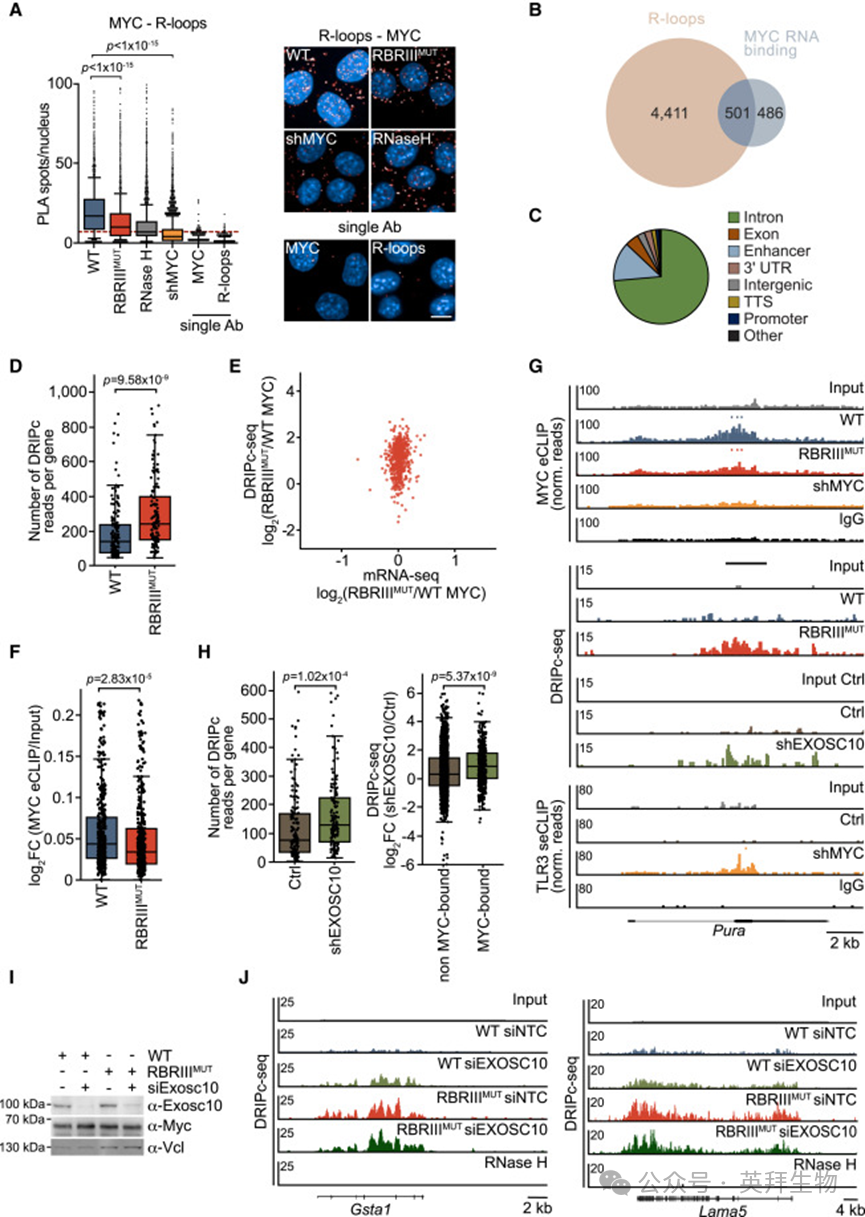
图7:TLR3结合的RNA-DNA杂合体是由MYC结合的核R-loop衍生的
结论
本研究揭示了MYC蛋白在新生RNA结合、RNA降解与先天免疫调控中的关键作用。首先,MYC可特异性结合染色质相关的新生RNA,尤其是内含子RNA,其结合与启动子DNA结合相互独立。MYC在DNA结合态与RNA结合态之间呈动态平衡,RNA积累或FACT/剪接体抑制可促使MYC从染色质重定位到新生RNA,从而形成多聚体。MYC多聚体在R-loop和dsRNA附近富集,并招募RNA外切体及相关RNA加工因子,对异常或未降解的RNA进行清除。通过体外与细胞实验,研究确认MYC是多价RNA结合蛋白,其中RBRIII区域为关键结构域,介导RNA结合、多聚化及RNA降解因子招募。RBRIII突变会削弱MYC的RNA结合和多聚能力,但不影响DNA结合。功能上,MYC通过RNA结合和多聚体形成,抑制R-loop与dsRNA在TLR3等模式识别受体上的积累,从而抑制TBK1激活和下游NF-κB/IRF信号,最终降低先天免疫反应。体内实验显示,RBRIII缺失的MYC虽保留DNA结合和细胞周期调控能力,但无法抑制先天免疫,导致肿瘤生长受限。综上,本研究揭示了一种通过RNA结合及多聚体形成来抑制先天免疫的新型MYC功能机制,即MYC作为RNA“枢纽”,协调新生RNA代谢与免疫信号,从而为肿瘤细胞提供生长优势。
参考文献
Uhl L, Aziba A, Löbbert S, Russell T, Krenz B, Montesinos F, Kannan T, Valanju OR, Schülein-Völk C, de Martines T, Bolz M, Fleischhauer D, Cossa G, Endres T, Solvie D, Gallant P, Rosenwald A, Maric HM, Papadopoulos D, Vos SM, Eilers M. MYC binding to nascent RNA suppresses innate immune signaling by R-loop-derived RNA-DNA hybrids. Cell. 2026 Mar 5;189(5):1371-1388.e29. doi: 10.1016/j.cell.2025.12.019. IF: 42.5 Q1.






