国自然热门领域之肠道菌群
GV971作为治疗阿尔茨海默症药物被批准上市,后有传言称饶毅教授举报三位知名研究人员,其中一位就是GV971的研究者耿美玉。自从GV971被批准上市后,就被广大科研人员质疑临床数据和明确的药理机制研究。我们今天主要谈论耿美玉发表在Cell Research上关于GV971通过脑肠轴影响阿尔茨海默症的论文及肠道菌群研究方向。

肠道微生物包括真细菌、古细菌、真菌以及病毒等类型,人类胃肠道中的微生物总量超过1014,其中细菌占99%以上,约1000-1150种,在食物分解吸收、抵御外界病原微生物等方面发挥重要作用。肠道菌群近年来在科学研究领域十分火热,在国自然基金申请上也十分给力。在2019年批准的国自然项目中,有210个项目与肠道菌群有关,且增长趋势明显,值得诸位研究人员长期关注。
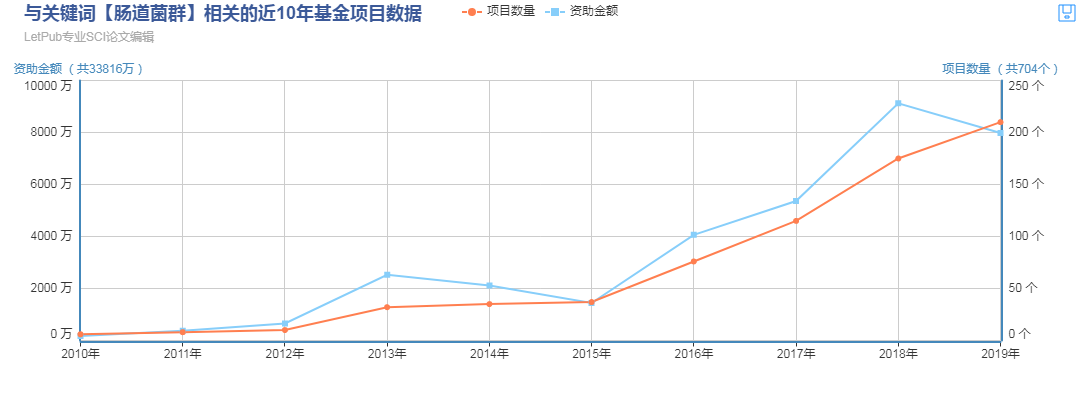
肠道菌群的实验设计非常圆滑,可以与许多方向相关联,包括中药学,预防医学,代谢生理,食品科学,消化系统疾病,循环系统,药理,肿瘤,微生物,中西医结合等诸多方向。听我说完你是不是有一点点心动,那我接下来以耿美玉的文章为例解析一下肠道菌群研究方法,这里我们不讨论文章逻辑,只说文章思路。
作者首先确认了在AD进程中,肠道菌群的改变与脑内侵润的免疫细胞具有相关性。小鼠模型使用的是5XFAD转基因(Tg)小鼠,随着AD病程进展,Tg小鼠肠道菌群组成发生了显著改变。追踪Tg小鼠菌群结构的动态变化过程发现,在Tg小鼠2-3月龄时,拟杆菌门、厚壁菌门和疣微菌门丰度最高(Bacteroides 47.3%, Firmicutes 33.0% 和Verrucomicrobia 12.2%),然而到了7-9月龄时,则以厚壁菌门为主导(Firmicutes 62.8%)。这些结果表明随着AD的进展,Tg小鼠肠道菌群的组成发生了明显的改变。
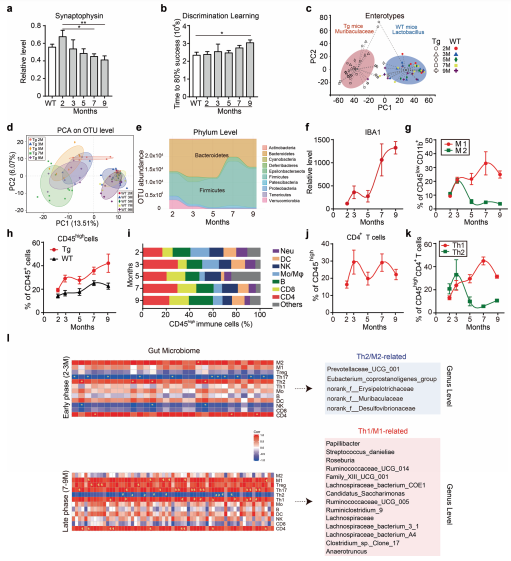
有研究提示肠道菌群参与触发大脑神经炎症。因此,作者假设在AD进程中,以上菌群变化和神经炎症有密切关系。首先,利用IBA1染色和流式细胞分析发现,Tg小鼠脑内小胶质细胞(Microglia)在2-3月龄和7-9月龄呈现两种截然不同的激活状态。在2-3月龄时,促炎的M1型和神经保护的M2型小胶质细胞活化都在增加,随着疾病的进展,促炎的M1型小胶质细胞持续增加,并在7-9月龄时达到顶峰,然而神经保护的M2型小胶质细胞在3-5月龄开始下降,之后就维持在一个较低的水平。进一步分析AD进程中Tg小鼠脑中外周免疫细胞侵润状态,发现脑内外周侵润的CD45high细胞比例显著增高,并且CD4+T细胞的两个主要亚型Th1和Th2表现出和促炎的M1型、神经保护的M2型小胶质细胞相似的变化过程。显然,该研究表明随着肠道菌群的失衡,脑内的神经炎症模式转为以Th1细胞和M1型小胶质细胞活化为主导。那么在AD的进程中,肠道菌群的丰度和大脑免疫细胞的变化是否有关联呢?这些结果表明,在AD的进程中,肠道菌群变化和脑内免疫细胞以及神经炎症密切相关。
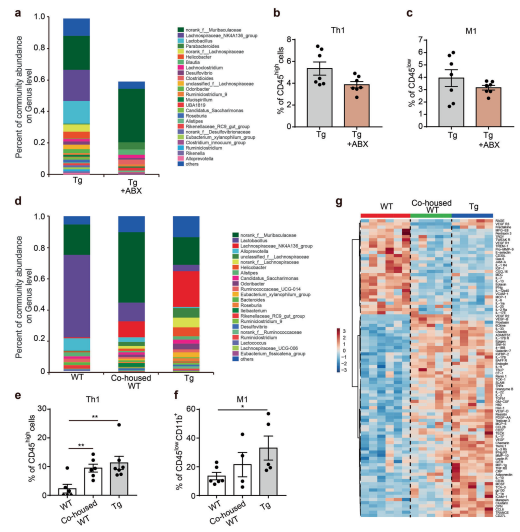
作者进一步从正反两个方面证实了肠道菌群是大脑免疫细胞浸润以及小胶质细胞激活所必需的。一方面利用抗生素处理Tg小鼠,使肠道菌群丰度显著降低,这时脑中侵润的Th1细胞比例和M1型小胶质细胞的活化也明显降低。同窝饲养实验从另一个角度证实了肠道菌群对脑内神经炎症的驱动作用。同窝的野生型(WT)小鼠由于长期暴露于Tg小鼠的粪菌中,其体内的菌群组成更接近于Tg小鼠,使得其脑中Th1、M1细胞的比例显著升高、细胞因子的表达谱和认知功能也更接近于Tg小鼠。短期的粪菌移植实验也同样证实,正常小鼠接受Tg小鼠粪菌后,脑中Th1细胞比例明显增加。相反,Tg小鼠接受正常小鼠粪菌后,脑中Th1细胞比例明显减少。这些结果都表明,在AD进程中,肠道菌群改变可以驱动脑内外周免疫细胞侵润以及神经炎症反应。
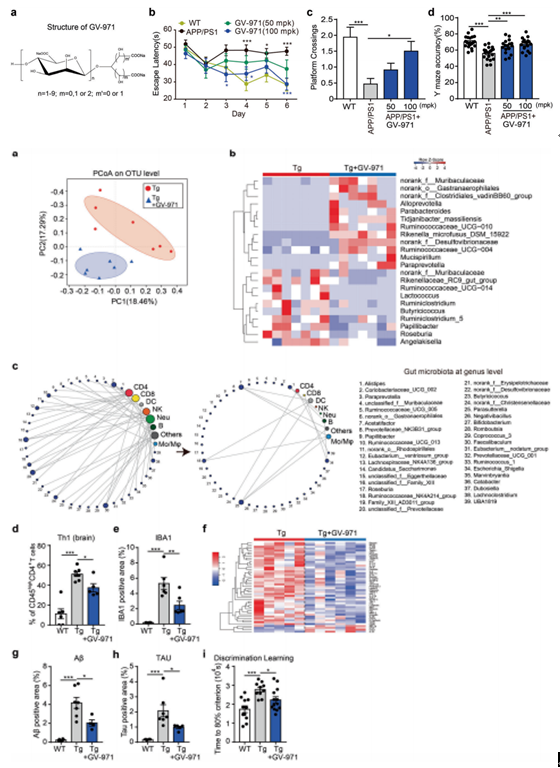
接下来 “大明星”GV971就要登场啦。通过小鼠行为学实验表明GV-971对认知障碍表现出改善作用。糖类分子是肠道菌群的营养来源,所以作者想看一下GV971是否对肠道菌群有影响。作者发现5XFAD转基因小鼠(Tg)口服GV-971一个月后,肠道菌群的组成更接近于野生型小鼠,且肠道菌群的分布发生了明显的双向变化。与肠道菌群的变化一致,GV-971治疗Tg小鼠后,之前脑内免疫细胞与肠道菌群间的相关性被打破,脑内促炎性Th1细胞比例下降,小胶质细胞的活化水平也显著降低,同时,脑内多种细胞因子水平广泛下降。并且,GV-971的治疗显著降低了Tg小鼠脑内Aβ斑块沉积和Tau蛋白的磷酸化,对Tg小鼠辨别学习能力也有明显的改善作用。这些结果表明,GV-971可以通过调节肠道菌群改善AD小鼠神经炎症和认知功能障碍。
许多研究表明肠道菌群可以通过代谢产物影响宿主的免疫系统。在AD的进程中,肠道菌群是否通过代谢产物调节大脑神经炎症。作者发现Tg小鼠粪菌培养上清可以刺激CD4+T细胞更多地分化成促炎性Th1细胞,说明菌群产生的相关代谢产物可以调节免疫细胞分化。通过非靶向代谢组学分析发现WT、Tg和GV-971治疗的Tg小鼠粪便中存在31种差异的代谢产物,这些代谢产物在Tg小鼠中与WT小鼠相比显著升高或降低,同时这种改变在GV-971处理后可以明显逆转。通过通路富集,作者发现这些代谢物主要集中在一些氨基酸相关代谢通路,特别是苯丙氨酸(Phenylalanine)等相关通路。
氨基酸可以通过特定的转运体被免疫细胞摄取,从而驱动免疫细胞的分化和增殖。作者检测了苯丙氨酸和异亮氨酸转运体SLC7A5的表达水平。他们发现在Th1细胞中存在SLC7A5表达。用13C同位素标记苯丙氨酸表明Th1细胞能够摄取苯丙氨酸,并且这种摄取可以被SLC7A5抑制剂阻断。进一步研究发现苯丙氨酸或异亮氨酸能刺激CD4+T细胞分化成Th1细胞,并可刺激Th1细胞的增殖。当给WT小鼠腹腔注射苯丙氨酸或异亮氨酸时,小鼠血液中Th1细胞的比例也显著增加。
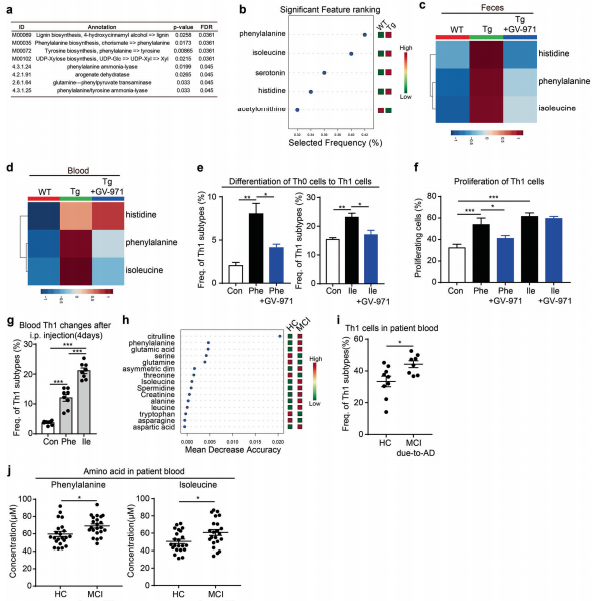
GV-971 处理一个月可明显降低Tg小鼠粪便和血液样本中苯丙氨酸和异亮氨酸的含量,并且减少苯丙氨酸或异亮氨酸所诱导的Th1细胞的分化,同步降低苯丙氨酸诱导的Th1细胞增殖。为了进一步验证上述小鼠模型上的研究结果是否在临床样本上具有可重现性,作者又比较了轻度认知障碍AD患者和对应年龄段的健康人血液中苯丙氨酸、异亮氨酸和Th1免疫细胞等含量的差别,结果发现轻度认知障碍AD患者Phe/Ile水平和Th1细胞含量比例较健康人均明显升高,提示了该工作具有潜在的临床转化价值。
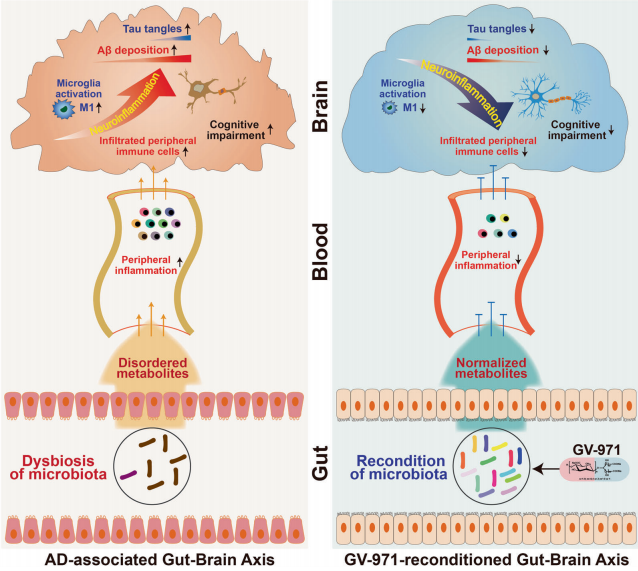
综上,在AD进程中,伴随Aβ的沉积以及Tau蛋白的磷酸化的发生,肠道菌群的组成发生变化,继而导致代谢产物异常,异常的代谢产物刺激外周免疫炎症,促使炎性免疫细胞Th1向大脑侵润,引起脑内M1型小胶质细胞的活化,导致AD相关神经炎症的发生,最终导致认知功能障碍。口服GV-971能够重塑肠道菌群,降低异常代谢产物,阻止外周炎性免疫细胞向大脑的侵润,抑制神经炎症,同时减少Aβ的沉积和Tau蛋白的磷酸化,从而改善认知障碍,达到治疗AD的目的。
最后我谈一下关于GV971这个抗AD的药物我个人的看法,临床前试验表明,GV971可能具有多靶点作用,包括β淀粉样蛋白、抑制神经系统炎症反应、重塑肠道菌群、抑制胆碱酯酶作用。但临床机制并未验证,包括最为核心的β淀粉样蛋白通路。GV971的试验周期只有36周,时间跨度不够大,并不能说明长期作用。GV971只能说是给我们一个新的希望,在全球范围内临床试验研究结束之前,我们还需要保持冷静的态度。毕竟绿谷药业的黑历史太多,抗癌靠保健品也是优秀啊,怎么看怎么像权健;那个宣传路子真像保健品。当然我们还需等待后续结果。就是这样,下回带大家看点别的,再见!






