肝星状细胞自噬抑制EV释放改善肝纤维化
研究背景:
自噬是真核生物的一种降解过程,称为自噬体的双膜小泡与溶酶体融合以降解胞浆蛋白和细胞器。自噬有助于肝内环境的稳定,其调节失调与一些慢性肝脏疾病有关。在肝细胞中,自噬已被证明具有保护作用,而在肝星状细胞(HSCs)中,自噬被提出通过脂噬(一种选择性的脂滴降解)诱导其激活。然而,自噬抑制剂雷帕霉素靶点(mTOR)促进星状细胞的活化和肝纤维化。因此,破译自噬参与的纤维化信号放大微调机制将提高我们对肝纤维化的理解。
在肝脏中,受损肝细胞和窦状内皮细胞(LSECs)产生的细胞外囊泡(EVs)可诱导HSC的活化和迁移。有趣的是,肝损伤后EV释放增加,而自噬抑制或溶酶体降解抑制与EV释放增加有关。然而,自噬如何调节前纤维化的HSC来源的EV的生物发生,目前仍缺乏了解。
在本研究中,作者证明了HSCs通过mTOR抑制自噬和激活RHOR相关蛋白激酶1 (ROCK1)信号来释放EV。此外,这种EV释放机制参与了肝纤维化进程。 总之,HSC自噬通过减少纤维化HSC来源的EV释放来减轻肝纤维化。本文于2020年5月7日发表在Journal of Hepatology(IF:18.946)杂志上。
结 果:
1、PDGF抑制自噬,增加EV释放
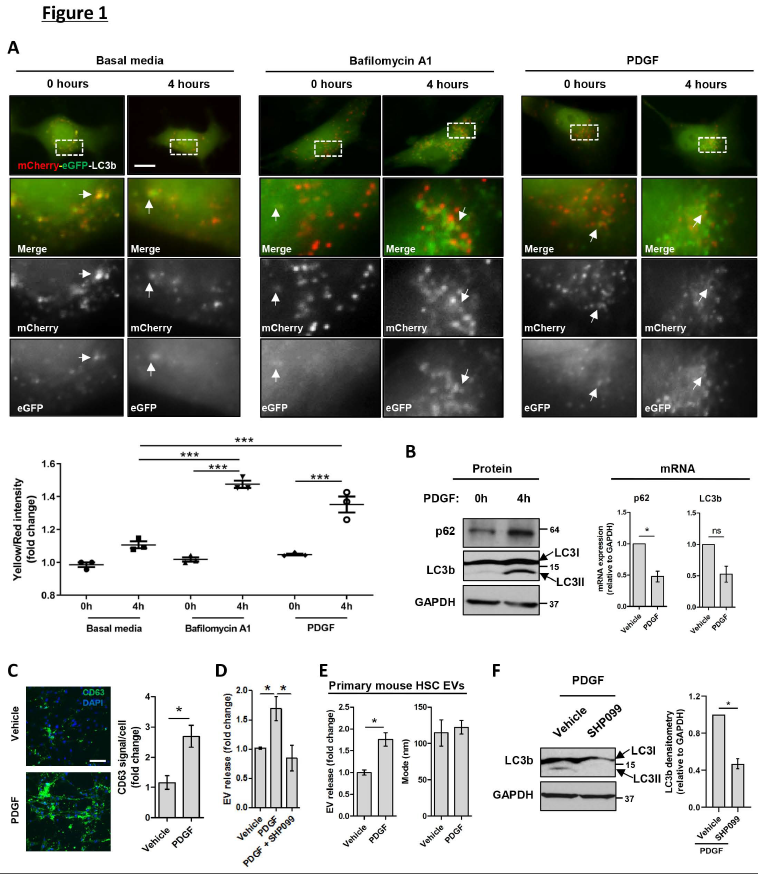
首先验证假设,在HSCs中,PDGF刺激模型抑制自噬以增加EV释放。用mCherry-eGFP-LC3b质粒转染LX2细胞(人肝星状细胞系),用自噬降解抑制剂bafilomycin A1或PDGF处理LX2细胞。正如预测的,与载体(图1A左)相比,bafilomycin A1处理增加了eGFP+-mCherry+自噬体池(黄色)(图1A中),导致黄/红比例增加(图1A图),提示自噬抑制。与bafilomycin A1相似,与基础培养基比较,PDGF在处理4h时提高了黄/红比例(图1A右),首次证明PDGF抑制自噬降解。
与这些结果一致,PDGF处理导致人肝星状细胞的自噬体LC3b和sequestosome-1 (p62) 蛋白质含量增加,但PDGF并没有增加LC3b或p62 mRNA水平(图1B,右),这表明蛋白质水平的增加是由于自噬降解的减少,而不是由于p62和LC3b的重新转录表达。PDGF介导的自噬抑制与原代HSC细胞MVB池的CD63+增加(图1C),以及人和小鼠HSC细胞来源的EV释放的增加相关(图1 d- e)。PDGF的关键下游信号分子之一是SHP2,通过竞争性抑制剂SHP099抑制SHP2,消除PDGF介导的EV释放(图1D)。SHP099还降低了LC3b蛋白水平(图1F),表明SHP2抑制促进了自噬降解。这些结果支持了HSCs中PDGF信号抑制自噬并增加EV释放的观点,提示自噬可能抑制EV释放。
2、EV释放受自噬激活因子REDD1调控
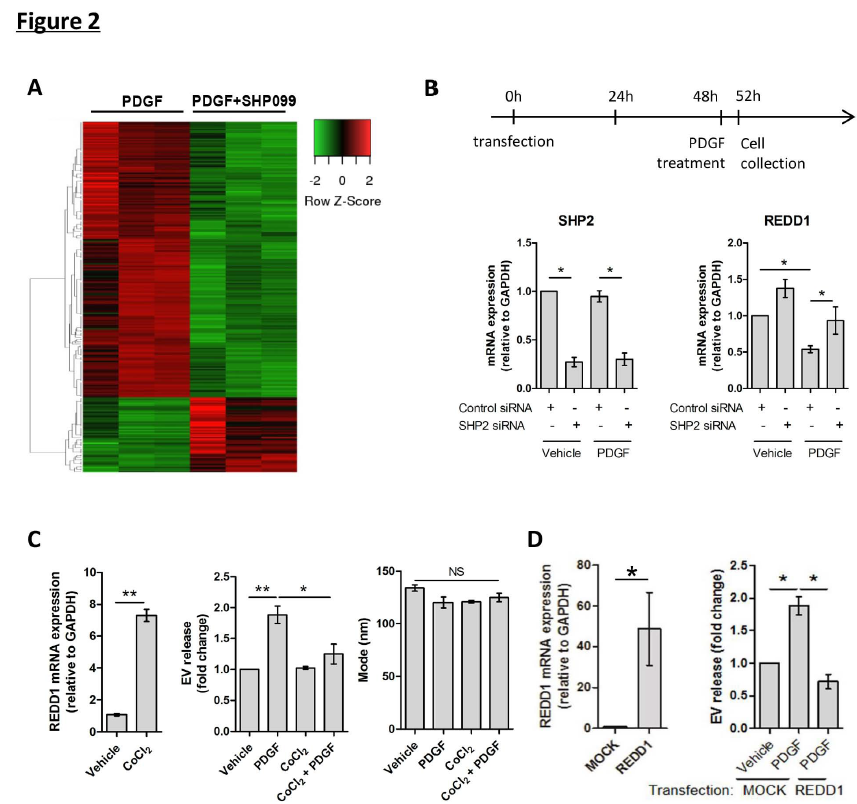
使用PDGF/SHP2模型进一步研究自噬如何抑制纤维性EV释放。为此,用PDGF+/-SHP099处理人原发性HSCs,然后全转录组RNA测序检测 (图2)。近25%的基因被SHP099上调(图2A)。结果得到REDD1,REDD1是mTOR的内源性抑制剂,是SHP2的首要靶点之一。在对照和PDGF处理和siRNA敲除SHP2均导致REDD1上调(图2B)。 这些结果表明,PDGF和SHP2负调控mTOR抑制剂和自噬激活剂REDD1的表达,提示REDD1在EV释放中的作用。
接下来,通过刺激REDD1的表达来了解REDD1在肝纤维化和HSC衍生的EV释放中的作用。使用REDD1刺激物 CoCl2(图2C,左)。在EV或PDGF存在下,用CoCl2处理原代人HSC。REDD1表达减弱了PDGF介导的EV释放(图2C,中间),而对EV大小没有影响(图2C,右)。接下来,我们在LX2细胞中过表达REDD1(图2D,左)。REDD1的过表达显着降低了HSC衍生的EV释放(图2D,右)。 总之,这些结果表明,REDD1是一种自噬激活剂和mTOR抑制剂,是HSC来源的纤维化EV释放的负调节剂。
3、mTOR信号通过抑制自噬和激活ROCK1来增加HSC诱导的EV释放
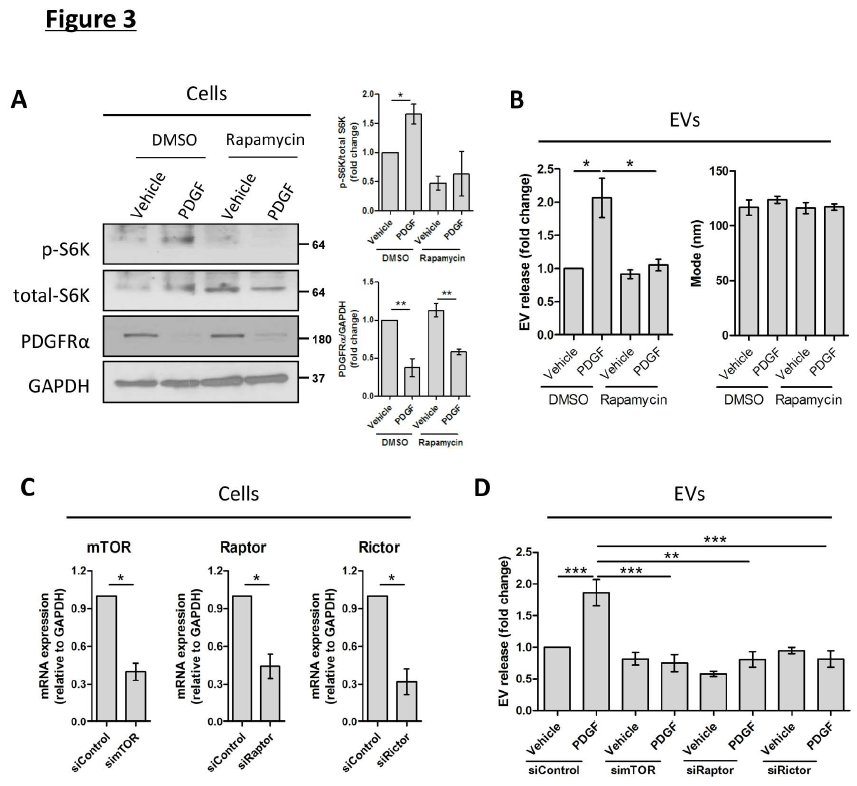
为了进一步了解自噬如何影响纤维化EV释放,研究了自噬抑制剂mTOR在HSC衍生的EV释放中的作用。结果表明,雷帕霉素对mTOR的抑制作用减弱了PDGF介导的EV释放,而对EV的大小没有任何影响(图3B)。 然后,在人HSC上进行了mTOR结合蛋白沉默,mTOR的调节相关蛋白(Raptor)和mTOR雷帕霉素不敏感相关蛋白(Rictor)沉默(图3C)。 与雷帕霉素结果一致,siRNA引起的mTOR敲除消除了PDGF介导的EV释放(图3D)。 Raptor或Rictor siRNA介导的敲低也获得了类似的效果(图3D),证实mTOR信号传导促进EV释放。
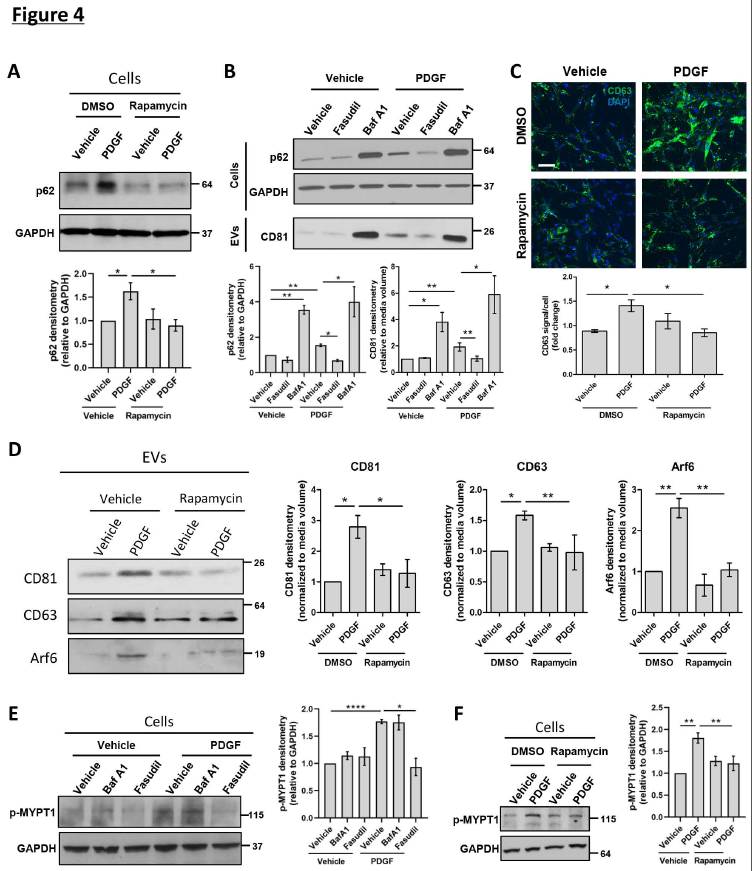
接下来,研究了原代人HSC中mTOR依赖的EV释放的起源。如图PDGF增加了p62蛋白水平,该水平被雷帕霉素减弱(图4A),表明PDGF通过mTOR抑制自噬。此外,通过bafilomycin A1(图4B)造成的自噬抑制作用显着增加了EV级分中的外泌体标记物CD81以及微泡标记物Alf6的表达。根据这些结果,作者研究了mTOR信号在原代人HSC中MVB的作用,其中CD63是MVB和外泌体标记。用PDGF处理细胞可增加MVB,雷帕霉素可将其消除,如免疫荧光法所证实(图4C)。与此相一致,雷帕霉素降低了PDGF介导的外泌体释放,如EV中CD81和CD63蛋白水平的降低得以证明(图4D)。这些结果表明,mTOR信号传导诱导外来体释放。
与外泌体相反,微泡释放取决于ROCK1的活性。因此,接下来研究了mTOR信号传导对ROCK1活性和微泡释放的影响。PDGF处理原发性人HSC细胞激活了ROCK1信号,表现为ROCK1下游信号分子,肌球蛋白磷酸酶靶标亚基1(MYPT1)的磷酸化水平升高(图4E)。通过用ROCK1抑制剂fasudil处理HSC可以消除这种情况(图4E)。随后,fasudil对ROCK1的抑制作用显着降低了PDGF介导的EV释放,如微泡标志物Arf6和外泌体标志物CD81表达下调,表明外泌体和微泡释放机制之间存在相互影响。PDGF介导的ROCK1活性也被雷帕霉素抑制,如MYPT1磷酸化减弱(图4F)表明PDGF通过mTOR诱导ROCK1活化。此外,雷帕霉素降低了PDGF介导的微泡释放,这通过降低EV馏分中的Arf6蛋白水平来证明(图4D)。这些数据表明,mTOR信号传导诱导微泡释放。
总之,mTOR信号通过抑制MVB的自噬降解诱导外泌体释放,并通过激活ROCK1信号传导来诱导微泡释放,提供了对PDGF介导的纤维化EV释放的机制的见解。
4、mTOR介导的EV诱导HSC细胞的体外迁移
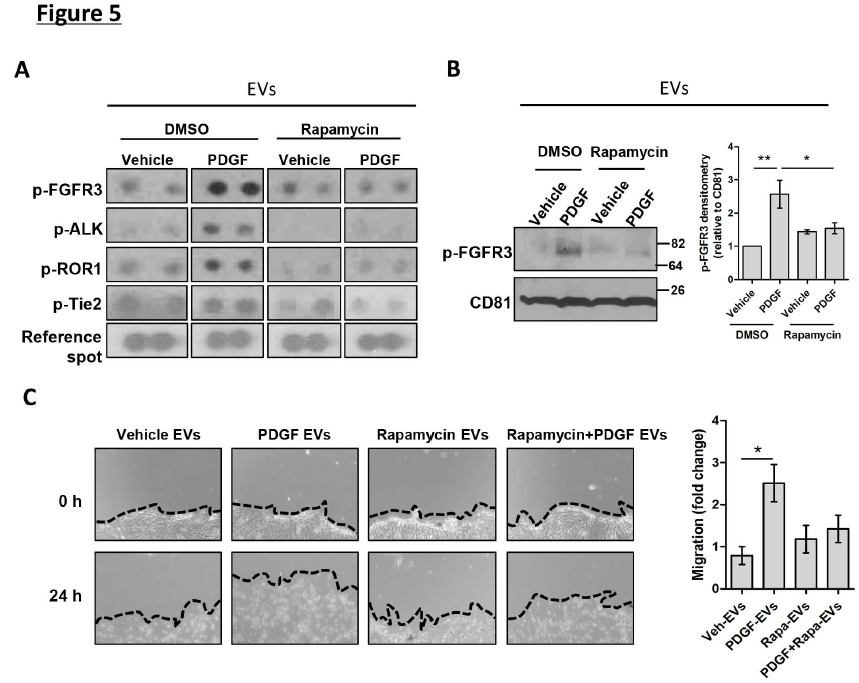
受体酪氨酸激酶(RTK)信号在纤维化中占据关键地位,因此我们利用磷酸化RTK蛋白阵列评估了EV含量。RTK阵列结果显示,PDGF处理后的EV中存在几种磷酸化的RTK,例如成纤维细胞生长因子受体3(FGFR3),内膜内皮细胞激酶(Tie2),间变性淋巴瘤激酶(ALK)和受体酪氨酸激酶-孤儿受体1(ROR1)(图5A)。受PDGF上调,被雷帕霉素降低最显著的是磷酸FGFR3(图5A),它参与成纤维细胞迁移。这些数据表明,mTOR信号不仅促进了EV的释放,而且还通过激活RTK介导EV的富集。由于以前已确定RTK与细胞迁移有关,所以接下来验证这些富含RTK的EV对HSC迁移的影响。与衍生自对照细胞的EV相比,衍生自PDGF处理的EV显着增加了受体HSC的迁移(图5C)。总之,这些结果表明,mTOR促进了转移前的RTK富集的EV的释放。
5、体内删除HSC特异性SHP2肝纤维化下降
由于SHP2是mTOR依赖性EV释放的上游调节剂,在全肝裂解物中,与健康个体相比,肝硬化患者的SHP2升高(图6A)。因此,验证HSC特异性SHP2缺失对肝纤维化建立的影响,由 CCl4 给药6周诱导肝纤维化。然后收集肝脏,并用天狼星红染色和WB进行分析。如预期的那样,慢性CCl4处理后同窝对照小鼠(SHP2f1 / f1)的肝胶原蛋白I,αSMA蛋白水平和天狼星红染色增加(图6B-C)。然而,如胶原蛋白I,αSMA和天狼星红染色的蛋白质水平所表明的,当在HSC(SHP2ΔHSC小鼠)中选择性删除SHP2基因时,肝纤维化显着减少。总之,HSCs中SHP2的选择性缺失显着减弱了肝纤维化。
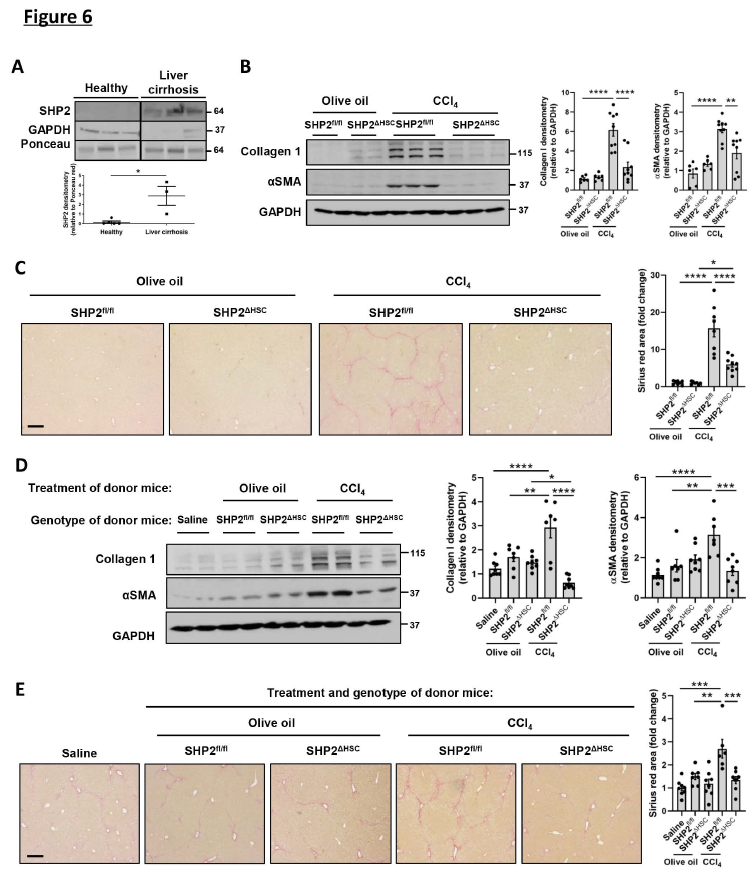
6、HSC特异性 SHP2敲除的老鼠EV减少了WT老鼠中 CCl4介导的肝纤维化
前文证明,由PDGF处理的HSC衍生的EV具有促纤维化作用,而SHP2对肝纤维化至关重要(图6B-C)。因此,接下来研究HSC特异性SHP2如何影响循环EV的纤维化潜力,以及这些EV如何在体内影响肝纤维化。与生理盐水对照相比,橄榄油处理的SHP2fl / fl或SHP2ΔHSC供体小鼠的EV不会影响肝纤维化。 但是,如WB和Sirius red(图6D-E)所示,来自经CCl4处理的SHP2fl / fl对照小鼠的EV显着增加了CCl4诱导的肝纤维化(图6D-E),表明这些EV具有成纤维性。 此外,从CCl4处理的SHP2ΔHSC小鼠中分离出的EV显着减少了CCl4诱导的肝纤维化(图6D-E),这表明在HSC中选择性删除SHP2会降低EV的纤维化潜力。 总之,HSC中SHP2的选择性缺失显着减弱了循环EV的纤维化特性。
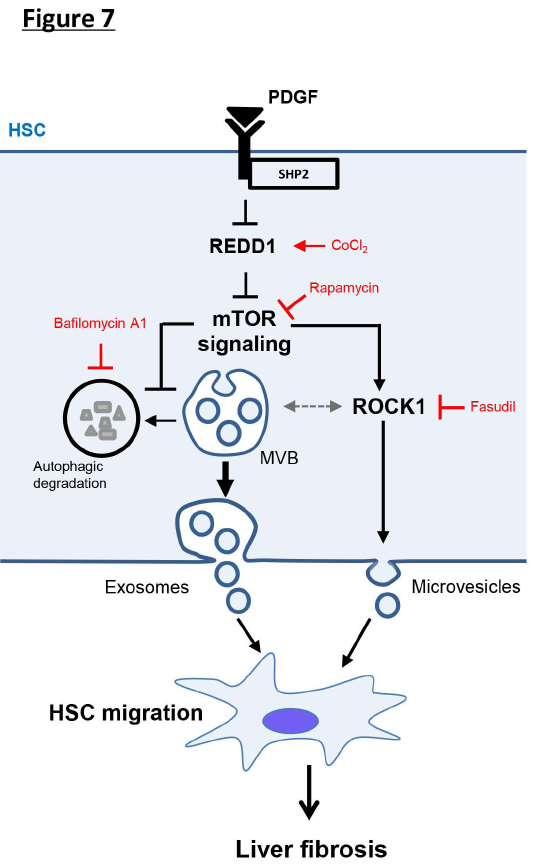
总之,HSC中的SHP2通过抑制自噬,REDD1和激活mTOR途径来增强纤维化电动汽车的释放,从而发挥其促纤维化作用。 SHP2-mTOR信号的抑制可能作为治疗肝纤维化的新靶标。






