分泌体和外泌体用于肺纤维化治疗啦!
特发性肺纤维化(Idiopathic pulmonary fibrosis, IPF)是一种致命的、无法治愈的肺间质疾病,持续损伤可导致瘢痕组织形成。随着纤维化变厚,肺组织失去了促进气体交换和为细胞提供所需氧气的能力。目前,除了肺移植外,IPF几乎没有治疗选择,也没有有效的治疗方法。在这里,作者提出了利用肺球状细胞分泌体(LSC-Sec)和外泌体(LSC-Exo)吸入来治疗不同模型的肺损伤和纤维化。本文于2020年2月发表在Nature Communication(IF:11.878)杂志上。
结 果:
1、细胞分泌体减轻博莱霉素(Bleo)诱导的纤维化和凋亡
小鼠PF模型中肺部炎症通常持续7天,并在第9天进入纤维化阶段,因此,作者在第10天开始干预,以保证治疗处于PF疾病阶段(Fig. 1a)。在首次组织学检查后,所有接受Bleo处理组均表现出出血性坏死(Fig. 1b), LSC-Sec或MSC-Sec处理均可减少坏死。由于Bleo诱导DNA损伤,检测了细胞分泌体处理对细胞凋亡的影响(Fig. 1c-f)。与PBS组相比,LSC-Sec治疗导致肺细胞凋亡减少(Fig. 1d-f)。LSC-Sec和MSC-Sec处理均通过保留肺泡上皮结构(Fig. 1g–h)和减少胶原沉积(Fig. 1i–k)来减少纤维化。只有LSC-Sec能够减少纤维化面积并将肺泡上皮损伤恢复到健康水平(sham对照组)。
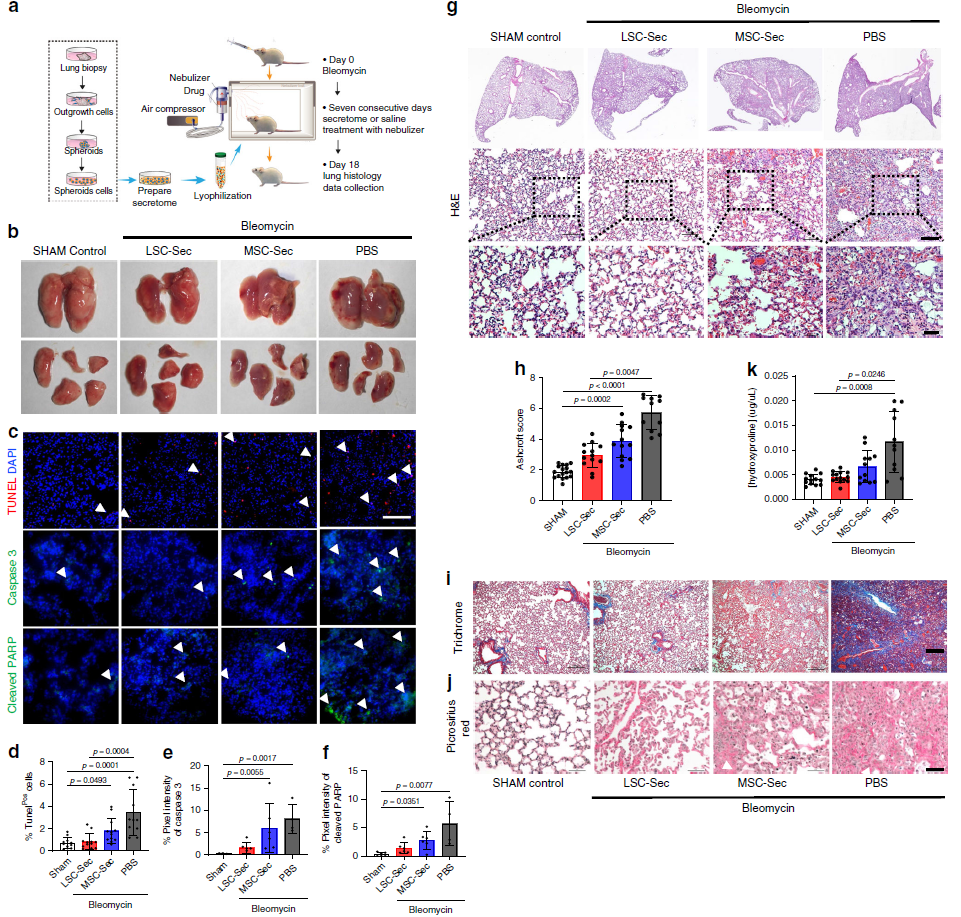
图1 LSC-Sec吸入逆转博莱霉素诱导的肺泡上皮细胞损伤
2、分泌体吸入促进血管和肺泡修复
肺泡是远端气道的末端结构。肺泡上皮由肺泡1型上皮细胞(AT1)和肺泡2型上皮细胞(AT2)组成,前者介导气体交换,后者产生和释放肺表面活性剂、抗氧化剂、细胞因子/趋化因子和其他对肺防御、损伤反应和稳态重要的分子。因此,检测了分泌体处理后Bleo损伤时AT1和AT2分布的变化,以评估上皮损伤和挽救(Fig. 2a)。AT1标记水通道蛋白5(AQP5)的免疫染色显示LSC-Sec处理能够逆转由Bleo引起的上皮损伤(Fig. 2a-d)。 但是,与PBS处理组相比,在LSC-Sec处理组中肺蛋白溶解产物的免疫印迹显示AQP5蛋白显着增加(Fig. 2e, f)。 此外,LSC-Sec处理显着提高了表面活性蛋白C(ProSPC +)阳性AT2细胞的增殖(Fig. 2a-c),该细胞增殖并分化为AT1细胞。这种现象在MSC-Sec处理中仍然发生,但程度较低,与PBS组无显着差异。只有LSC-Sec处理能够增加PF肺中von Willebrand因子(vWF +)阳性脉管系统的表达(Fig. 2a, b)。与PBS组相比,在分泌体处理组中,ProSPC和vWF肺蛋白水平的免疫印迹显示增加的趋势(Fig. 2e, f)。
同时,通过测量α-平滑肌肌动蛋白(αSMA,指示IPF的成肌纤维细胞标志物)的蛋白质水平来检查纤维化反应(Fig. 2e, f)。与PBS处理的对照组相比,LSC分泌体处理组αSMA表达下降。与PBS组相比,两个分泌组中肺组织中基质金属蛋白酶(MMP)2的蛋白表达均呈增加趋势。采用细胞因子阵列来探究全身细胞因子表达,作为免疫原性的量度。有趣的是,与PBS对照相比,LSCSec的促炎性IL-4表达呈下降趋势(Fig. 2g, h)。IL-4是呼吸道疾病(例如哮喘)中促炎功能的重要介质。
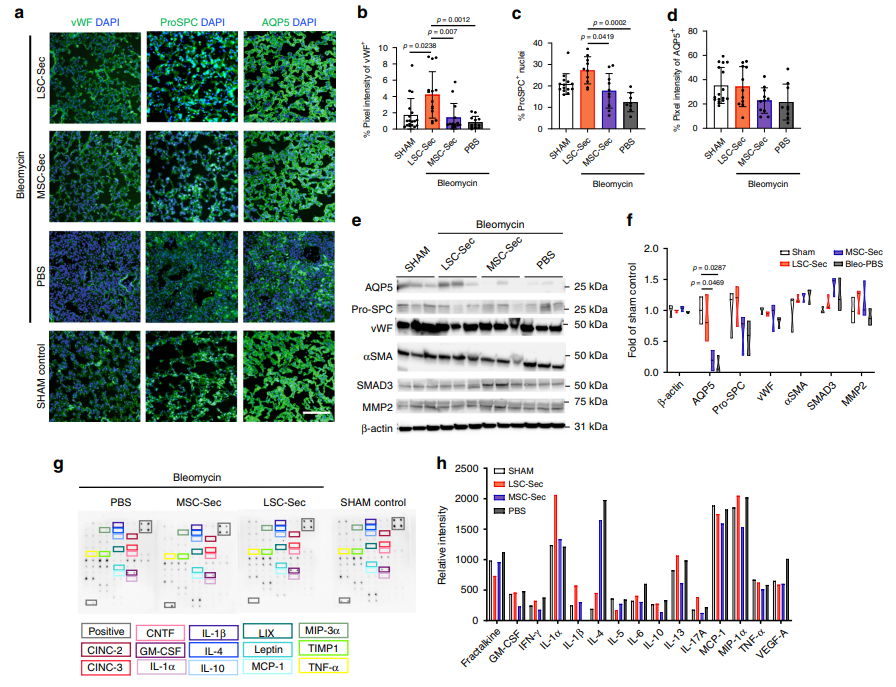
图2 LSC-Sec吸入处理促进肺泡修复
3、LSC分泌体治疗二氧化硅诱导的肺纤维化
为了评估LSC-Sec的再生作用可以被应用于其他的肺损伤模型,使用二氧化硅诱导肺纤维化。与之前的Bleo研究一样,使用喷雾器连续7天给予可吸入细胞分泌体或生理盐水(Fig. 3a)。在所有处理组,对凋亡细胞的影响均无显着差异(Fig. 3b)。但是,与PBS处理组相比,LSC-Sec能够显着降低纤维化的严重程度(Fig. 3c, d)。二氧化硅诱导的结节周围的纤维化组织强度较小且分布较广,但在LSC-Sec和MSC-Sec处理组中均持续存在(Fig. 3c-f)。 与PBS处理相比,细胞分泌蛋白质组处理减少了胶原蛋白沉积并减少了肺泡上皮损伤,尽管胶原蛋白沉积仍显着高于健康假对照组(Fig. 3f, g)。
对AQP5 + AT1细胞和ProSPC + AT2细胞的检查显示,在所有二氧化硅损伤的肺中,两种肺泡标记物均无明显下降(Fig. 3h-j)。但是,与PBS组相比,LSC-Sec能够通过促进ProSPC + AT2细胞表达并维持AQP5 + AT1细胞群体来减少肺泡上皮损伤。表达AQP5的AT1细胞不存在纤维化结节,但ProSPC +和vWF +细胞的表达仍然有限(Fig. 3h-k)。
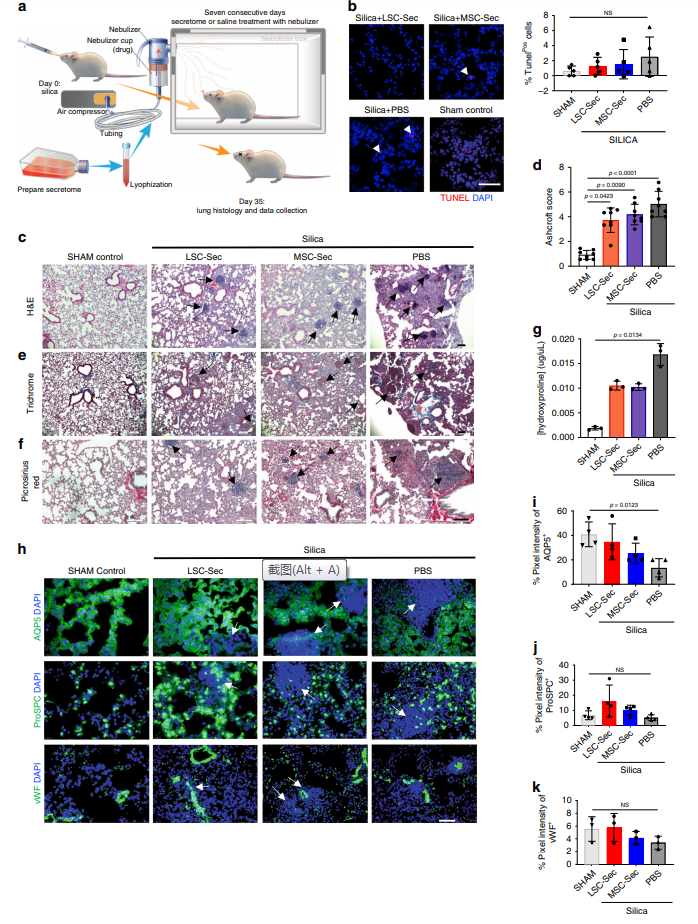
图3二氧化硅损伤后小鼠肺的修复和纤维化
4、LSC分泌体和外泌体的蛋白质组成
为了更好的了解上述观察到的LSC-Sec的再生能力的分子过程,作者尝试构建它的蛋白组的组成。结果发现虽然这三株LSC细胞系来自不同性别、种族和年龄的个体(图4a),但却具有非常相似的蛋白质组(Fig. 4a)。在共享的蛋白中,29.6%被标注为具有已知分泌膜受体的胞外蛋白,47.5%被标注为不存在已知分泌途径的胞质蛋白(Fig. 4b)。在三个LSC-Sec中鉴定的103个细胞外蛋白中,有20个的相对丰度较高(Fig. 4c)。此外,在LSC-Sec中发现的102种常见细胞外蛋白中,约有一半也在LSC-Exo中发现(Fig. 4e)。Fig. 4d和Fig. 4f分别是LSC-Sec和LSC-Exo中鉴定的胞外蛋白的GO分析。
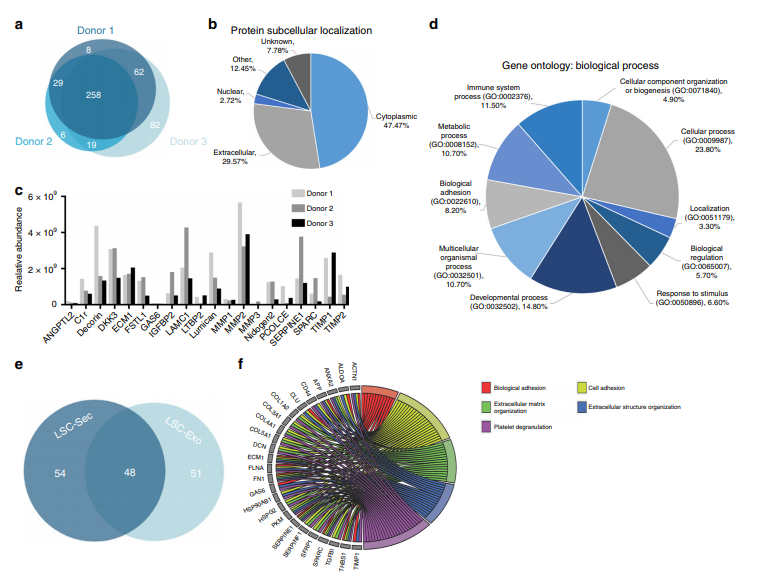
图4 LSC-Sec和LSC-Exo的蛋白组分析
5、LSC外泌体的治疗作用
通过大小、形态和常见的外泌体标记(CD63、CD81和TSG101)对LSC-Exo和MSC-Exo进行了表征(Fig. 5a-c)。所有分泌体和外泌体处理组均在维持正常肺结构(Fig. 5e-f)和减少纤维化(Fig. 5h)、肺凋亡和胶原沉积(Fig. 5j-i)方面均显示出治疗效果。值得注意的是,与PBS处理组相比,只有LSC-Sec和LSC-Exo显著降低了胶原沉积。此外,只有LSC-Sec可显著降低纤维化(Ashcroft评分)至与sham对照组相似的水平。治疗组的肺αSMA蛋白含量没表现明显下降的趋势(Fig. 5j)。LSC-Sec和LSC-Exo处理减缓了肺泡上皮和血管损伤,并降低纤维化反应,表现为AQP5 +和vWF +细胞增加和αSMA +细胞减少(Fig. 5k-n)。
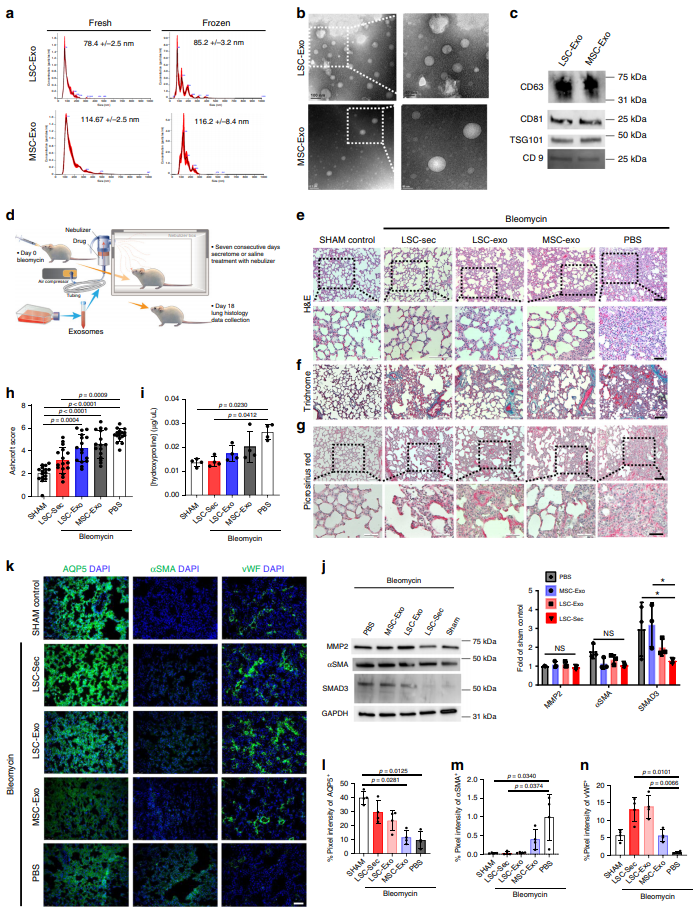
图5外泌体吸入处理肺纤维化大鼠的治疗潜力
6、外泌体治疗改善Bleo诱导后的肺功能
作者检测发现MMP-2和MCP- 1的表达显著响应LSC-Sec和LSC-Exo治疗(Fig. 6a)。接下来,预测LSC-Sec和LSC-Exo治疗受损肺结构和纤维化的临床影响(Fig. 6b)。与预期一样,吸气量(IC)、阻力(Rrs)、顺应性(Crs)、迟滞面积、用力呼气容积(FEV)与用力肺活量(FVC)之比较基线均下降了(Fig. 6c-e, g, h),且呼吸弹性(Ers),顺应性的倒数,在中点分析时增加(Fig. 6f)。总之,所有Bleo动物的肺功能持续受损,如预期的那样,肺损伤,导致组织硬度和弹性反冲增加。
在终点分析中,通过分泌体和外泌体治疗后仅部分恢复了肺功能。LSC-Sec,LSC-Exo或MSC-Exo治疗后,吸气能力和呼吸顺应性均显着改善(Fig. 6c-e)。仅使用LSC-Exo治疗,呼吸阻力有明显恢复(Fig. 6d)。治疗后弹性,滞后面积和FEV / FVC比均无明显变化。

图6外泌体治疗改善Bleo诱导后的肺功能和外泌体miRNA分析
7、LSC和MSC外泌体的microRNA分析
对LSC-Exo和MSC-Exo进行了小RNA深度测序,并分析了它们的miRNA组成的差异。在这些LSC-Exo和MSC-Exo样本中,总共检测到超过600种独特的miRNA,这表明外源性miRNA在这些样本中可能具有多种调控作用。除去丰度较少的miRNA后,仍有142个miRNA用于进行下游分析(Fig. 6i, j)。在两种外泌体类型中总共发现42个差异表达的miRNAs。LSC-Exo中上调最多的miRNAs是hsa-miR- 99a-5p和hsa-miR-100-5p(Fig. 6j)。它们也是LSC-Exo中含量最高的两个miRNAs,属于miR-99家族(Fig. 6k)。
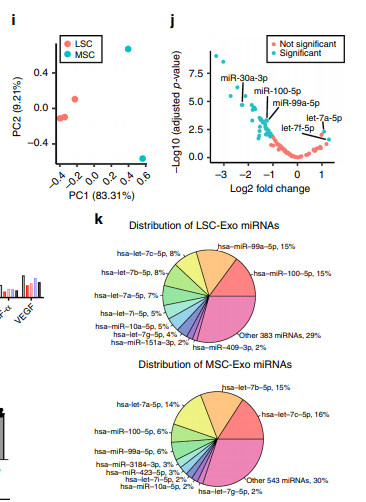
图7外泌体治疗改善Bleo诱导后的外泌体miRNA分析
总而言之,本文报告了新型脱细胞治疗剂,即LSC-Sec和LSC-Exo,在啮齿动物中博莱霉素诱导和二氧化硅诱导的肺纤维化治疗中被证明是安全有效的。本文证明,LSC-Sec介导的再生机制可能与外泌体,MMP-2活性以及细胞分泌物中发现的大量蛋白质有关。分泌体和外泌体的免疫原性远低于其亲本,并且这些因子的施用可以克服干细胞的局限性,同时保持相似的治疗效果。在LSC-Sec中对miR-30a和miR-99和let-7家族的miRNA的鉴定值得进一步研究,因为已知miR-30a在IPF患者以及miR-99和let-7家族中被下调。IPF目前是一种不可治愈的呼吸系统疾病,发病率和死亡率均在上升,目前没有有效的疗法,LSC-Sec和LSC-Exo为IPF疗法的发展提供了新的希望。






