干细胞来源的外泌体与细胞焦亡
焦亡是新近发现的程序性细胞死亡方式,可导致细胞快速裂解和炎症物质的释放。circRNA是一类具有各种生物学功能的非编码RNA,外泌体是不同类型的细胞分泌的包含许多非编码RNA的细胞外囊泡,介导细胞间的通讯。外泌体circRNA与焦亡碰撞出哪些火花,这篇文章告诉你。

技术路线:

结 果:
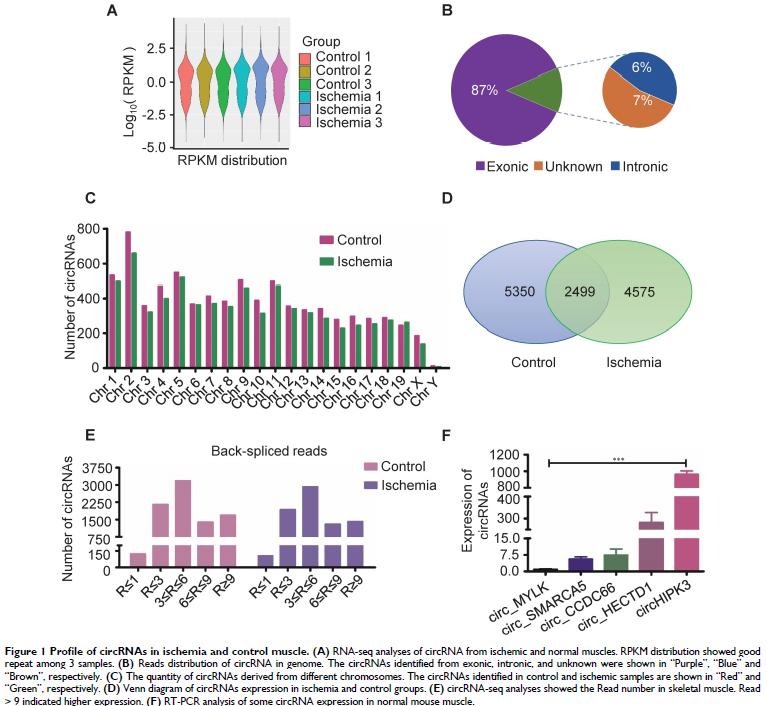
1. 肌肉组织中circRNA分析
缺血性肌肉组织和正常肌肉组织RNA测序,鉴定circRNA表达谱。源自HIPK3基因第2外显子的circRNA(circHIPK3)在组织中具有高表达水平,表明circHIPK3可能在急性缺血诱导的骨骼肌损伤中发挥重要作用。
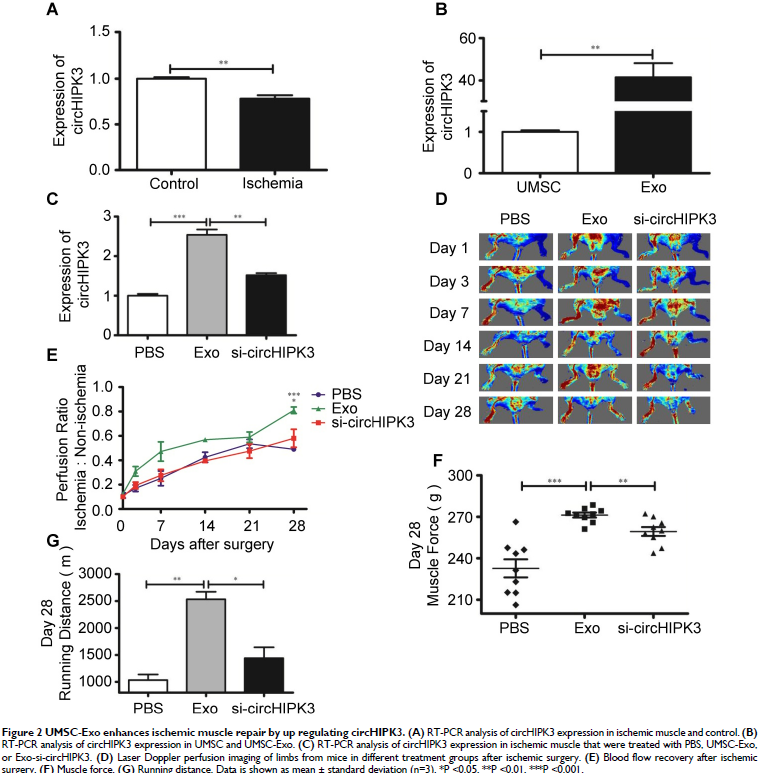
2. 外泌体在体内传递circHIPK3促进缺血性肌肉的修复
外泌体治疗缺血性后肢,发现circHIPK3的表达显著上调,显著增强灌注,改善肌肉力量和跑步距离,敲低circHIPK3后无效应。表明间充质干细胞衍生的外泌体(UMSC-Exo)通过释放circHIPK3促进缺血性后肢修复。
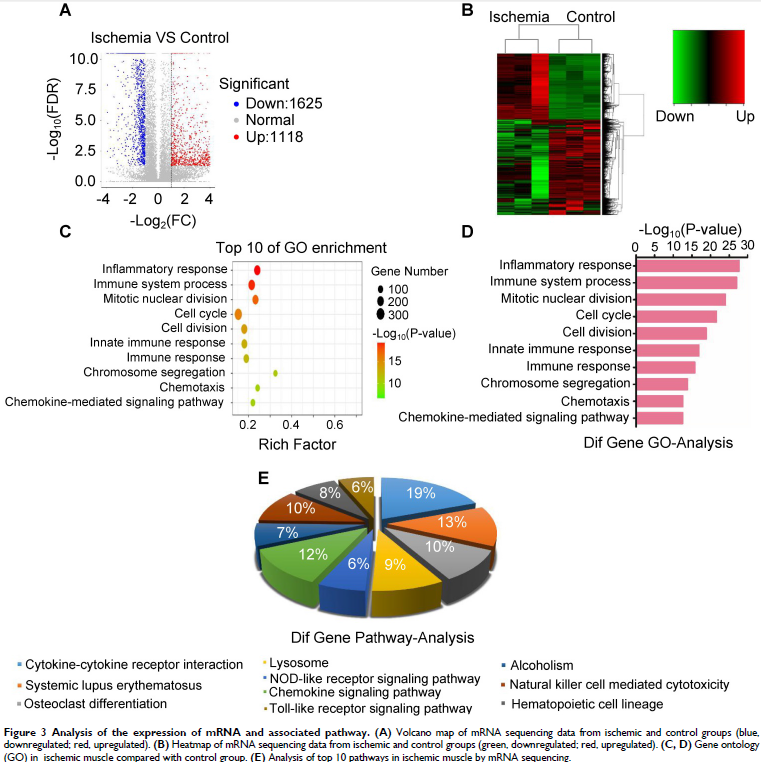
3. 局部缺血肌肉中爆发炎症反应
缺血和正常腓肠肌RNA测序筛选差异表达RNA,发现2743个差异表达mRNA,GO和KEGG分析发现炎症反应和NOD、Toll样受体信号通路在缺血中明显激活。接下来关注炎症反应途径和相关分子。蛋白质预测出80个差异表达蛋白质,通过对缺血组和对照组的转录组和蛋白质组分析发现28个基因和相关蛋白发生类似变化。mRNA和蛋白质相关性分析发现NLRP3和IL-1β缺血性肌肉中均显著增加。
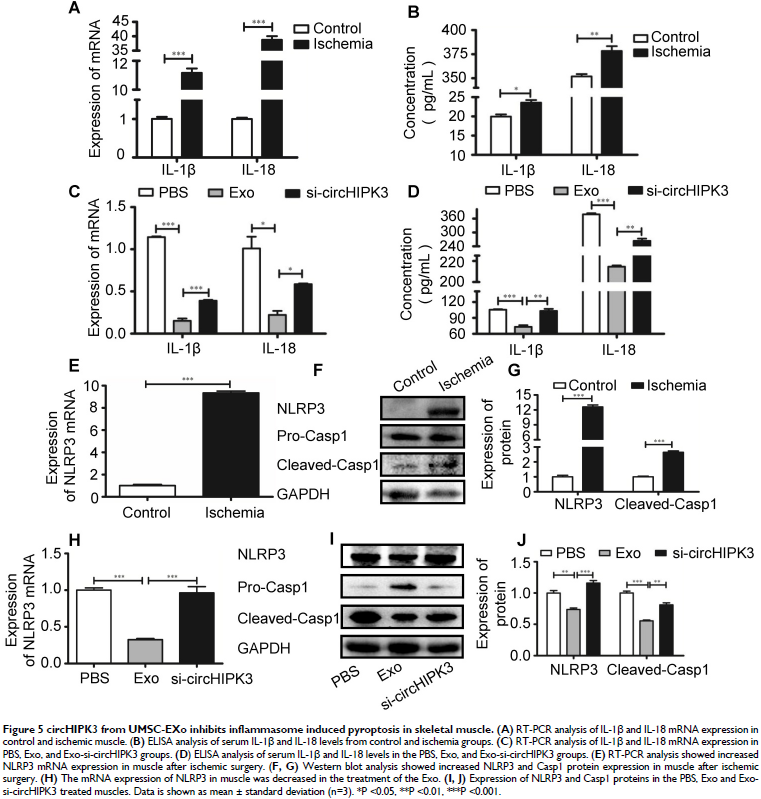
4. circHIPK3抑制骨骼肌细胞焦亡
缺血肌肉中IL-18和IL-18表达升高,提示诱导骨骼肌焦亡。外泌体治疗减少细胞因子水平,可被si-circHIPK3逆转,表明该能力依赖circHIPK3。缺血肌肉中NLRP3和caspase-1的表达水平升高,外泌体治疗后降低。以上表明,外泌体可预防骨骼肌焦亡,这种有益效果由circHIPK3介导。
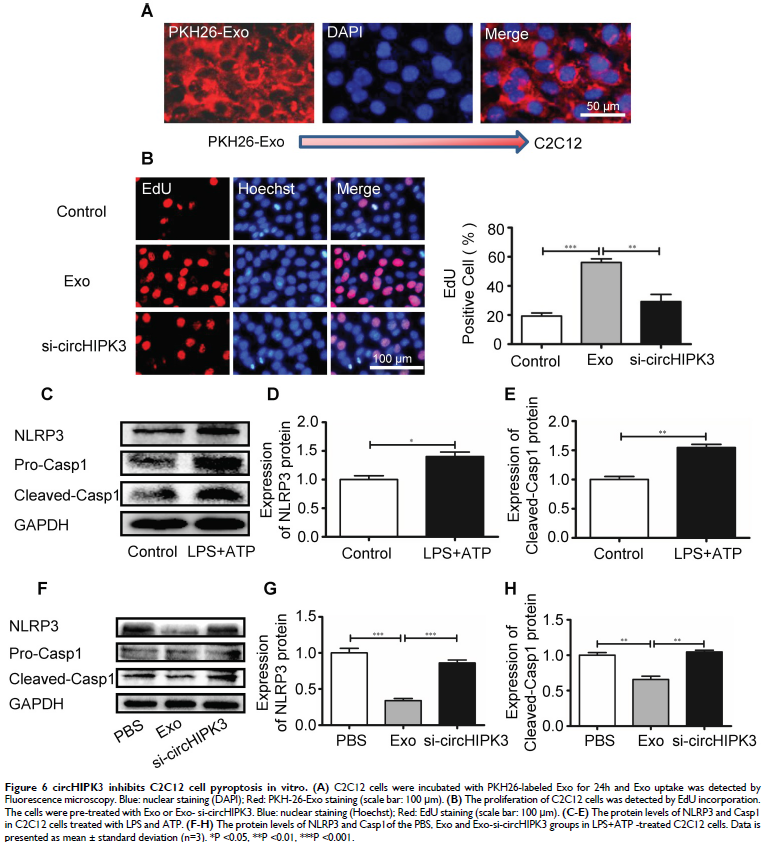
5. 外泌体通过释放circHIPK3刺激C2C12细胞增殖并抑制NLRP3和caspase-1表达
体外孵育鼠成肌细胞系C2C12细胞与外泌体,PKH26标记的外泌体进入C2C12细胞,细胞增殖增加。C2C12细胞用LPS预处理和诱发发炎小体形成,发现存在外泌体时,NLRP3和caspase-1明显下调,并且si-circHIPK3逆转外泌体的作用。这些表明外泌体通过传递circHIPK3增加细胞生长并防止炎性体产生。
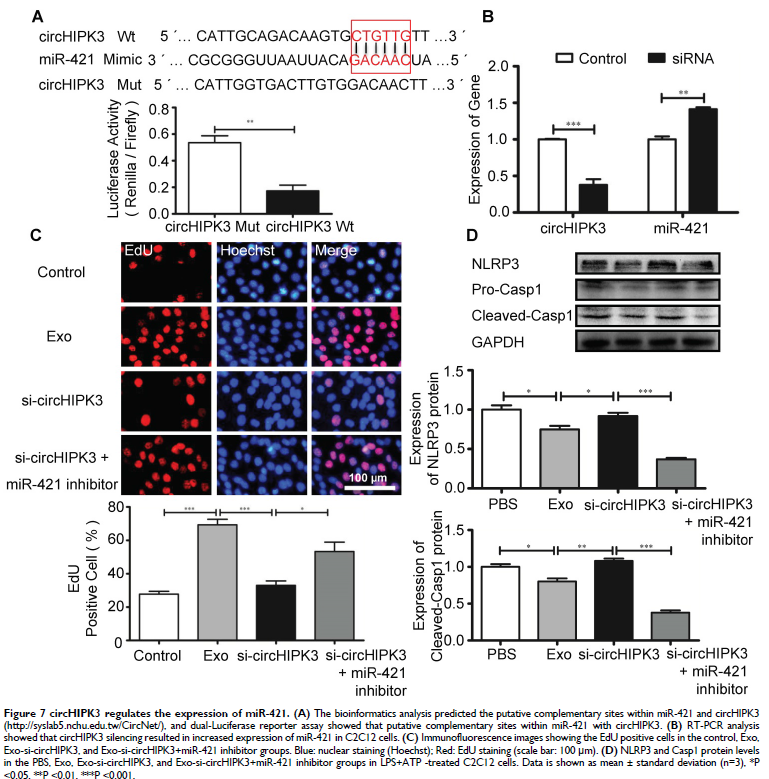
6. circHIPK3用作miR-421的海绵
生物信息学分析显示,miR-421含有circHIPK3结合位点。C2C12细胞中的circHIPK3沉默导致miR-421的表达增加。Exo促进细胞增殖,并被si-circHIPK3抑制;circHIPK3的沉默作用被miR-421抑制剂逆转。在存在miR-421抑制剂时,C2C12细胞中NLRP3和caspase-1的表达减少。这些表明miR-421是circHIPK3的直接靶标。
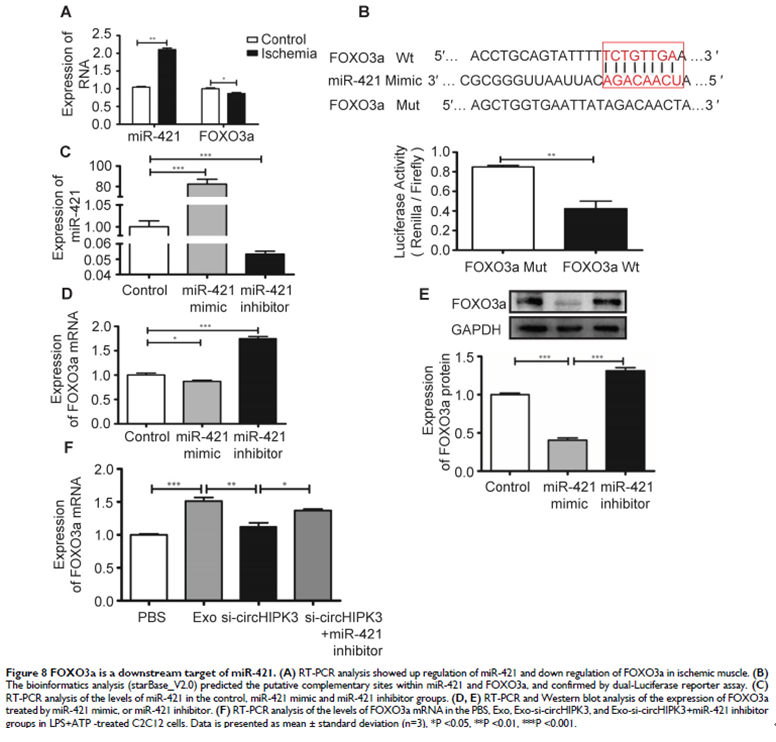
7. FOXO3a是miR-421的直接靶标
在缺血性后肢组织中升高的miR-421表达与FOXO3a的mRNA表达降低相关。生物信息学预测miR-421与靶基因的潜在结合位点,荧光素酶报道基因证实。miR-421 mimic抑制FOXO3a的表达,而miR-421 inhibitor增强FOXO3a的表达。Exo通过传递circHIPK3来增加FOXO3a的表达,进一步证实FOXO3a是miR-421的直接靶标。
总 结:
1. circHIPK3作为miR-421海绵抑制炎症,增加FOXO3a表达,并阻止炎症小体NLRP3和caspase-1的激活;
2.UMSC-Exo通过传递circHIPK3抑制骨骼肌细胞焦亡,增强缺血后肢修复。
3.研究为缺血性损伤的治疗提供一种有效的治疗方法。






