外泌体circRNA参与肿瘤免疫治疗
外泌体,circRNA,肿瘤免疫微环境和肿瘤免疫治疗的都是近年来生命科学研究热点,也是国自然基金申请重点领域。今天我们讲一篇2020年6月27日发表在Molecular Cancer的文章,题名:Cancer Cell-Derived Exosomal circUHRF1 Induces Natural Killer Cell Exhaustion and May Cause Resistance to anti-PD1 Therapy in Hepatocellular Carcinoma。这篇文章来自复旦大学附属中山医院研究团队,文章主要讲述了外泌体circUHRF1主要由HCC细胞分泌,通过诱导HCC中的NK细胞功能障碍参与免疫抑制,CircUHRF1可能驱动抗PD1免疫疗法的耐药性。

技术路线:
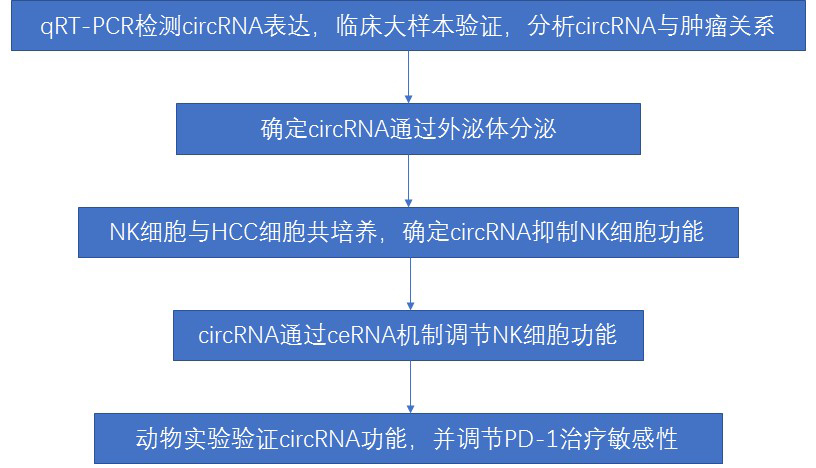
结 果:
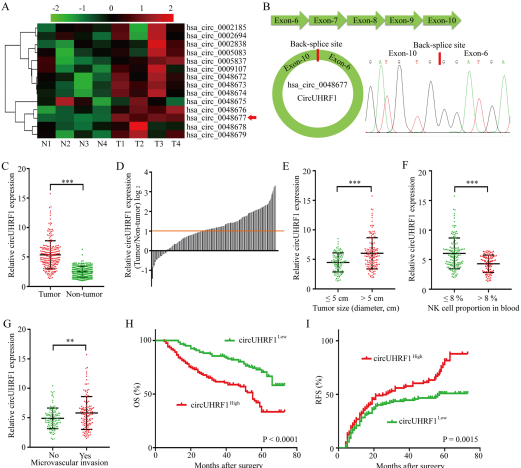
1.肝癌组织中与UHRF1相关的circRNA的分析
具有PHD和RING指域1(UHRF1)的泛素样蛋白是参与调节DNA甲基化的关键分子,通常在包括HCC在内的许多癌症中过表达。UHRF1过表达可促进肝癌的发生和发展。因此,作者推测UHRF1衍生的circRNA表达可能被上调并可能促进HCC的进展。
qRT-PCR检测从UHRF1衍生的14个circRNA的表达水平,qRT-PCR又检测circUHRF1在240例HCC组织和癌旁的表达,肝癌组织高表达。circUHRF1 高表达的HCC患者肿瘤较大并血液中的NK细胞比例降低,微血管转移增多。KM生存分析表明circUHRF1 高表达患者的临床预后较差。数据表明,HCC细胞中circUHRF1表达上调与患者不良预后相关,并表明circUHRF1表达增加可能与HCC的进展有关。
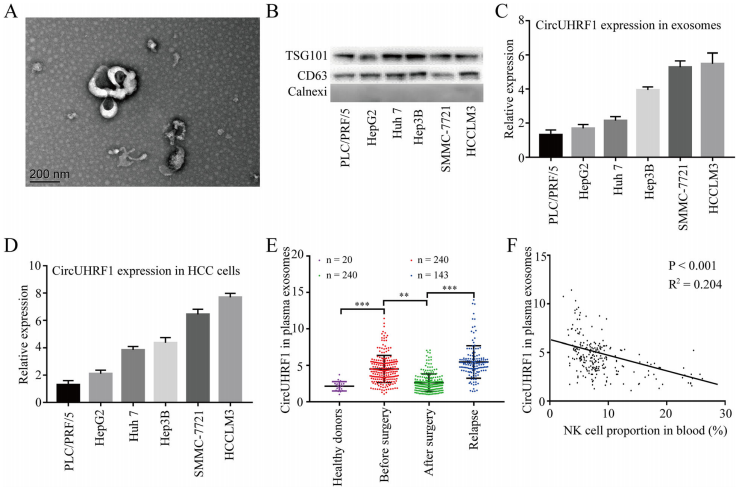
2.HCC细胞以外泌体方式分泌circUHRF1
从HCC细胞系上清液中分离了外泌体,并通过TEM和Western blot对其进行了评估。在6个HCC细胞系及对应的外泌体中进行qRT-PCR检测, HCCLM3和SMMC-7721细胞系中circUHRF1显著上调,且外泌体中circUHRF1的表达趋势与亲代细胞的一致。与健康供体相比,HCC患者的血浆外泌体circUHRF1水平升高。肿瘤切除后血浆外泌体circUHRF1水平降低,而在肿瘤复发患者中升高,这表明血浆外泌体circUHRF1主要由HCC细胞产生。有免疫逃逸的患者血浆中外泌体circUHRF1水平显著升高,外周血中NK细胞比例降低。这些数据表明血浆外泌体circUHRF1可以作为NK细胞相关的免疫逃逸的关键分子。
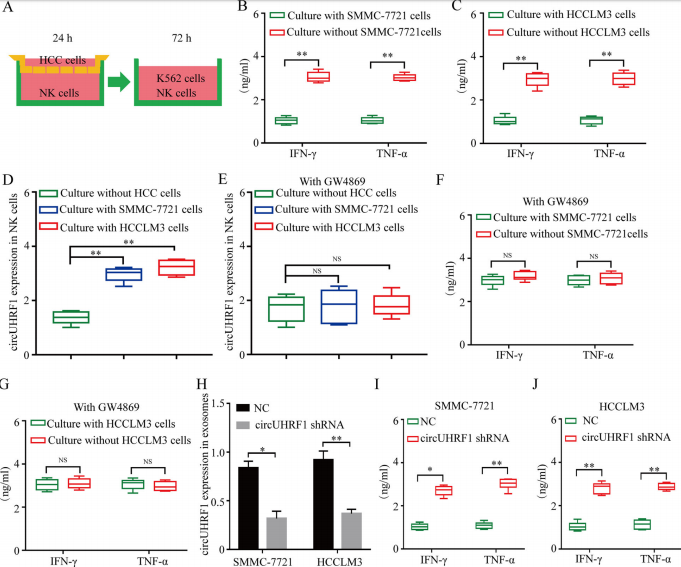
3.HCC细胞通过外泌体circUHRF1抑制NK细胞功能
将来自健康供体的NK细胞与HCCLM3和SMMC-7721细胞以1:1的比例共培养24h。与NK细胞相比, SMMC-7721和HCCLM3细胞共培养的NK细胞在随后与K562细胞共培养时表现出IFN-γ和TNF-α分泌的显著降低。SMMC-7721和HCCLM3细胞共培养的NK细胞中circUHRF1表达显着增加,并受到外泌体抑制剂GW4869的抑制,抑制剂GW4869处理后IFN-γ和TNF-α表达恢复正常水平。使用shRNA慢病毒载体构建HCCLM3和SMMC-7721 circUHRF1敲低细胞。在circUHRF1敲低细胞中外泌体circUHRF1的表达显着降低,外泌体circUHRF1水平的降低有效减弱了HCC衍生的外泌体诱导的NK细胞中IFN-γ和TNF-α分泌的损伤。结果表明,源自HCC的外泌体circUHRF1损害NK细胞的功能。
4.CircUHRF1和miR-449c-5p在NK细胞中相互作用
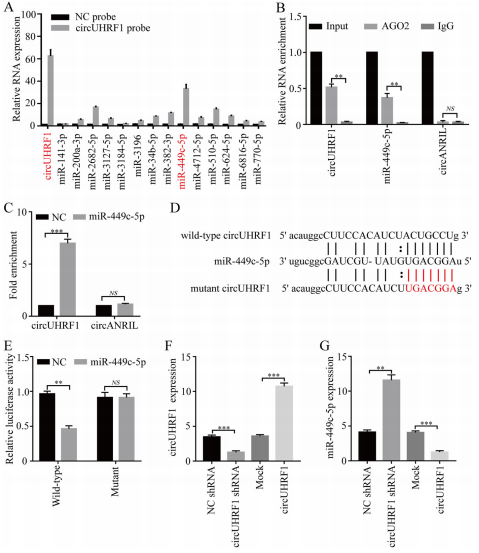
通过StarBase v3.0分析,预测有14个miRNAs可能是circUHRF1的靶标。使用circUHRF1特异性探针进行circRNA免疫沉淀(circRIP),并使用qRT-PCR检测到了与circUHRF1形成复合体的14种预测miRNA。与对照相比,circUHRF1和miR-449c-5p显着富集,而其他miRNA没有富集或仅有少量富集。在NK-92细胞中进行了AGO2-RIP实验,抗AGO2抗体显着富集了circUHRF1和miR-449c-5p,pulldown和荧光素酶基因报告实验也验证这一结果。在NK-92细胞中过表达miR-449c-5p后,circUHRF1的水平显着降低,而在circUHRF1过表达后,miR-449c-5p的水平显着降低。结果证实,circUHRF1是miR-449c-5p分子海绵,且在在NK细胞中相互影响。miR-449c-5p的过表达表达显着抑制肿瘤活性(促进IFN-γ和TNF-α分泌),增加circUHRF1表达可显着抑制miR-449c-5p的肿瘤抑制功能,证明了了HCC衍生的外泌体circUHRF1可能通过miR-449c-5p相关途径抑制NK细胞功能的关键能力。
5.CircUHRF1通过抑制miR-449c-5p活性上调TIM-3表达
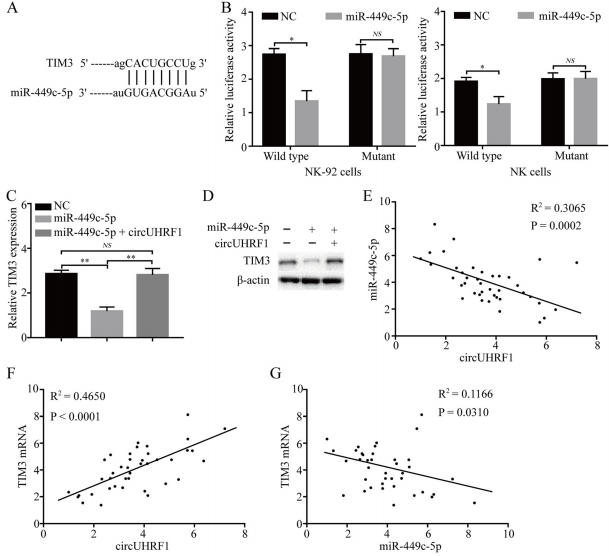
StarBase v3.0预测了miR-449c-5p在TIM-3上的结合位点,荧光素酶基因报告实验验证预测结果。miR-449c-5p的过表达后TIM-3表达显着降低。回复实验表明miR-449c-5p过表达导致TIM-3的mRNA和蛋白表达降低,而circUHRF1逆转了miR-449c-5p对TIM-3表达的抑制作用。接下来调查了40例HCC患者外周血NK细胞中circUHRF1和miR-449c-5p / TIM-3表达之间的相关性。外周血NK细胞中circUHRF1表达与miR-449c-5p表达负相关,且与TIM-3 mRNA表达呈正相关,miR-449c-5p表达与外周NK细胞中TIM-3 mRNA的表达呈负相关。表明外泌体circUHRF1的上调消除了miR-449c-5p对NK细胞中TIM-3的肿瘤抑制作用。
6.CircUHRF1以NK细胞依赖性方式诱导HCC进展
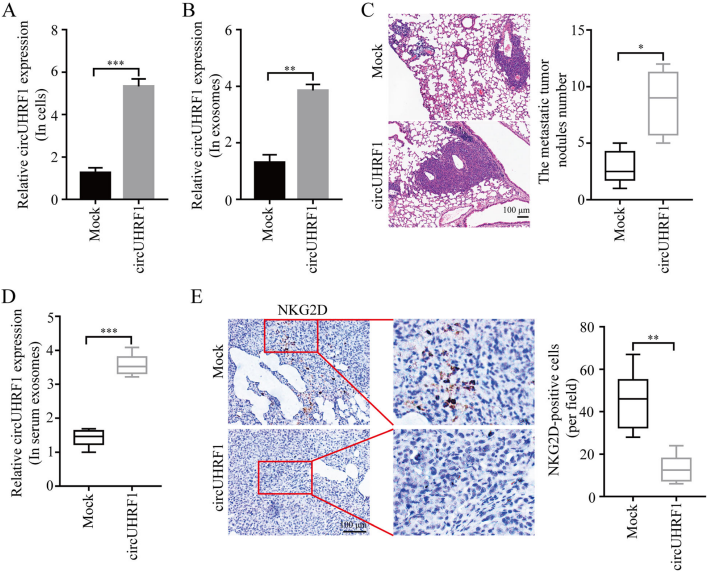
使用慢病毒载体在PLC / PRF / 5细胞中构建circUHRF1过表达细胞系。结果显示过表达成功,且外泌体中circUHRF1表达升高。使用上述细胞进行裸鼠肺转移模型构建(注射健康供体的NK细胞),过表达circUHRF1的PLC / PRF / 5细胞转移性肿瘤结节数显着增加,转移小鼠的血清外泌体circUHRF1水平升高,转移性肿瘤结节中NKG2D阳性细胞的数量明显减少。这些结果表明circUHRF1以外泌体和NK细胞依赖性方式促进HCC进展。
7.CircUHRF1增强HCC对抗PD1治疗的抵抗力
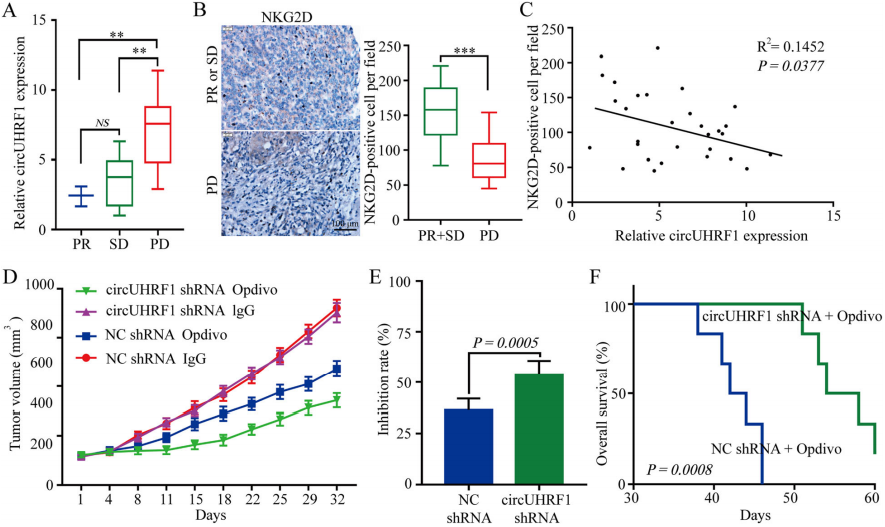
作者分析了30例接受抗PD1免疫治疗的复发性远处转移(包括肺转移)的HCC患者的回顾性数据,这些患者在免疫治疗前2-36个月接受了肝切除术。六个治疗周期后,使用CT评估疗效。结果显示,部分缓解(PR)3例,疾病稳定(SD)7例,进行性疾病(PD)20例。测量circUHRF1的表达显示,PD组的circUHRF1的表达水平远高于SD和PR组。为了进一步探讨circUHRF1与免疫逃避之间的关系,检查了30例HCC患者组织中NKG2D的表达。与易受PD1治疗的HCC患者相比,抗PD1治疗的HCC患者的NKG2D阳性细胞数量明显减少,HCC组织中circUHRF1表达与NKG2D阳性细胞数呈负相关。为了进一步评估circUHRF1对抗PD1治疗的抗性,通过皮下植入circUHRF1基因敲除的HCCLM3细胞建立了异种移植模型。circUHRF1敲低细胞可提高对抗PD1治疗的敏感性并提高总生存率。综上所述,这些发现表明过表达circUHRF1可能会阻碍HCC对抗PD1治疗的反应,而靶向circUHRF1可能是恢复HCC对抗PD1治疗敏感性的有前途和有效的方法。
结 论:
HCC衍生的外泌体通过诱导NK细胞上TIM-3表达来抑制IFN-γ和TNF-α的产生。肿瘤外泌体通过circUHRF1抑制NK细胞功能,为HCC细胞与NK细胞之间的串扰提供了新证据。






