癌细胞分泌的外泌体促进骨髓转移
癌细胞分泌的外泌体促进骨髓转移
导语:肿瘤微环境是肿瘤进展的关键要素,骨髓基质作为一种独特的转移微环境,通过促进肿瘤细胞存活,促进转移过程。外泌体可以介导小分子从肿瘤细胞转移到远处器官的靶细胞,促进转移定植。癌细胞分泌的外泌体是否骨髓转移?小编这里有话说。
参考文献:Colletti M , Tomao L , Galardi A , et al. Neuroblastoma-secreted exosomes carrying miR5 promote osteogenic differentiation of bone-marrow mesenchymal stromal cells[J]. Journal of Extracellular Vesicles, 2020, 9(1):1774144. (IF: 14.976)
技术路线:
结果:
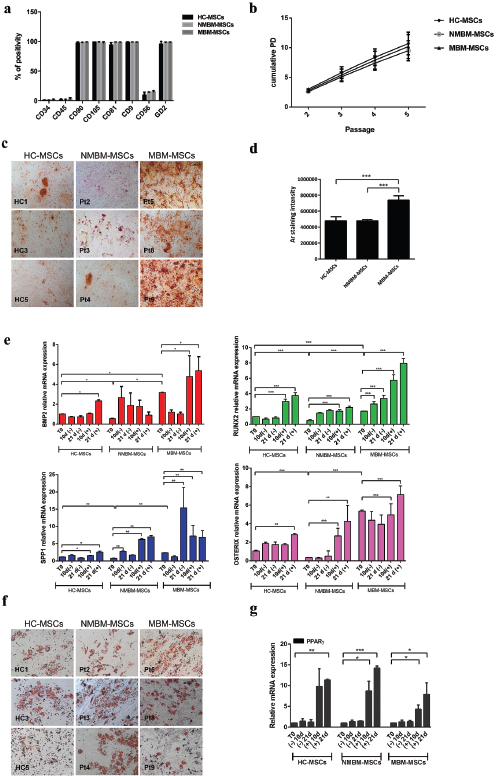
1. 成神经细胞瘤(NB)伴骨髓(BM)转移患者的BM-MSCs具有较强的成骨能力
从12例NB患儿和7例健康对照(HC)患儿中分离并鉴定BM-MSCs,在NB患者中,8例呈现BM转移(MBM-MSCs、转移性骨髓-MSCs),4例无BM转移(NMBM-MSCs、非转移性骨髓MSCs)。分析MSC细胞免疫表型,检测间充质、造血和神经元标志物的表达。MBM-MSCs中钙沉积含量较高,成骨分化相关转录因子,成骨标志物表达更高。以上表明,与无骨髓转移患者的BM-MSCs相比,从有骨髓浸润的NB患者中分离的BM-MSCs具有更强的成骨分化能力。
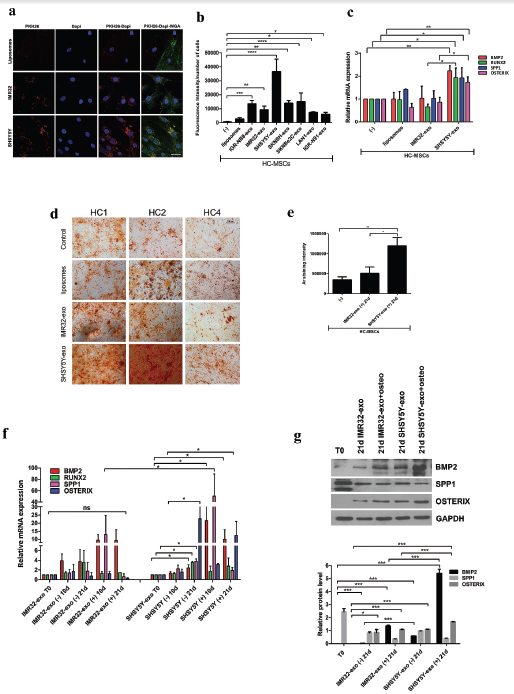
2. 来源于BM转移的NB细胞的外泌体可增强HC-MSCs的成骨作用
探索骨髓转移衍生的NB细胞系产生的外泌体是否与BM-MSCs的相互作用,原发性(PT)肿瘤细胞系(IMR32,IGR-NB8)和五个BM转移衍生的NB细胞系(SKNSH,SH5YSY,SKNBe2 c,LAN-1,IGR-N91)分离外泌体,发现NB细胞来源的外泌体被HC-MSCs有效内化,诱导细胞成骨mRNA的表达和更高的钙沉积含量。这些数据表明,BM转移来源的NB细胞释放的外泌体在调节BM-MSCs成骨分化。
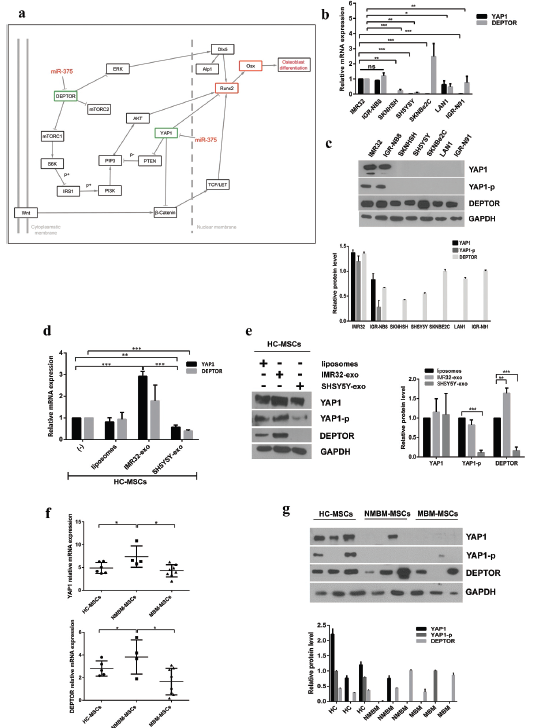
3. MiR-375在BM转移来源的NB细胞系释放的外泌体中和MBM-MSCs中高表达
分析PT来源和BM转移来源细胞系之间外泌体miRNA的表达水平,5个miRNA表达上调,miR-375的水平更高,与SHSY5Y-外泌体共培养可显著增加HC-MSCs中miR-375的表达。靶标预测分析miR-375的潜在靶标Yes蛋白相关蛋白1(YAP1)和含有mTOR相互作用蛋白的DEP结构域(DEPTOR)。与PT来源的细胞系相比,NB BM转移中YAP1和DEPTOR表达水平均较低,YAP1及其磷酸化形式(YAP1-p)在NB BM转移来源的细胞系中均不表达,DEPTOR在分析的所有NB细胞系中大量表达,在转移性细胞系中少量表达。


4. MiR-375调节成骨转录因子的表达
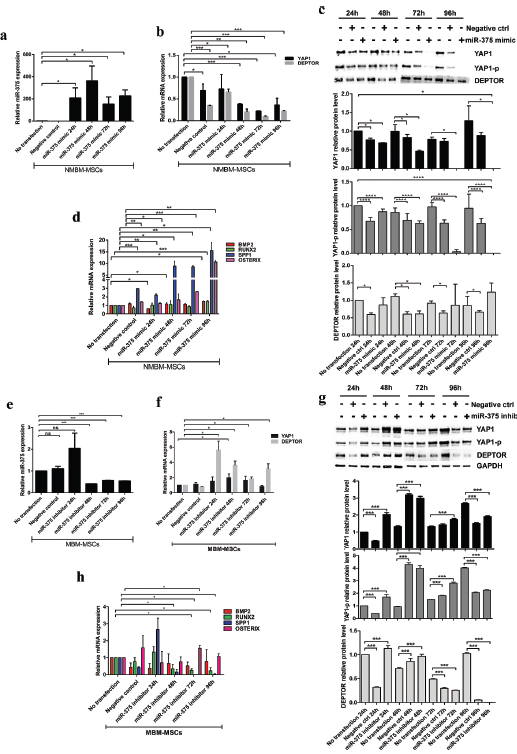
为证实MiR-375参与BMMSCs成骨分化,在NMBM-MSC中过表达或敲除MiR-375,miR-375的过表达显著降低其靶基因YAP1表达,在较小程度上降低DEPTOR,增加成骨标志物表达。抑制miR-375 显著上调YAP1和DEPTOR,未观察到参与成骨细胞分化的基因的下调。
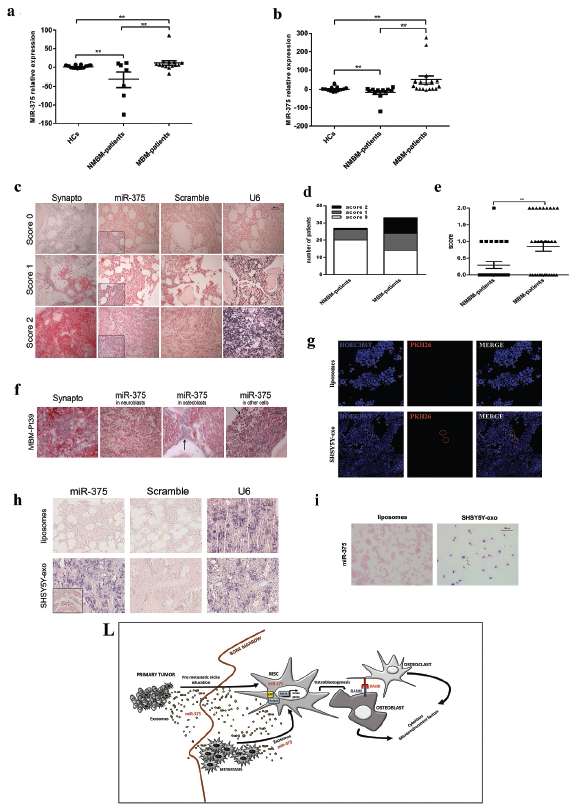
5. MiR-375表达与NB患者BM疾病相关
为检测NB患者MiR-375表达水平与BM浸润之间的可能相关性,从HC、NMBM患者或MBM患者的外周血血浆和骨髓血浆中分离外泌体,发现MBM患者外泌体中miR-375水平显著高于NMBM患者,miR-375的阳性染色与转移分期和BM浸润相关。为确定NB来源的外泌体是否能够到达BM,我们在NOD SCID小鼠注射PKH26标记的外泌体,证实BM细胞摄取外泌体,外泌体携带miR-375并能够将其转移到骨髓MSCs。以上表明,循环外泌体和骨髓中高水平的miR-375与骨髓转移有关。