小胶质细胞HO-1阻断通过影响铁死亡在衰老过程中发挥保护作用
研究背景:HO-1是一种抗炎、抗氧化和具有神经保护作用的诱导酶,但是,在衰老过程中和年龄相关疾病中,HO-1的表达增加与神经毒性铁沉积有关。因为小胶质细胞与脑内固有免疫反应有关,Cristina Fern´ andez-Mendívil等人在Redox Biology(IF= 9.986)这一杂志上发表文章,阐明在炎症条件下的老年鼠中小胶质细胞HO-1的作用。
技术路线图:
研究结果:
1. 在LPS 刺激和老年的小鼠脑内小胶质细胞中,HO-1的表达上调
与成年小鼠相比,老年小鼠的大脑中HO-1表达上调(图1A-D)。图1 A和E,与生理盐水处理的老年鼠相比,LPS处理的老年鼠Iba1+小胶质细胞中HO-1水平显著升高。结果表明,随着年龄的增长,小胶质细胞HO-1表达上调,在急性炎症损伤中,HO-1的过表达进一步增加。
Fig.1

2. 老年鼠接受炎症刺激之后,小胶质细胞HO-1的缺失使铁代谢变化恢复
如图2B所示,WT小鼠经lps注射之后脑内非血红素铁的含量显著增加,但是在HMOX1M-KO小鼠中并没有增加。此外,Perl s溶液染色显示在注射LPS的WT小鼠海马和皮质中铁积累(图2C和D),与生理盐水WT小鼠相比。这些沉积在LPS刺激的HMOX1M-KO小鼠中较低(图2C和D)。表明在衰老过程中LPS依赖的小胶质细胞HO-1上调可能在铁沉积的形成中发挥关键作用。LPS处理的WT小鼠大脑中观察到的铁沉积与不同铁代谢标志物的改变有关(图2E)。铁转运体DMT1和铁蛋白L-ferritin升高,而铁转运蛋白FPN1下降 (图2E和F)。然而,这些改变在LPS处理的HMOX1M-KO小鼠中被逆转,这意味着在衰老的WT小鼠中,LPS导致了铁流入和储存增多,而外排减少,从而导致铁积累。在老化的HMOX1M-KO中,没有铁积累。
Fig.2

3. 在老年WT小鼠中,炎症刺激导致脑内氧化应激,铁死亡和认知降低
如图3ABC, 荧光染料H2DCFDA和DHE标记小鼠海马中ROS的产生,发现在老年WT小鼠中ROS显著增加,而LPS刺激的HMOX1M-KO小鼠中,ROS减少。并且,通过图3A和D 观察PI染色发现,LPS注射WT小鼠会导致海马细胞死亡的增加。LPS刺激的HMOX1M-KO小鼠中,细胞死亡减少。LPS注射WT小鼠GPX4的表达降低,HMOX1M-KO小鼠中没有变化(图3E和F)。由于铁死亡导致神经元死亡,之后又研究LPS是否也会导致认知能力下降,通过NOR(新事物识别)任务进行评估 (图3G)。事实上,LPS在WT小鼠中诱导了认知能力的下降,测量结果是DI的下降,但在HMOX1M-KO中没有 (图3H)。因此,这些结果表明,在年老的WT小鼠中观察到LPS诱导的小胶质细胞HO-1的上调导致的的铁积累,可能导致OS、铁下垂,并最终导致认知能力下降。但是,LPS处理的HMOX1M-KO小鼠中,所有这些特征均显著减弱并部分恢复。
Fig.3

4. 小胶质细胞HO-1缺失改善了LPS诱导的炎症状况和衰老小鼠的疾病行为
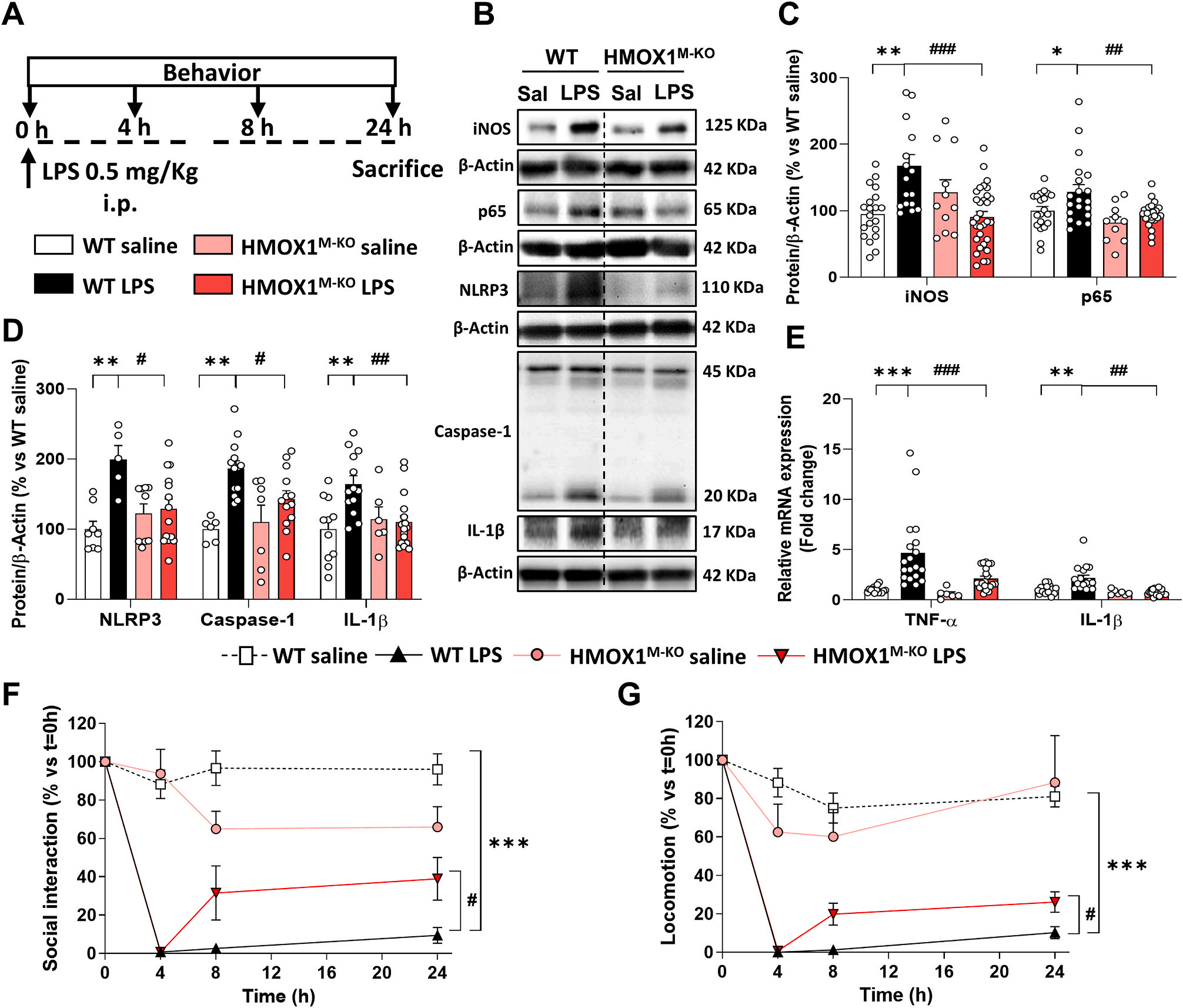
报道显示铁沉积与神经炎症关系密切。之后,我们研究了LPS依赖性的小胶质细胞HO-1过表达,除了导致铁代谢改变外,是否与脑内促炎改变相关,尽管其具有抗炎作用。我们分析了LPS注射24小时后海马区不同的炎症标志物(图4A)。iNOS和p65,与炎症小体相关蛋白质NLRP3、 caspase-1和IL- 1β,和细胞因子TNF -α和IL- 1β(图4 e)。与注射盐水的WT小鼠相比,注射LPS的WT小鼠中这些蛋白或细胞因子的表达显著增加。然而,LPS刺激的HMOX1M-KO小鼠中这些参数显著降低。
Fig.4
5. ZnPP对HO-1的药理抑制可以恢复LPS引起的炎症、氧化和铁变化
使用ZnPP作为HO-1抑制剂,证实遗传小鼠模型获得的结果。按照图6A的方法。ZnPP减少了LPS诱导的非血红素铁的积累(图6B), ZnPP能够至少部分恢复LPS诱导的铁代谢改变(图6D)。此外,ZnPP处理降低了LPS诱导的iNOS、p65和CD68的增加(图6E和F)、炎性体相关蛋白、IL-1β、NLRP3和caspase-1的表达(图6G和H) 以及细胞因子TNF和IL-1表达减少(图6I)。此外,ZnPP改善了小鼠在疾病行为测试中的表现(图6J和K)。综上所述,这些结果支持了HO-1在受到炎症刺激的老年鼠中对铁代谢、炎症和行为改变的作用
Fig.5

6. 去铁胺(DFX)治疗可以改善LPS处理的老年小鼠的铁代谢改变、炎症和疾病行为
DFX能够减少不稳定铁(图7B)并恢复LPS诱导的铁代谢变化(图7 c和D). 此外,DFX减少炎性标记物的表达,如iNOS和p65, 而不是CD68(图7E和F)和炎性体相关标志物NLRP3、caspase-1和成熟IL-1 (图7 g和H)。此外,DFX也减少了TNF-α和IL- 1β (图7I)。此外,DFX改善了小鼠在疾病行为任务中的表现(图7J和K)。DFX能够恢复LPS处理的老年小鼠的大部分变化,这一事实表明,老年WT小鼠中,铁负荷可能是LPS依赖性小胶质细胞HO-1过表达的结果,与炎症、氧化应激和认知障碍有关。
Fig.6







