人脐带血来源的MSCs外泌体通过抑制铁死亡缓解急性心肌梗死小鼠心肌损伤
急性心肌梗死(Acute myocardial infarction, AMI)常因氧和血供突然减少而引起心肌损伤和心力衰竭,是发病和死亡的主要原因之一。铁死亡是一种氧化的、依赖铁的细胞死亡形式,不同于坏死、凋亡和自噬。

细胞内谷胱甘肽(GSH)依赖的抗氧化防御系统失活,导致毒性脂质活性氧(ROS)的积累,从而导致铁细胞膜下垂。据报道,铁tosis可发生在缺血再灌注(I/R)损伤、癌症等。铁死亡是心肌细胞死亡的一种重要形式。ferroptosis在急性心肌梗死中起重要作用。人脐带间充质干细胞(hub -MSCs)因其免疫原性低、增殖因子高、转染效率高,具有广阔的应用前景。有报道称,HUCBMSCs来源的外泌体缓解了AMI损伤。那么,间充质干细胞外泌体是否对AMI中ferroptosis有调节作用呢?二价金属转运体DMT1 (Slc11a2)作为复杂生理过程的关键组成部分,可以调节体内铁的水平。在哺乳动物中,dmt1是一种铁(2+)的转运体,对适当维持铁的稳态至关重要。有鉴于此,河南省人民医院,阜外中华心血管病医院麻醉科的Yufang Song、河南省人民医院阜外中国中部心血管医院心血管外科Zhenwei Ge等研究人员,探讨DMT1在AMI体外和体内模型中的表达及作用。
据报道,人脐血来源的MSCs外泌体对急性心肌梗死(AMI)和心肌细胞缺氧损伤小鼠模型有心肌保护作用,但具体机制有待进一步研究。
本文旨在研究hucb - msc -外泌体抑制铁死亡减轻心肌损伤的作用。RT-PCR和western blotting结果显示,与假手术组和常氧组比较,二价金属转运体1 (DMT1)表达显著升高,Prussian蓝染色、铁离子(Fe2+)、MDA和GSH水平检测结果显示,缺氧损伤后心肌梗死和心肌细胞出现铁死亡。过表达DMT1促进H/ r诱导的心肌细胞铁死亡,而敲除DMT1则显著抑制了心肌细胞铁死亡。hub - msc来源的外泌体抑制了铁死亡和减少心肌损伤,miR-23a- 3p敲除后在外泌体中消失。双荧光素酶报告基因实验证实DMT1是miR-23a-3p的靶基因。综上所述,hucb - mscs -外泌体可能通过miR-23a-3p抑制DMT1的表达,从而抑制铁死亡,减轻心肌损伤。
技术路线:
结果:
一、在AMI小鼠中上调DMT1的表达并增加铁死亡
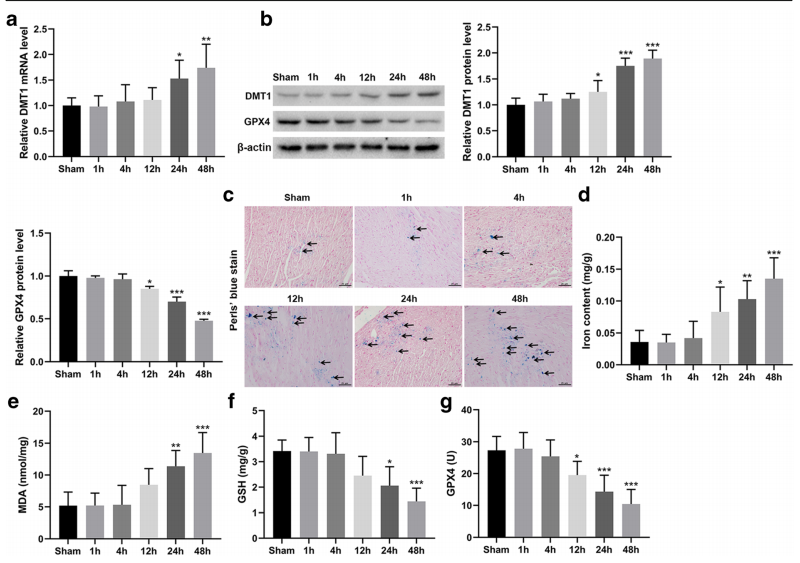
B.建立小鼠AMI模型,分别于术后1 h、4 h、12 h、24 h、48 h采集左心室心肌组织。RT-PCR和western blot结果显示,AMI小鼠24 h和48 h时DMT1表达明显高于假手术组,而GPX4蛋白表达降低.表明AMI模型建立后24 h DMT1明显上调。
C.使用Prussian蓝染色和铁检测试剂盒,AMI小鼠在12 h、24 h和48 h铁沉积和亚铁(Fe2+)水平增加(图1c、d)。
D.AMI小鼠24 h和48 h MDA水平升高,GSH水平和GPX4活性均下降。提示AMI模型LAD后24 h可出现心肌组织铁死亡。
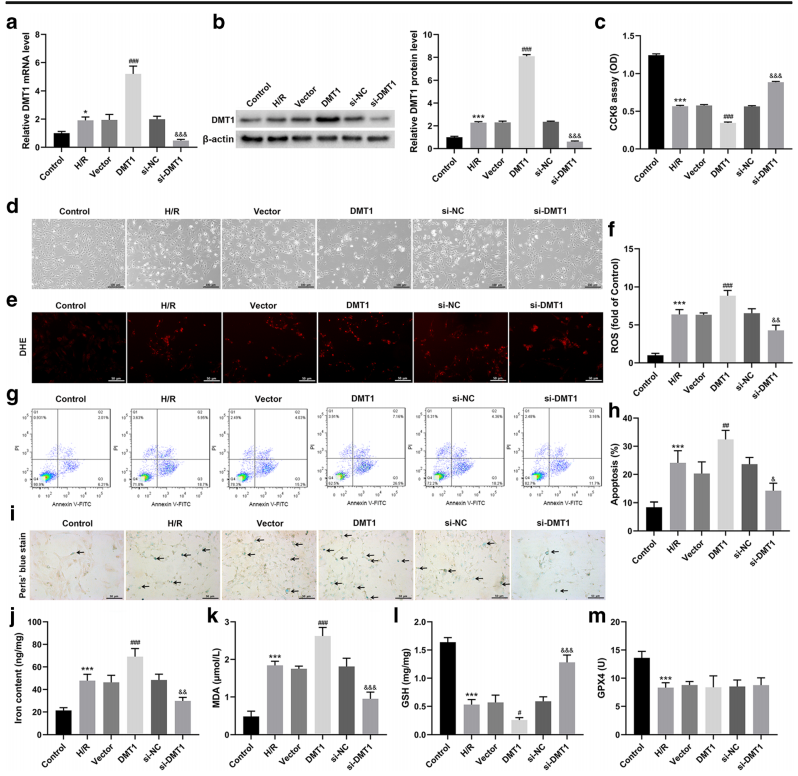
A-B.用H/R处理新生小鼠心肌细胞,并转染携带DMT1表达序列/DMT1干扰序列或阴性对照的慢病毒。与对照组相比,H/R组DMT1 mRNA和蛋白表达水平均上调(图2a, b)。
C. 在H/R处理下,细胞活力测定和形态学的变化显示,过表达DMT1进一步降低了细胞活力,而敲除DMT1则明显提高了细胞活力(图2c)。
D. 正常心肌细胞伪足相互接触呈放射状排列,H/R处理使细胞突触变薄、收缩、胞浆萎缩。在H/R处理下,DMT1过表达进一步引起细胞凋亡,核染色质凝集碎裂,细胞收缩,而DMT1敲除明显改善细胞质收缩(图2d)。
G,H. 流式细胞仪分析数据显示,H/R诱导细胞凋亡,过表达DMT1进一步加重细胞凋亡,而敲除DMT1则显著抑制细胞凋亡.
F,J-K . H/R组细胞内ROS水平、铁沉积、亚铁(Fe2+)、MDA水平均升高,过表达DMT1进一步提高了H/ r诱导的ROS水平、铁沉积、亚铁(Fe2+)和MDA水平,而敲除DMT1则显著降低了H/ r诱导的ROS水平、铁沉积、亚铁(Fe2+)和MDA水平.
H/R组发现GSH水平和GPX4活性降低,过表达DMT1进一步降低GSH水平,而敲除DMT1则显著提高GSH水平(图2l)。
DMT1对GPX4活性无显著影响(图2m)。
这些数据表明,DMT1过表达促进H/ r诱导的细胞铁死亡,而敲除DMT1则显著抑制H/ r诱导的细胞铁死亡。
二、HUCB-MSCs和外泌体的分离与鉴定
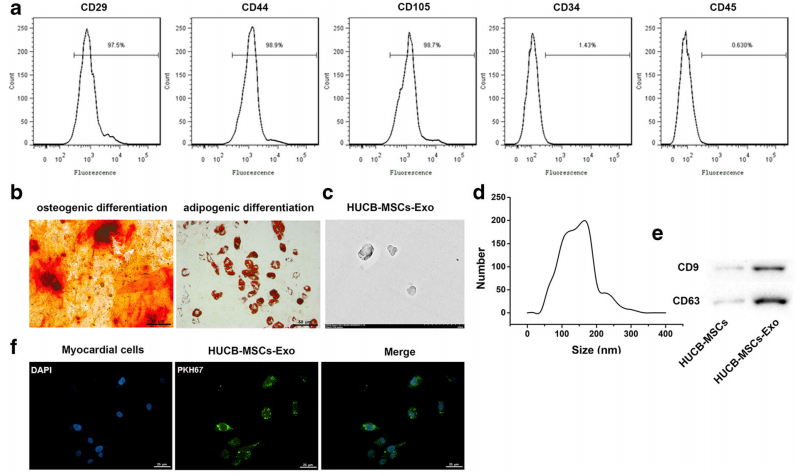
为了证明hub - mscs衍生的外泌体可以改变心肌细胞的基因表达。证明了外泌体可以被心肌细胞吸收。标记PKH67的hucb - mscs外泌体加入心肌细胞培养液中。孵育6 h后如图3f所示,大部分心肌细胞获得了pkh67标记的外泌体,hucb - mscs外泌体在心肌细胞的细胞质中分布相似。
三、hub - msc衍生的外泌体可传递miR-23a-3p来抑制ferroptosis
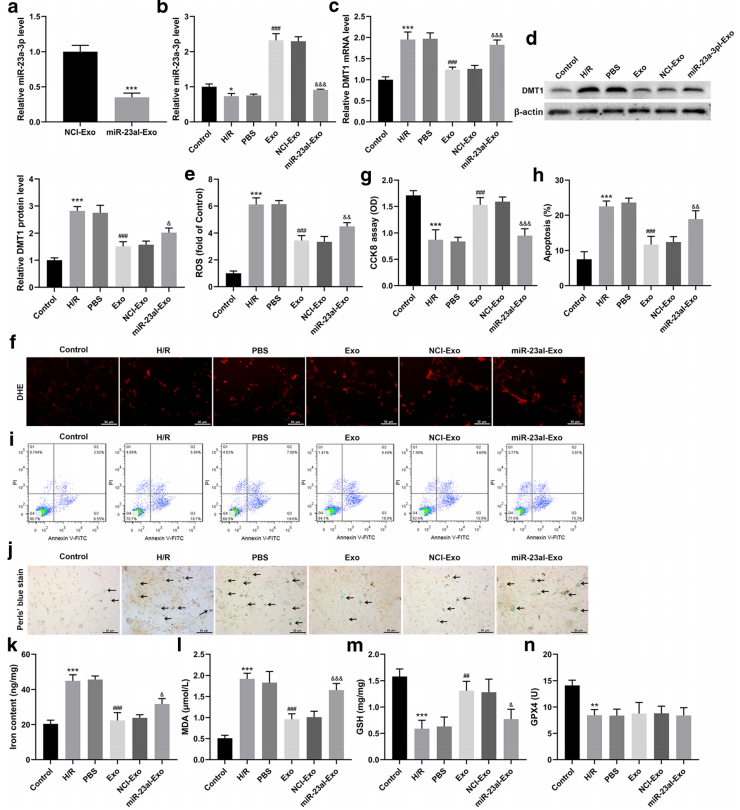
A-B.miR-23a-3p在形成的外泌体中被成功敲低。为了进一步研究外泌体对心肌细胞ferroptosis的影响,构建H/ r诱导的心肌细胞,模拟体外心肌损伤.
C-D. H/ r诱导的细胞中miR-23a-3p表达降低,而与外泌体共培养的心肌细胞中miR-23a-3p表达升高。与hucbmscs -外泌体共培养的心肌细胞中,DMT1 mRNA和蛋白表达与miR-23a-3p相反.
E-M.过表达DMT1可进一步降低H/ r处理心肌细胞的细胞活力和GSH水平,增加细胞凋亡、细胞内ROS水平、铁沉积、亚铁(Fe2+)和MDA水平。图4e -m所示的结果与DMT1表达的变化趋势相同,说明DMT1是hub - mscs来源的外泌体传递miR-23a-3p抑制ferroptosis的关键靶点之一。mir -23a-3p耗损HUCB-MSCs外泌体在心肌细胞铁质下垂中发挥微弱的抑制作用,与NCI-Exo组相比,细胞活力和GSH水平降低,细胞凋亡、细胞内ROS水平、铁沉积、亚铁(Fe2+)和MDA水平升高.
N. hub - msc -外泌体对GPX4的活性没有显著影响(图4n)。
总之,hucb - msc衍生的外泌体传递miR-23a-3p抑制铁死亡。
四、hucb - mscs来源的表达mir -23a-3p的外泌体通过靶向DMT1抑制了ferroptosis
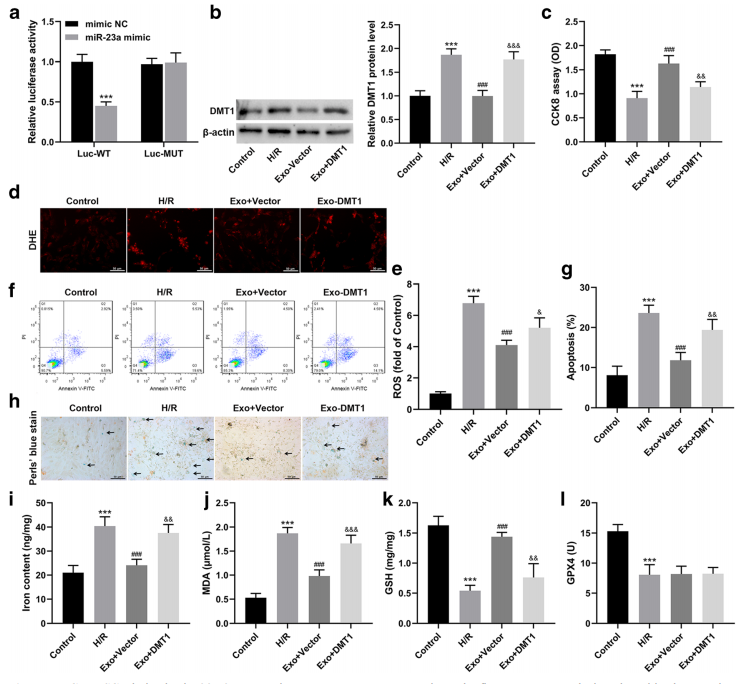
A. Starbase软件预测了miR-23a-3p与DMT1的3 UTR的结合关系。
B. 转染miR-23a-3p mimic的细胞在DMT1- WT共转染体系中荧光素酶活性降低,而在DMT1- mut共转染体系中无明显变化,说明miR-23a-3p与DMT1直接结合。
C. 用hucb - msc -外泌体孵育时,用过表达的DMT1慢病毒感染心肌细胞。DMT1 mRNA和蛋白表达水平在ExoVector组降低,Exo + DMT1组升高,提示hubmscs -外泌体对DMT1表达的负调控作用(图5b)。
D. 过表达DMT1慢病毒感染后,hucbmscs -外泌体诱导的细胞活力升高和GSH水平降低,细胞凋亡减少,细胞内ROS水平、铁沉积、亚铁(Fe2+)、MDA水平升高,表明hucbmscs来源的表达mir -23a-3p的外泌体通过靶向DMT1抑制了ferroptosis。
五、hucb - mscs -外泌体对AMI小鼠心肌细胞的铁死亡有抑制作用
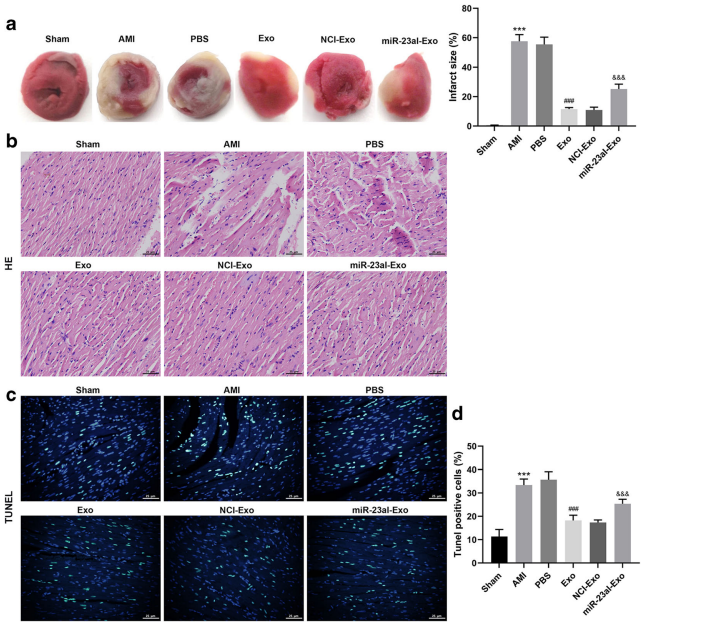
E. TTC染色显示hucb - msc -外泌体减轻AMI小鼠梗死面积,而miR-23a-3pI-Exo减轻AMI小鼠梗死面积的作用明显减弱.
F. hucbmscs -外泌体给药可减轻心肌损伤,而miR-23a-3pI-Exo给药可明显减弱减轻AMI小鼠心肌损伤的作用。
G. 心肌梗死小鼠心肌组织中tunel阳性细胞比例显著增加HUC bmscs -外泌体的植入可以消除这种现象。然而,miR-23a-3pI-Exo移植比NCI-Exo移植具有更高的凋亡指数.
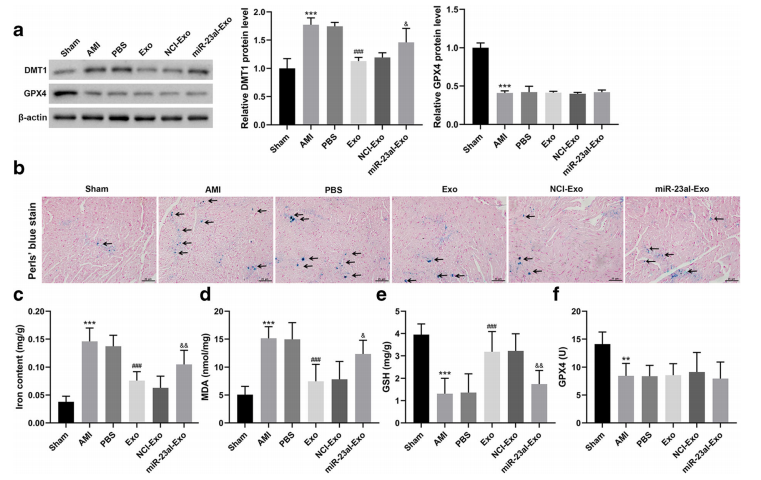
D.HUCB-MSCs外泌体明显抑制DMT1表达、铁沉积、亚铁(Fe2+)和MDA水平,上调GSH水平,但miR-23a-3pI-Exo对这些的作用明显减弱。
E. HUCB-MSCsexosomes对AMI小鼠GPX4活性没有显著影响(图7f)。这些结果表明HUCB-MSCs外泌体抑制了铁死亡。






