铁死亡孔诱导Ca2+通量和ESCRT-III激活来调节细胞死亡动力学

铁死亡是一种与脂质过氧化相关的调节坏死的铁依赖形式。尽管它在铁死亡的炎症结果中起关键作用,但在这种类型的细胞死亡过程中导致质膜破坏的分子事件知之甚少。
2020年11月,来自德国科隆大学遗传学研究所、埃伯哈德-卡尔大学生物化学学院间研究所、德拉萨大学化学系等团队合作在Cell Death & Differentiation杂志上发表了文章“Ferroptotic pores induce Ca2+ fluxes and ESCRT-III activation to modulate cell death kinetics.”。此文献发现胞质Ca2+的持续增加是铁死亡的一个标志,它发生在细胞完全破裂之前。质膜损伤导致铁死亡与半径只有几纳米的膜纳米孔有关,而铁死亡可以被渗透保护剂延迟,而不是脂质过氧化。铁死亡过程中的Ca2+通量可诱导ESCRT-III 依赖的膜修复机制的激活,从而平衡细胞死亡动力学并调节铁死亡的免疫学特征。团队关于铁死亡的发现提供了一个统一的概念,即在质膜破裂之前胞浆Ca2+的持续增加是受调控的坏死类型的共同特征,并将ESCRT-III激活作为这些溶性细胞死亡途径中的一般保护机制。
铁死亡是一种不依赖于caspase的调控性坏死,其特征是细胞膜中产生铁依赖的脂质过氧化物。通过铁死亡导致的细胞死亡的特征是质膜破裂和释放其他受限的细胞内成分,包括促炎症损伤相关的分子模式。因此,铁死亡这种类型的细胞死亡与坏死性炎症和先天免疫系统的激活有关。已有研究表明,铁死亡可导致缺血/再灌注损伤、组织损伤和器官死亡,以及其他几种病理,包括神经退行性疾病和癌症。因此,了解铁死亡过程中膜破裂的分子机制不仅具有生物学意义,而且具有医学意义。
执行铁死亡的一个基本步骤是质膜的最终破坏。然而,然而,导致质膜完整性丧失的分子机制以及铁死亡症膜损伤的性质和大小仍未被探索。其他形式的坏死细胞死亡,如坏死性死亡、或毒素诱导的细胞死亡对质膜的损伤导致离子通量的激活。在这些情况下,Ca2+通量与膜修复机制的激活有关。转运所需的核内体分选复合体(ESCRT)机制似乎发挥了关键的平衡作用,可以延迟坏死和焦亡中的细胞死亡。
在不同的细胞模型中,研究了Erastin-1和RSL3触发铁死亡时质膜通透性的分子机制。利用活细胞成像和流式细胞术,我们并行追踪了铁死亡不同特征的动力学。我们发现在铁死亡过程中脂质过氧化发生在胞质Ca2+持续增加和最终质膜破裂之前。我们还确定纳米孔的形成是铁死亡过程中触发质膜破裂的核心机制,因此,适当大小的渗透保护剂可以抑制质膜破裂。最后,将铁死亡中胞质Ca2+的增加与ESCRT-III机制的激活联系起来,该机制作为一种延迟细胞死亡的保护机制。这对免疫有影响,因为ESCRT-III的缺失可调节铁死亡细胞的细胞因子分泌,从而重塑铁死亡的炎症特征。研究结果支持ESCRT-III机制在调节坏死过程中平衡膜损伤和调节免疫结果的一般作用。
技术路线:
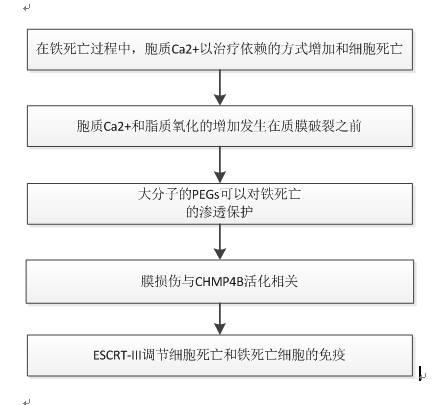
一、胞浆内Ca2+的持续增加是铁死亡的一个标志

在使用Erastin-1或RSL3处理的小鼠成纤维细胞(NIH-3T3)中,我们通过活细胞共聚焦成像(图1A, B)和流式细胞术(图1C H)检测细胞浆Ca2+水平,同时检测细胞形态和质膜破裂的变化。我们使用氟-4乙酰氧基甲基(氟-4 AM)作为Ca2+指示剂[27]的荧光形式,来观察细胞内Ca2+水平,PI作为不可逆质膜破坏和细胞死亡的标记。
在使用Erastin-1或RSL3处理NIH-3T3细胞后,胞浆Ca2+浓度明显升高(图1A, B)。这伴随着细胞形状的改变,包括细胞圆形和出现单个肿胀水泡,随后质膜完整性完全破裂。当用RSL3处理人类纤维肉瘤细胞(HT-1080)和人类乳腺癌细胞(Mda-157)时,也可以看到类似的事件(图S1)。在所有的细胞模型系统中,最终的膜破坏导致细胞内Ca2+和fluo - 4am染料的损失,尽管动力学和扩展取决于所使用的铁下垂诱导物和所研究的细胞系(图1和S1)。胞浆Ca2+、细胞圆化和质膜破裂的增加均被铁死亡抑制剂铁他汀-1 (Fer- 1)特异性抑制,但坏死抑制剂坏死性他汀-1 (necc -1s)和泛半胱天酶抑制剂zVAD均未被抑制,表明所有这些事件都是铁死亡的特征(图1A F)。
与NIH-3T3细胞类似,fer1也完全抑制了RSL3处理后HT-1080和Mda-157细胞胞浆Ca2+的增加和细胞死亡(图S1)。
我们通过流式细胞术平行追踪fluo - 4am和PI荧光的时间过程(图1G, H)。独立于治疗,胞浆Ca2+在质膜破裂前数小时就出现了增加。
在erastin -1处理的细胞中,我们发现fer1并没有完全消除胞浆内Ca2+的增加(图1A),约40%的细胞群保留fluo - 4am阳性(图1C, G)。
相反,当RSL3诱导铁死亡时,fer1完全阻止胞质Ca2+的增加(图1B, D, H)。这些结果表明,Erastin诱导了两种不同的Ca2+信号通路:一个与铁死亡无关,另一个与铁死亡特异。
胞质Ca2+的晚期增加可以被认为是铁死亡的标志,因为它被fer1抑制,在Erastin-1或RSL3-诱导的铁死亡中很常见。
二、脂质氧化先于胞质Ca2+的增加和质膜的破裂
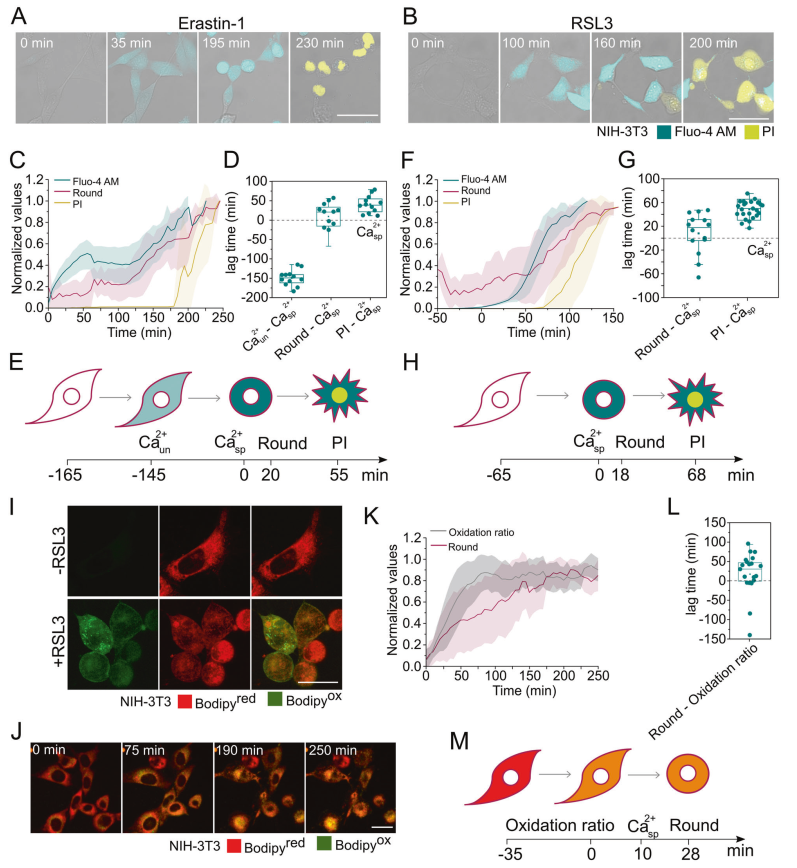
使用活细胞共聚焦显微镜在单细胞水平上量化了fluo - 4am信号的增加、细胞圆度和PI摄入。从单细胞动力学曲线(图2C, F, K)来看,计算了实现每种铁死亡表型50%变化(t50)所需的时间。
这使得我们可以设置铁死亡过程中每个过程之间的延迟时间(图2D, G, L)。
与使用的铁晶体触发器无关,胞质Ca2+的增加先于细胞圆化和完全的质膜塌陷(图2A, B)。
然而,流式细胞术实验表明(图1G),在存在Erastin-1的情况下,细胞内Ca2+的增加是一个两阶段的过程,具有两相行为(图2C)。
第一个事件在最大Ca2+信号的40%左右达到饱和,对应于不相关的钙(Ca2+ un)增加,因为它没有被fer1抑制(图1)。
第二种Ca2+升高,这是RSL3处理的常见现象,并被fer1抑制(图1H和2F),对应于胞浆内Ca2+升高,特异性于铁下垂(Ca2+ sp)。
在时间上,Ca2+ un在Erastin-1处理后增加,随后是Ca2+ sp上升,细胞圆角和最终的PI摄入量(图2C E)。
相比之下,rsl3处理的细胞具有独特的特异性Ca2+升高事件,随后是细胞圆整和最终的PI摄入(图2F-H)。
为了观察膜中的脂质过氧化,我们使用了脂质过氧化传感器C11 BODIPY 581/591。RSL3处理确实促进了质膜和亚细胞膜的脂质过氧化,可以通过增加BODIPY (BODIPYox)的绿色荧光信号来检测(图2I)。接下来,我们平行追踪氧化率和细胞圆角的变化(图2J, K)。脂质过氧化先于细胞圆角。考虑到胞浆Ca2+的增加到细胞圆角的滞后时间始终低于脂质过氧化到细胞圆角的滞后时间,我们可以估计,Ca2+的增加发生在脂质过氧化之后(图2M)。
这一估计是基于fluo - 4am增加的独立动力学(图2fh)和BODIPY氧化率(图2K, L)之间的外推。
三、渗透活性药物保护细胞免受铁死亡
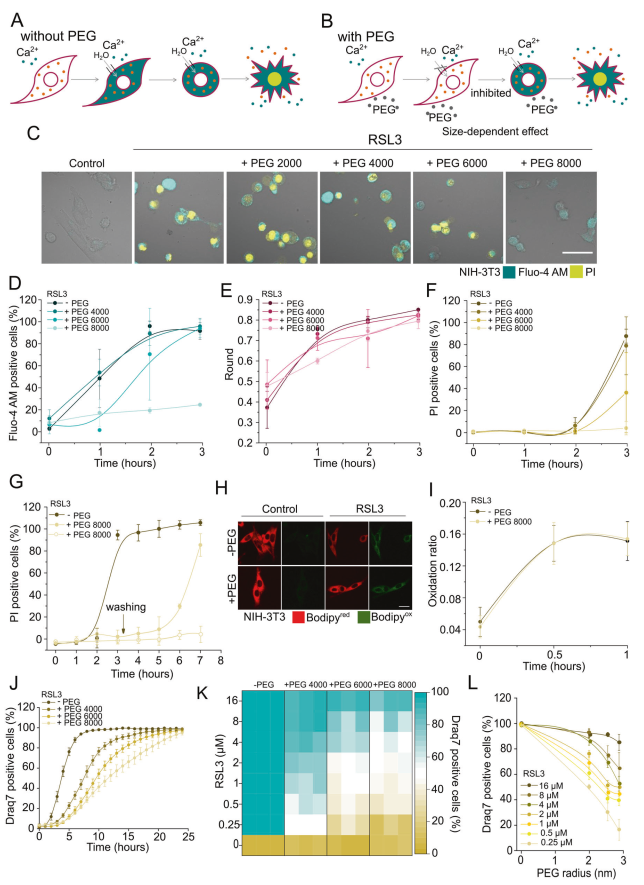
孔的形成是不同类型调控细胞死亡的共同特征,包括凋亡[29]、坏死[13]和焦亡[30]。质膜孔的打开导致水分子的净流入,这是由于高浓度的不能通过膜孔的细胞内大分子造成的渗透不平衡的结果(图3A)。可以通过添加适当大小的不能通过孔进入细胞的渗透保护剂来阻止这种影响,从而平衡细胞内渗透压、水流入和随之而来的细胞崩溃(图3B)。由此可见,聚乙二醇(peg)的渗透作用可以调节膜孔的渗透性,而离子通道的渗透性则不受调节。为了研究在铁死亡细胞中观察到的质膜通透性是否与膜孔有关,我们评估了不同大小的peg对不同铁死亡的动力学和程度的影响。
更小的peg的添加达到4000,并没有阻止胞浆Ca2+的增加,细胞圆角或细胞死亡(图3C F和S2)。
相比之下,高分子量peg(6000和8000)存在时,细胞浆Ca2+水平的升高和细胞死亡都以大小依赖的方式延迟(图3D, F和S2D)。
在PEG 8000的存在下,我们还观察到细胞舍圆动力学的延迟(图3E)。这些结果表明,胞浆Ca2+的增加、细胞圆润和质膜破裂都是由渗透力驱动的事件。值得注意的是,PEG 8000对铁死亡的保护作用在洗涤后恢复,这表明随着时间的推移,膜损伤是稳定的(图3G)。我们还发现,PEG 8000不能防止rsl3处理的NIH-3T3细胞的脂质过氧化(图3H, I)。
值得注意的是,对于所有使用的PEG大小,当NIH-3T3细胞处理较长时间(24小时)时,细胞死亡恢复(图3J)。
peg对铁死亡动力学的抑制作用也随着RSL3浓度的增加而降低(图3K、L和S3A)。
以在低浓度RSL3下能够起到保护作用的PEG大小作为参考,我们可以粗略估计在2.5 nm半径附近的质膜穿孔部分较小的尺寸(图3L)。
四、ESCRT-III复合物在铁死亡过程中被激活并拮抗细胞死亡

最初,CHMP4B主要表现为均匀的胞浆分布,然而,在RSL3处理后,蛋白定位于不同的斑点,随着时间的推移,蛋白数量和荧光强度增加(图4A、B和S4)。
这一观察结果与报道的CHMP4B在坏死[22,23]和焦亡[17]中的行为相似,表明ESCRT-III复合体在铁死亡过程中被激活。
接下来,我们通过活细胞共聚焦成像在单细胞水平上量化了CHMP4B斑点形成与细胞质Ca2+浓度增加、细胞圆角和最终质膜破裂的时间相关性。CHMP4B斑点的形成大致与胞质Ca2+浓度的增加相吻合(图4C E和S4)。
此外,这些结果表明,细胞聚集在这两个事件发生的同一时间(图4C E),这与渗透力的假定作用是一致的。在细胞浆Ca2+水平持续升高、细胞圆化和esrt - iii复合体激活后发生最终的膜破裂,可能是当细胞修复机制最终被淹没时(图4B, E, F)。

PEG 8000也阻断了CHMP4B斑点的形成,这可能是抑制Ca2+通量的结果(图4G J)。
为了检验ESCRT-III在铁死亡中的功能作用,我们评估了敲除CHMP4B对NIH-3T3细胞死亡的影响(图5A, B)。
我们开始使用蛋白质组分析器XL细胞因子阵列试剂盒(图5C和S6)来确定铁下垂是否可以直接调节不同细胞系中的细胞因子分泌。
在铁下垂的诱导下,我们检测到出现细胞系和治疗依赖的细胞因子亚群水平的变化。此外,敲除CHMP4B改变了RSL3(图5C, D)或Erastin-1(图S6C)处理后获得的细胞因子谱。






