促癌小分子的新成员——LncRNA ITGB8-AS1
LncRNA在结直肠癌(CRC)的发生发展中发挥着重要作用,但大多数lncRNA在CRC中的功能及其分子机制尚不清楚。本文发现lncRNA ITGB8-AS1在CRC中高表达起到促癌作用,并且可能是潜在的治疗靶点。该文于2021年8月发表于《Molecular Therapy》IF:11.454杂志上。
技术路线:

主要实验结果:
1、ITGB8-AS1是CRC生长和迁移所必须的
作者在HCT116和DLD-1细胞系中敲除ITGB8-AS1后,发现两个细胞系的增殖和集落形成,以及细胞的迁移。在体内,敲除ITGB8-AS1后肿瘤的生长受到显著抑制。此外,作者还构建了ITGB8-AS1过表达载体验证ITGB8-AS1对肿瘤的影响,实验证明ITGB8-AS1是CRC生长和迁移所必须的。
2、在CRC中ITGB8-AS1正调控Focal黏附信号通路
作者对ITGB8-AS1敲除的细胞和对照细胞进行转录组测序,挖掘差异表达基因,并对其进行KEGG分析,发现差异表达基因主要富集与Focal黏附信号通路。如图1,作者使用WB检测了该通路中的几个关键基因,发现敲除ITGB8-AS1后两个细胞系中他们的表达或磷酸化都显著下降。这些结果表明在CRC中ITGB8-AS1正调控Focal黏附信号通路。
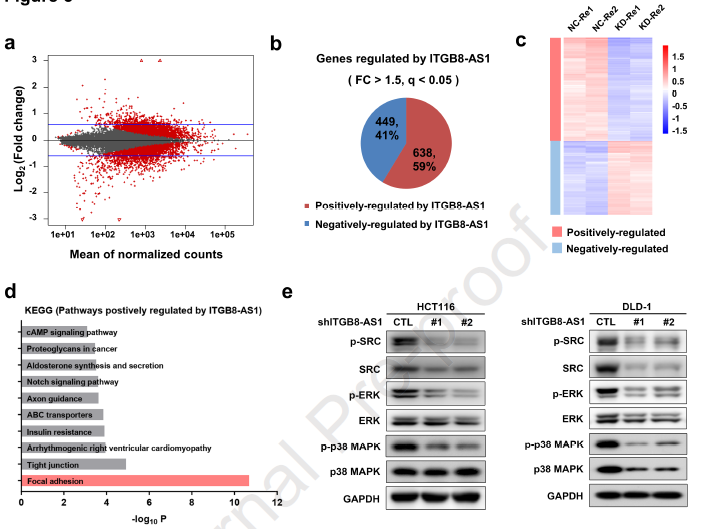
图1 ITGB8-AS1正调控Focal黏附信号通路
3、ITGB8-AS1作为miR-33b-5p和let-7d-5p/let-7d-5p的海绵调节整合素的表达
为了探究ITGB8-AS1调节Focal黏附信号通路的机制,作者试图探究ITGB8-AS1的编码潜力。如图2所示,和ACTB不同,多核糖体谱分析表明ITGB8-AS1富集于free-RNA组分,表明其没有编码能力,随后作者使用FISH分析了ITGB8-AS1的细胞质定位,发现其主要分布在细胞质中。这些提示ITGB8-AS1可能以ceRNA机制发挥作用。
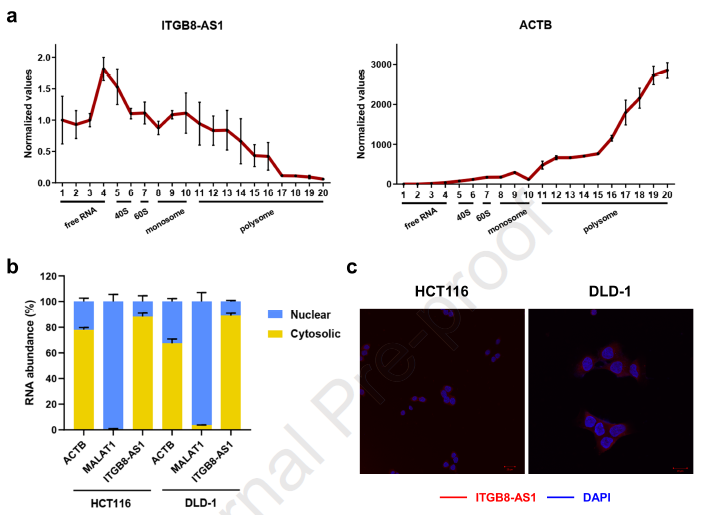
图2 ITGB8-AS1在CRC细胞中的编码潜能及亚细胞定位分析
为了验证ITGB8-AS1是否以ceRNA发挥作用,作者在线预测并构建了以ITGB8-AS1为中心的ceRNA调控网络。随后,敲除ITGB8-AS1后检测miRNA靶向的mRNA的表达,结果表明ITGA3,ITGA5和ITGB3的表达在两个细胞系中都显著下降,而过表达ITGB8-AS1后他们的表达都显著升高(图3)。值得一提的是ITGA3,ITGA5和ITGB3都是整合素家族基因。

图3 ITGB8-AS1海绵吸附miRNA调控整合素的表达
为了进一步确定哪些miRNA在连接ITGB8-AS1和整合素基因中起作用,作者在HCT116细胞中进行挽救试验。如图4所示,miR-33b-5p抑制剂可以显著挽救因ITGB8-AS1敲除导致的ITGA3,ITGA5和ITGB3基因表达下调,而其余的miRNA抑制剂则不行。此外,RIP结果表明ITGB8-AS1显著富集于AGO2蛋白蛋白复合物中,而双荧光素酶实验表明ITGB8-AS1和miR-33b-5p,以及let-7c-5p/let-7d-5p之间存在直接作用。以上表明ITGB8-AS1可以海绵吸附miR-33b-5p和let-7c-5p/let-7d-5p以调节ITGA3和ITGB3的表达进而作用于CRC的进展。图5的实验结果证实了这一结论。
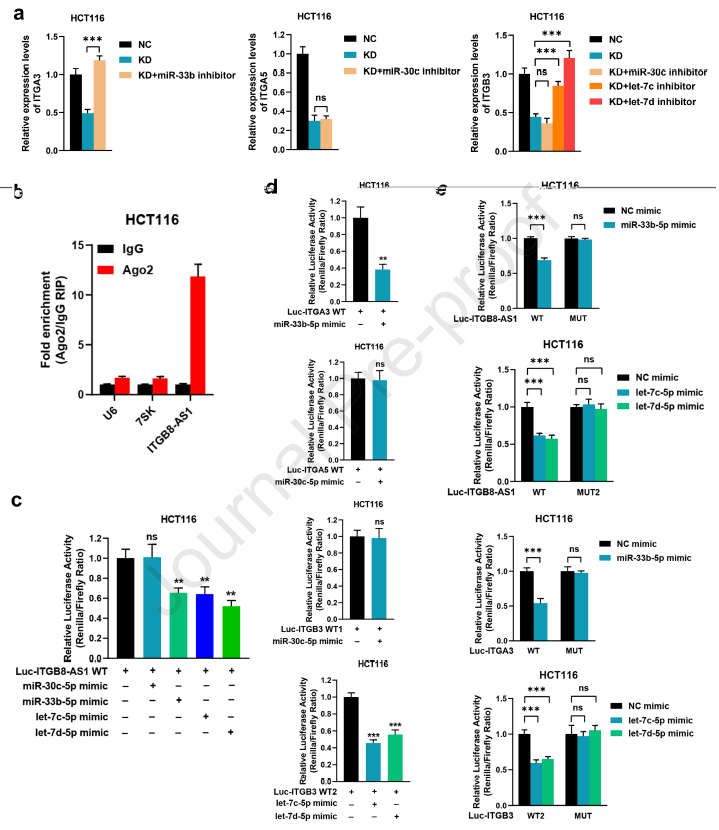
图4 ITGB8-AS1/miRNA/integrins的ceRNA网络验证

图5 ITGB8-AS1海绵吸附miR-33b-5p和let-7c-5p/let-7d-5p促进CRC生长迁移
4、ITGB8-AS1可作为CRC的潜在诊断和预测biomarker
使用GEPIA在线数据库预测了ITGB8-AS1在结肠癌和直肠腺癌中的表达,结果显示ITGB8-AS1在肿瘤样本中高表达。随后作者检测了14对术后CRC组织和对应的癌旁中ITGB8-AS1的表达,同样是癌组织高于癌旁。为了探究ITGB8-AS1在液体活检中的作用,作者检测了7例健康对照和CRC患者血浆中ITGB8-AS1的表达,得出了一样的结果。此外,在一个独立队列结果中,血浆ITGB8-AS1水平与肿瘤分化显著正相关。III期和IV期患者血浆ITGB8-AS1水平均高于I-II期患者。淋巴结受累者易出现高ITGB8-AS1血浆水平,但差异无统计学意义。而年龄、性别、原发肿瘤位置和远端转移与则ITGB8-AS1的血浆水平无关。ITGB8-AS1的血浆水平还与其靶基因表达表现出正相关性。这些结果表明ITGB8-AS1可作为CRC的诊断和预测生物标志物。

图6 ITGB8-AS1可作为CRC的潜在诊断和预测biomarker
5、ITGB8-AS1是治疗CRC的潜在靶点
如前文所述,ITGB8-AS1在CRC中上调并促进CRC的恶性行为,这为针对该lncRNA的治疗提供了理论依据。为了探索ITGB8-AS1抑制的治疗潜力,针对ITGB8-AS1的反义寡核苷酸(ASO)被应用于各种CRC临床前模型,包括患者来源的异种移植(PDX)。如图7a-c所示,ITGB8-AS1-ASO显著抑制细胞的增殖和集落形成。为了验证在体内靶向ITGB8-AS1的活性,进行PDX和HCT116来源的异种移植。结果发现ITGB8-AS1-ASO的抗肿瘤效率在CRC PDX和HCT116细胞负荷的小鼠中都可显著抑制肿瘤生长(图7d-e),同样也可以抑制肿瘤的肝转移,并且miR-33b-5p,let-7c-5p和let-7d-5p抑制剂都可以缓解ITGB8-AS1-ASO的抗肿瘤效果(图7f-g)。因此,ITGB8-AS1可以作为靶向治疗CRC的新靶点,而ASO似乎是一种有潜力的治疗方式。

图7 ITGB8-AS1是CRC潜在的治疗靶点
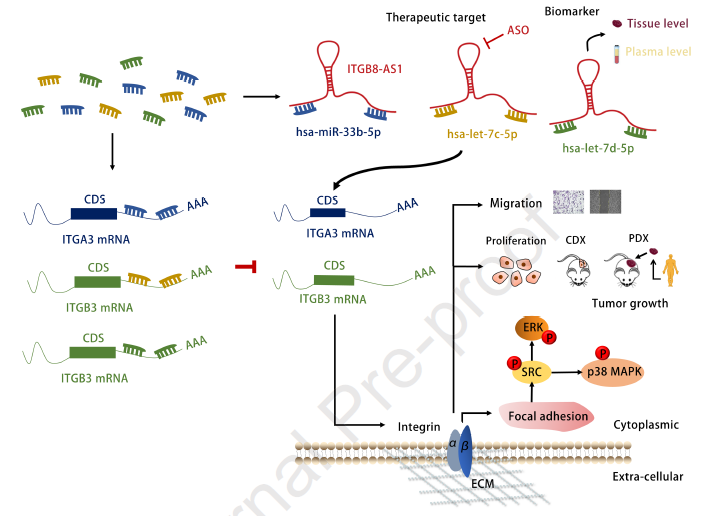
图8本研究的机制模型图
ITGB8-AS1通过吸附miR-33b-5p来调节ITGA3的表达,同时通过let-7c-5p和let-7d-5p来调节ITGB3的表达,然后激活整合素介导的Focal粘附信号。ITGB8-AS1可作为CRC患者新的治疗靶点和循环生物标志物。
参考文献:
Lin X, Zhuang S, Chen X, Du J, Zhong L, Ding J, Wang L, Yi J, Hu G, Tang G, Luo X, Liu W, Ye F, LncRNA ITGB8-AS1 functions as a ceRNA to promote colorectal cancer growth and migration through integrin-mediated focal adhesion signaling, Molecular Therapy (2021), doi: https://doi.org/10.1016/j.ymthe.2021.08.011.






