小CDD|外泌体:【细胞交互】+【分子交互】,一文get研究思路
在胶质瘤恶性进展中,作者发现外泌体来源的circWDR62诱导胶质瘤细胞对替莫唑胺(TMZ)产生抗性并促进细胞增殖、迁移和侵袭潜能。体内和体外实验表明,circWDR62通过调节miR-370-3p/MGMT轴促进胶质瘤恶性表型。本文于2022年7月发表在《Cell Death Disease》杂志上,IF=9.685。
技术路线图

主要结果
1)在对TMZ抵抗的胶质瘤细胞中circWDR62表达水平上调。
首先,为探索对TMZ抵抗的胶质瘤细胞来源的外泌体中circRNA的表达,作者通过梯度诱导的方法成功地建立了稳定对TMZ抵抗的胶质瘤细胞系(附图1A-F)并分离胶质瘤细胞来源的外泌体。透射电镜表明由U343-R和U343细胞分泌的外泌体是圆形的(图 1A)。外泌体浓度粒径分析表明U343-R细胞分泌的外泌体(U343-R-exos)和U343细胞分泌的外泌体(U343-exos)的浓度分别为12.0×107/mL和8.6×107/mL;此外,大多数颗粒的直径在50-250 nm;U343-R-exos和U343-exos直径的中位值分别是142.4 nm和129.6 nm(图 1B)。Western blot结果表明外泌体特异性标记CD63和TSG101在U343-R和U343细胞的外泌体表达(图 1C)。这些结果证实成功提取到标准外泌体。为筛选对TMZ敏感的胶质瘤细胞和耐TMZ的胶质瘤细胞分泌的外泌体之间的差异表达的circRNA,作者对U343-R-exos和U343-exos进行了微阵列分析。火山图结果提示与U343-exos相比,U343-R-exos中差异表达数千个circRNA(图 1D)。Hsa_circ_0050688是其中表达水平最高的circRNA之一(图 1E)。通过UCSC基因组数据库,作者将circ_0050688的结构和定位进行可视化分析并发现其来源于宿主基因WDR62(图1F)。此外,circPrimer软件表明circ_0050688由WDR62基因的第8-15外显子经反向剪接而形成。该circRNA成熟转录本的序列长度为1076 nt,作者称为“hsa_circ_0050688”或“ circWDR62”(图 1G)。此外,circWDR62能够抵抗RNase R的消化;然而,经过RNase R处理后,WDR62 mRNA的表达水平显著降低(图1H)。qRT-PCR显示,与原发肿瘤患者相比,来自复发的胶质瘤患者血清样本的外泌体中circWDR62的表达显著升高;胶质瘤患者中circWDR62的表达高于正常对照组(图 1I)。如图1J所示,复发性胶质瘤患者组织中circWDR62的表达高于原发性肿瘤患者。此外,Kaplan-Meier生存曲线显示,circWDR62低表达组复发性胶质瘤患者的生存率高于高表达组(图1K)。这些结果提示,外泌体circWDR62的高表达与胶质瘤的恶性进展有关。
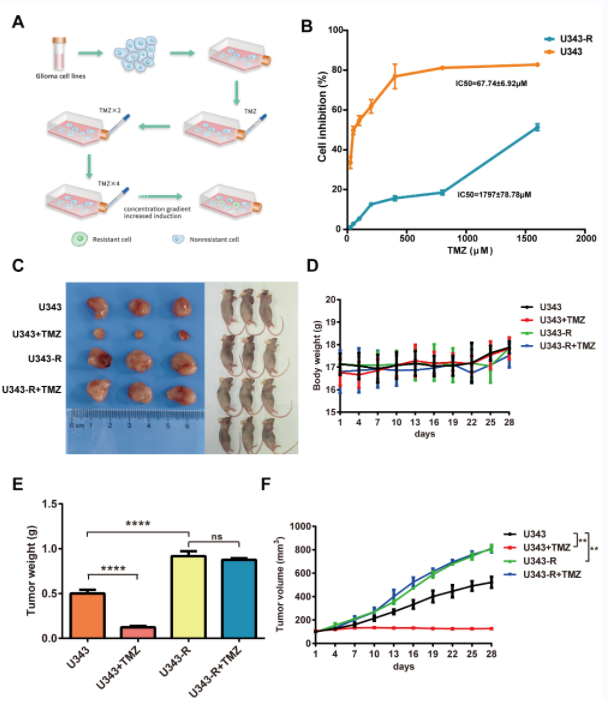
附图1 构建对TMZ抵抗的胶质瘤细胞
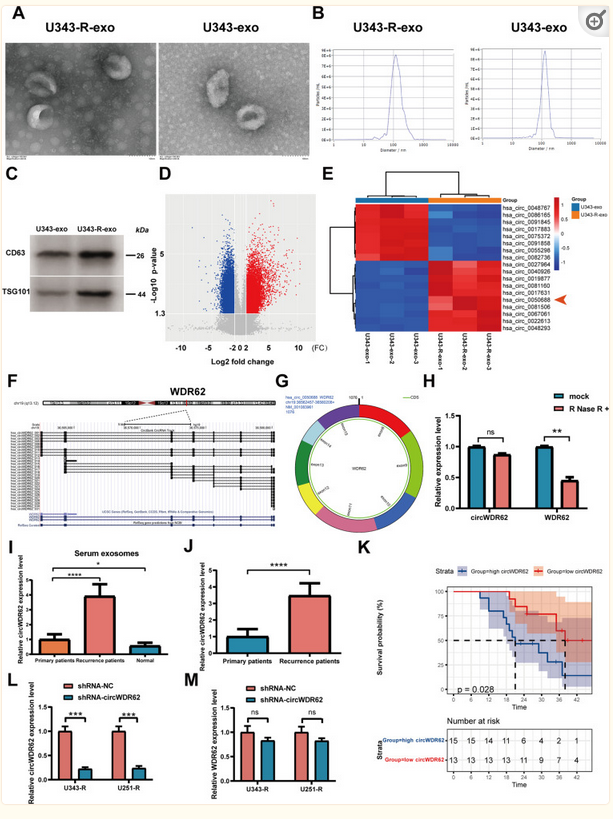
图1在对TMZ抵抗的的神经胶质瘤中circWDR62的表达上调。
2)敲低circWDR62抑制胶质瘤细胞对TMZ的抗性和恶性进展。
进一步,为探索circWDR62的生物学功能,作者评估了circWDR62在U343-R和U251-R细胞以及对TMZ敏感的细胞中的表达水平。qRT-PCR数据显示,与与对TMZ敏感的细胞及其分泌的外泌体相比,两种耐TMZ的神经胶质瘤细胞系及外泌体中circWDR62的表达水平显著增加(附图2A&B)。由于circWDR62在TMZ耐药细胞中的表达上调,因此构建circWDR62敲低模型用于评估其在胶质瘤细胞恶性表型中的作用(附图2C)。敲低circWDR62降低了U343-R和U251-R细胞中TMZ的IC50、增殖活性、迁移和侵袭(附图2D-G)。
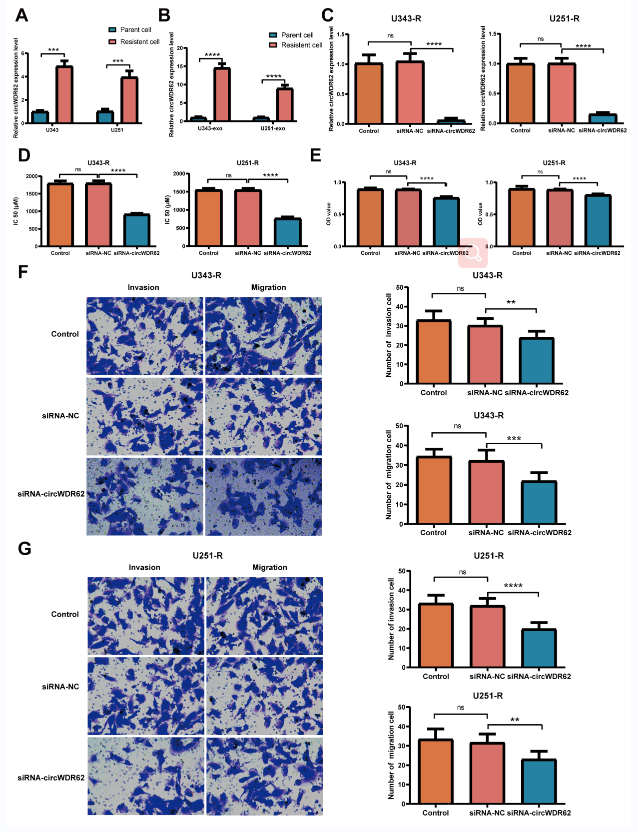
附图2敲低circWDR62抑制胶质瘤细胞对TMZ的抗性和恶性进展。
3)circWDR62通过充当miR-370-3p的海绵来促进神经胶质瘤细胞对TMZ的抗性和恶性表型
为了进一步阐明circWDR62的作用机理,作者通过circBank数据库筛选筛选到circWDR62潜在的miRNA。作者专注于9种与神经胶质瘤恶性进展和TMZ耐药性密切相关的miRNA,并具有强的结合潜能的miRNA作为后续筛查的关键研究对象。在这些miRNA中,miR-370-3p和circWDR62结合。Fish实验表明,miR-370-3p和circWDR62共同定位于在U343-R和U251-R细胞胞质中(图2A),这表明circWDR62可作为神经胶质瘤中的miRNA海绵。生物信息学分析预测了miR-370-3p和circWDR62之间潜在的结合位点(图2B)。双荧光素酶报告基因实验表明,miR-370-3p mimics显著抑制野生型circWDR62的荧光素酶的活性;但是对于突变型circWDR62的荧光素酶的活性没有显著的影响(图2C)。这些数据表明在胶质瘤细胞中circWDR62可吸附miR-370-3p。

图2 circWDR62通过充当miR-370-3p的海绵来促进TMZ耐药和细胞增殖。
为探索circWDR62的海绵机制,作者设计了circWDR62 shRNA和miR-370-3p抑制剂。转染sh-circWDR62后,显著下调了U343-R和U251-R细胞中circWDR62的表达(图1L)。然而,sh-circWDR62没有显著改变WDR62 mRNA表达(图1M)。qRT-PCR分析表明,将miR-370-3p抑制剂转染U343-R和U251-R细胞后miR-370-3p的表达中被下调(图2D)。与阴性对照组相比,敲低circWDR62后显著降低胶质瘤细胞的IC50,而miR-370-3p的抑制剂显着增加了U343-R和U251-R细胞的IC50。然而,在U343-R和U251-R细胞中敲低circWDR62引起的调控作用可被共转染miR-370-3p抑制剂削弱(图2E)。细胞实验表明,miR-370-3p抑制剂部分逆转了因敲低circWDR62对胶质瘤细胞恶性表型的抑制作用,包括细胞增殖(图2F)、迁移(图3A)、侵袭(图3B)、靶基因PCNA、增殖相关标记PCNA、EMT相关蛋白(图3C-G)。
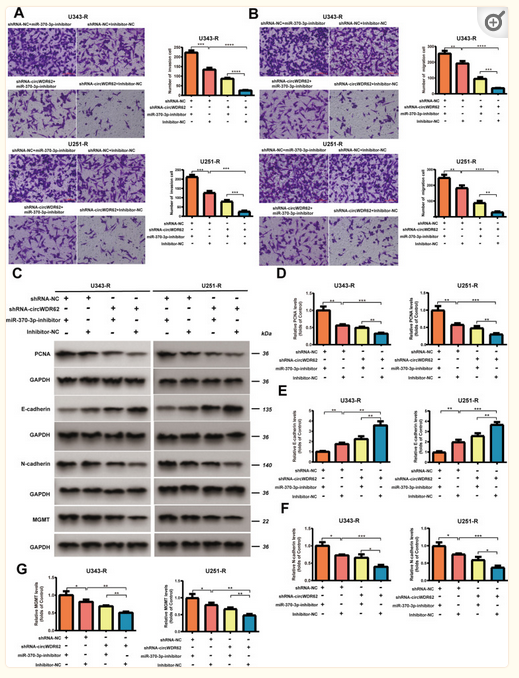
图3 circWDR62通过充当miR-370-3p的海绵来促进细胞侵袭和迁移。
4)MGMT是胶质瘤中circWDR62/miR-370-3p轴的直接靶基因。
采用三个数据库(miRDB, miRTarBase, and TargetScan)预测miRNA的潜在靶标mRNA。维恩图显示23个mRNA是miR-370-3p的最可能靶基因(图4A)。进一步,敲低circWDR62后作者检测了潜在靶基因的表达水平。结果表明FOXO1表达没有显着变化(图4B)和MGMT表达降低(图4C)。如图4D所示,生物信息学预测miR-370-3p和MGMT之间潜在的结合位点。与TMZ敏感的神经胶质瘤细胞相比,在TMZ耐药神经胶质瘤细胞中MGMT的蛋白质表达上调(图4E)。此外,GEPIA2数据库表明MGMT高表达与神经胶质瘤患者的总生存率较低有关(图4F)。此外,Fish结果表明,在U343-R和U251-R细胞中,miR-370-3p和MGMT共定位在细胞质(图4G)。
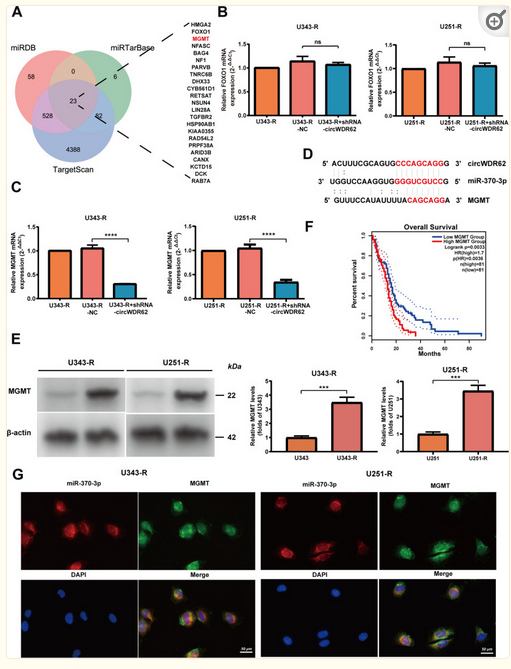
图4 MGMT是胶质瘤中circWDR62/miR-370-3p轴的直接靶基因。
进一步,挽救性实验证实过表达MGMT显著逆转了敲低circWDR62引起的胶质瘤细胞对TMZ抗性的抑制作用(图5A)。此外,MGMT过表达削弱了敲低circWDR62引起对胶质瘤细胞恶性表型的抑制作用,包括增殖、迁移和侵袭(图5B-D)。
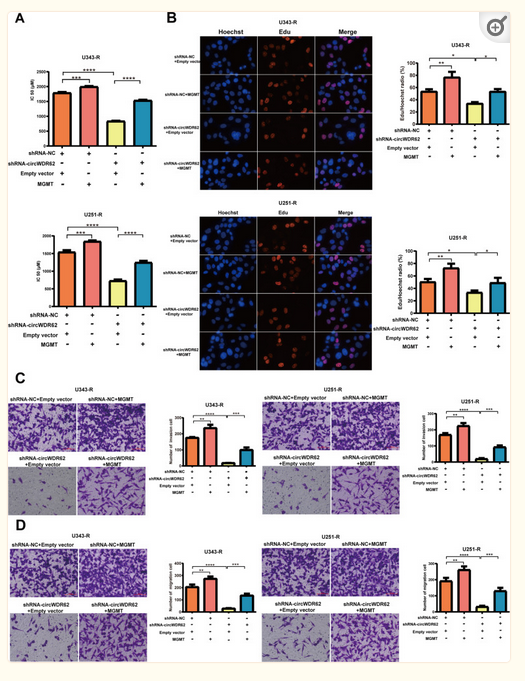
图 5 MGMT过表达逆转了circWDR62敲低诱导的TMZ耐药性和神经胶质瘤细胞的恶性进展。
5)circWDR62增强了胶质瘤TMZ耐药性和体内肿瘤的生长
为了在体内研究胶质瘤中circWDR62和TMZ抗性之间的关系,作者构建动物模型。每3天将TMZ注射到裸鼠体内。转染shRNA-circWDR62组的肿瘤显著小于对照组(图6A)。两组小鼠的体重没有显著性的差异(图6B)。然而,无论TMA处理如何,敲低circWDRE62显著抑制肿瘤体积和重量(图6C&D)。另外,与shRNA-NC组相比,在shRNA- circWDR62组中,肿瘤组织中circWDR62的表达被下调(图6E)。此外,WB分析证实,shRNA- circWDR62组中MGMT蛋白表达显著低于对照组(图6F)。
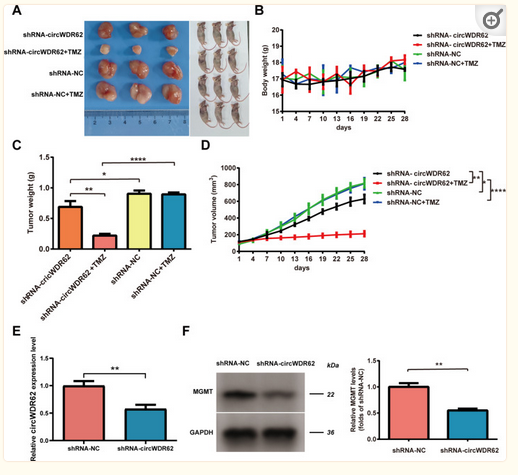
图6 CircWDR62增强胶质瘤细胞TMZ耐药性和体内肿瘤的生长。
6)在体外和体内外泌体介导的cirwDR62的传递诱导胶质瘤的TMZ耐药性和恶性进展
随后,将PKH67标记的TMZ抗胶质瘤细胞分泌的外泌体与TMZ敏感的胶质瘤细胞共培养(图7A)。可以观察到对TMA敏感的胶质瘤细胞摄取了对TMZ抵抗的胶质瘤细胞分泌的外泌体(图7B)。qRT-PCR分析结果表明,经过对TMZ抵抗的胶质瘤细胞衍生的外泌体处理后,对TMZ敏感的胶质瘤细胞后中cirwDR62的表达水平显著升高,并且随着外泌体的浓度增加,在TMZ敏感的神经胶质瘤细胞中的表达水平显着升高(图 7C)。但是,在添加GW4869(外泌体分泌阻滞剂)后,在Transwell共培养系统中cirwDR62的表达显著降低(图7D)。这些结果表明,来自于抗TMZ的胶质瘤的circWDR62可经由外泌体传递到对TMZ敏感的胶质瘤细胞中。进一步,细胞功能实验表明经过来源于对TMZ抵抗的胶质瘤细胞所分泌的外泌体处理后,U343和U251细胞的增殖、迁移和侵袭潜能显著增强(图7E-G)。

图7外泌体介导的cirWDR62递送可在体外诱导胶质瘤细胞的TMZ耐药性和恶性进展。
体内实验的结果表明,经过U343-R来源的外泌体处理后,U343组的肿瘤大小、体重和体积显著高于对照组;但是两组中小鼠的体重没有显著差异(图8A-D)。此外,与U343组相比,U343+U343-R-exo组中circWDR62的表达水平显著上调(图8E)。因此,circWDR62可以通过外泌体在TMZ抗性和TMZ敏感的神经胶质瘤细胞之间运输。来自TMZ耐药的细胞的外泌体circWDR62在受体敏感细胞中赋予了TMZ耐药性,同时还增强了受体敏感细胞的细胞增殖,迁移和侵袭。总而言之,这些结果表明外泌体来源于circWDR62通过吸附miR-370-3p来调节MGMT表达,从而导致质瘤的TMZ耐药性和恶性进展(图8F)。
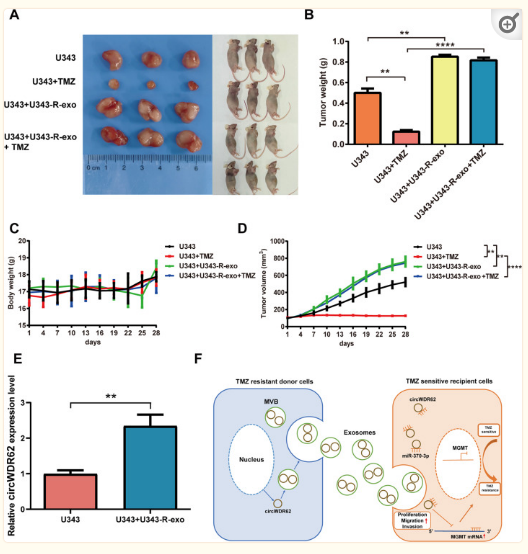
图8外泌体介导的cirWDR62传输可诱导体内神经胶质瘤的TMZ耐药性和恶性进展。
参考文献
Xiuchao Geng, Yuhao Zhang, Xiaomeng Lin, Zhaomu Zeng, Jun Hu, Liangchao Hao, Jianglong Xu, Xinjuan Wang, Hong Wang, Qiang Li. Exosomal circWDR62 promotes temozolomide resistance and malignant progression through regulation of the miR-370-3p/MGMT axis in glioma. Cell Death Dis. 2022 Jul 11;13(7):596. doi: 10.1038/s41419-022-05056-5.






