新发现——铁死亡促进椎间盘退化症
铁离子过载是老年群体中普遍现象。大量临床研究表明铁过载与椎间盘退化(IVDD)的发生率和病理进展之间的有关联。然而,铁参与IVDD进展的作用和潜在机制此前未见报道。本研究发现铁超载促进终板退变和钙化,从而导致IVDD进展,且这与氧化应激和铁死亡通路有关。本研究于2022年8月发表在《Free Radical Biology and Medicine》IF:8.101期刊上。
技术路线:

主要实验结果:
本研究将腰椎间盘突出症(LDH)患者分为严重椎间盘退化组(Pfirrmann grade IV or V)和不严重椎间盘退化组(Pfirrmann grade I II or III),如表2所示。结果发现,严重椎间盘退化组患者血清铁蛋白的水平在显著高于不严重组(图1A)。随后评估铁过载和软骨终板骨软骨炎的关系,将患者依据modic分为2组。结果显示与non-modic组比较,modic组患者的血清铁蛋白的水平显著升高(图1B)。
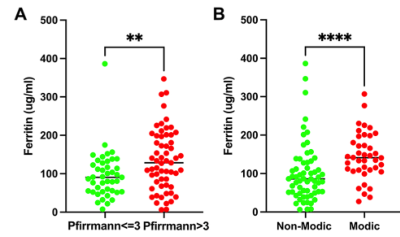
图1铁离子过载是IVDD的独立风险因子
之后通过建立小鼠铁超载模型,评估铁超载对椎间盘的直接影响。将小鼠随机分为3组,对照组,低剂量铁给药组,和高剂量铁给药组。HE染色结果显示高剂量铁给药组小鼠松质骨和终板组织可见大量铁沉积,此外,与对照组相比,低铁剂量组小鼠体内还观察到了铁沉积(图2A-2B)。对照组的椎间盘显示正常,表现为髓核含有丰富的脊索细胞,周围有大面积的细胞外基质,软骨终板由软骨细胞组成的透明软骨组成。铁过载组椎间盘出现退行性改变,其髓核变小,软骨终板深部可见含骨髓和矿化骨的骨组织。铁过载组的椎间盘组织学评分也显著高于对照组(图2D)。为进一步评估铁过载对软骨退化和钙化的影响,进行了micro-CT(图2C),三维骨结构定量显示铁超载组BV/TV较对照组明显升高,与对照组相比,铁超载组椎间盘高度降低(图2E-2F)。这些结果表明,在小鼠模型中过量的铁加速了软骨终板的退变,并以剂量依赖的方式加速了IVDD的进展。
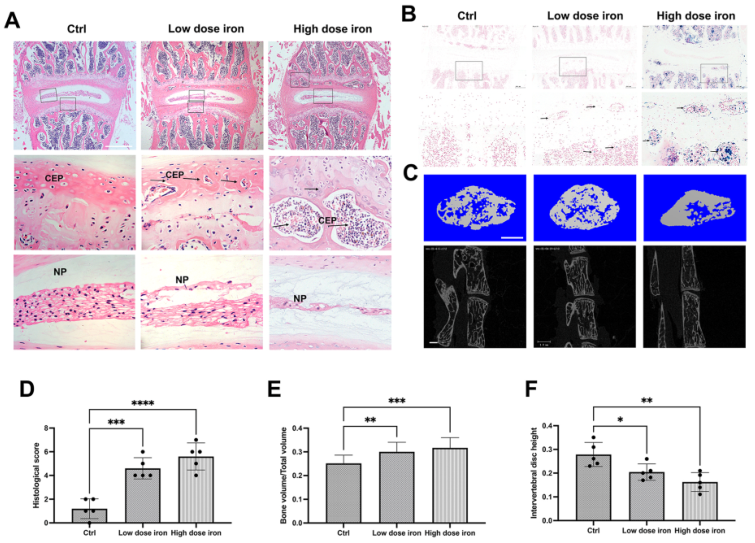
图2铁超载加速IVDD的发生,促进软骨终板钙化
3、铁超载促进终板软骨细胞矿化
IVDD是一个复杂的病理过程,包括纤维环和终板的退化,以及髓核的脱水和收缩。最近的研究表明,软骨终板退化和钙化是IVDD发生的初始和主要诱因。为进一步研究铁超载对终板退变和钙化的影响,采用免疫组化染色检测软骨细胞退化标志物COL10和OCN的表达水平。如图3A-3D所示,与对照组相比,铁超载组终板软骨细胞COL10和OCN阳性的比例更高。有趣的是,与低剂量铁组相比,高剂量铁组的COL10和OCN阳性细胞的百分比较低,尽管高剂量铁组存在含有骨髓和骨矿化的组织。
此前有报道称,铁对成骨有正、负两方面的作用,其作用取决于铁的浓度。为探讨过量铁对终板软骨细胞矿化的影响,分离终板软骨细胞,在添加不同浓度柠檬酸铁铵(FAC)的成骨分化培养基中培养21天。如图3E-H所示,10 μM FAC处理可导致终板软骨细胞钙沉积和ALP活性,而25 μM FAC对钙沉积和ALP活性均有抑制作用。在WB中也观察到类似的趋势,FAC处理后COL10和runx2蛋白表达增加,且呈剂量依赖性。此外,中度FAC处理显著促进终板软骨细胞COL10和RUNX2蛋白表达,而100 μM以上的FAC显著抑制成骨分化标志物RUNX2的表达(Fig. 3I-J)。
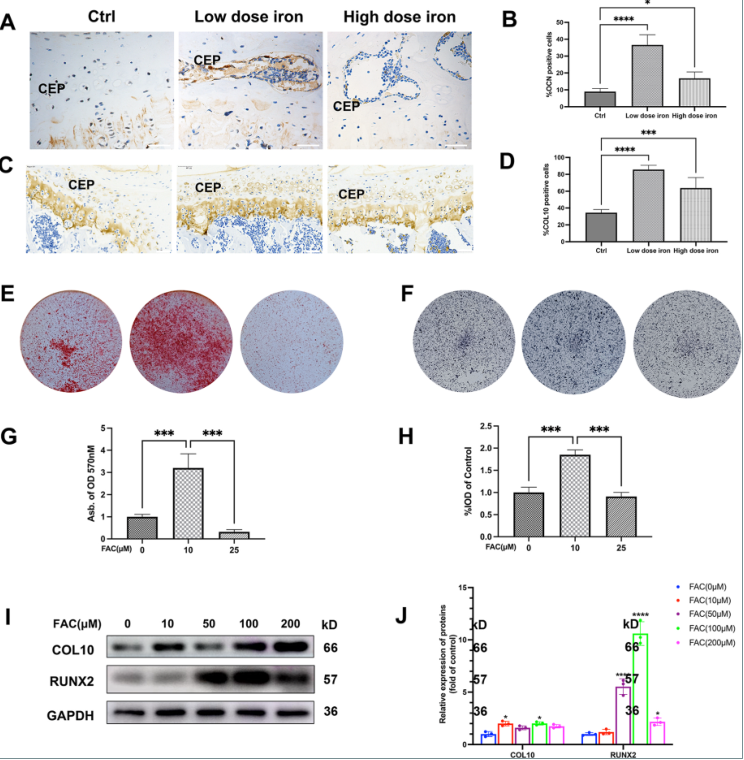
图3过量的铁促进终板软骨细胞的成骨分化和矿化
为了评估过量铁对终板软骨细胞的不利影响,软骨细胞用不同浓度的FAC处理24小时。如图4A所示,FAC处理降低II型胶原酶(COL2)的合成。同时WB显示FAC处理呈剂量依赖的方式促进MMP3和MMP13的表达,降低COL2的表达(图4B-C)。随后引入铁螯合剂DFO进一步验证铁过载的影响,结果显示DFO显著逆转FAC对软骨细胞的不利影响(图4D-G)。同时,DFO处理后SOX9和COL2表达水平上调,逆转了铁超载的影响。类似的结果在体内也被观察到,IHC显示铁超载抑制终板软骨细胞中COL2的表达并促进MMP3和MMP13的表达(图4H)。
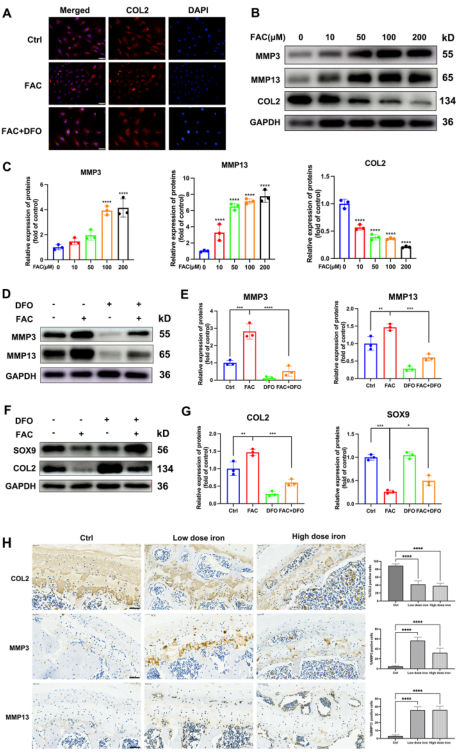
图4铁超载加速软骨终板退化
为研究铁超载促进终板软骨细胞退化的潜在机制,软骨细胞与浓度增加的FAC孵育24小时,并使用DCFH-DA探针评估ROS的产生。免疫荧光和流式分析结果显示FAC以剂量依赖的方式促进ROS的产生(图5A-C)。据报道氧化应激在终板矿化和退化中起作用。过量的铁通过芬顿反应催化产生剧毒的羟基自由基。因此,进一步研究过量铁诱导的氧化应激是否介导终板软骨细胞退化和矿化。为此,用100 μM的FAC和100 μM的抗氧化剂NAC处理原代软骨细胞。如图5D-G所示,100 μM FAC能显著促进MMP3和MMP13的表达,抑制SOX9和COL2的表达,NAC共处理显著逆转了铁超载对终板软骨细胞的有害影响。此外,NAC显著抑制FAC诱导的肥厚和成骨标志物COL10和RUNX2的表达(图5H-I)。这些结果表明,氧化应激在铁超载诱导终板软骨细胞退化和矿化过程中起重要作用。
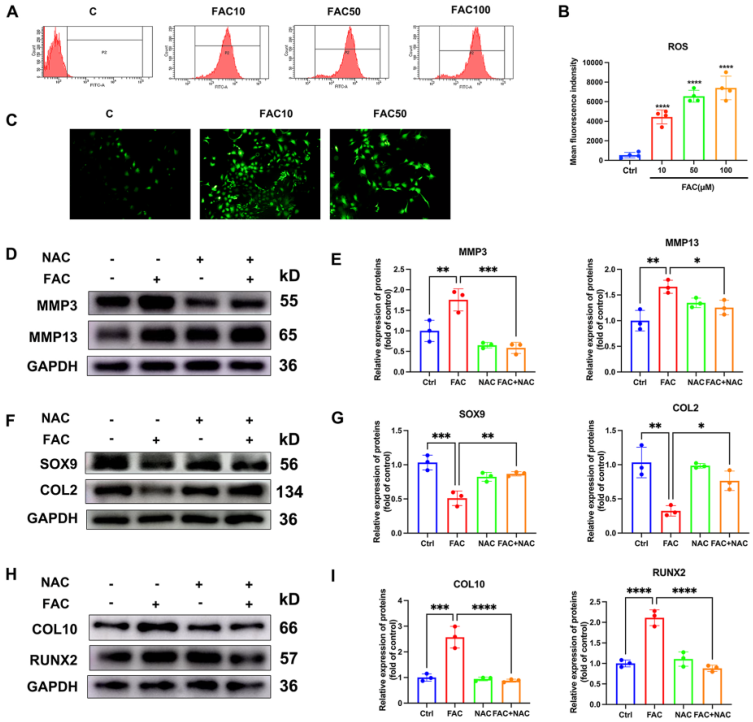
图5铁超载介导的氧化应激诱导终板软骨细胞退化和矿化
随后研究铁超载诱导的终板软骨细胞铁死亡是否参与了终板软骨细胞退化。WB显示GPX4和SLC7A11的表达随着FAC浓度的增加而逐渐减少,GPX4的免疫荧光染色支持了该结果,即FAC处理抑制铁死亡相关蛋白GPX4和SLC7A11的表达(图6A-C)。在小鼠铁超载模型中,也观察到GPX4表达以FAC剂量依赖的方式下降(图6E-F)。这些结果表明铁超载通过抑制GPX4和促进脂质过氧化(4HNE)促进体内终板软骨细胞铁死亡。此外,免疫荧光观察到健康软骨细胞的线粒体呈细长的线状,而经FAC处理后,缩短的线粒体数量显著增加(图6D)。铁螯合剂DFO可以挽救铁超载引起的GPX4和SLC7A11蛋白表达下降(图6I-J)。
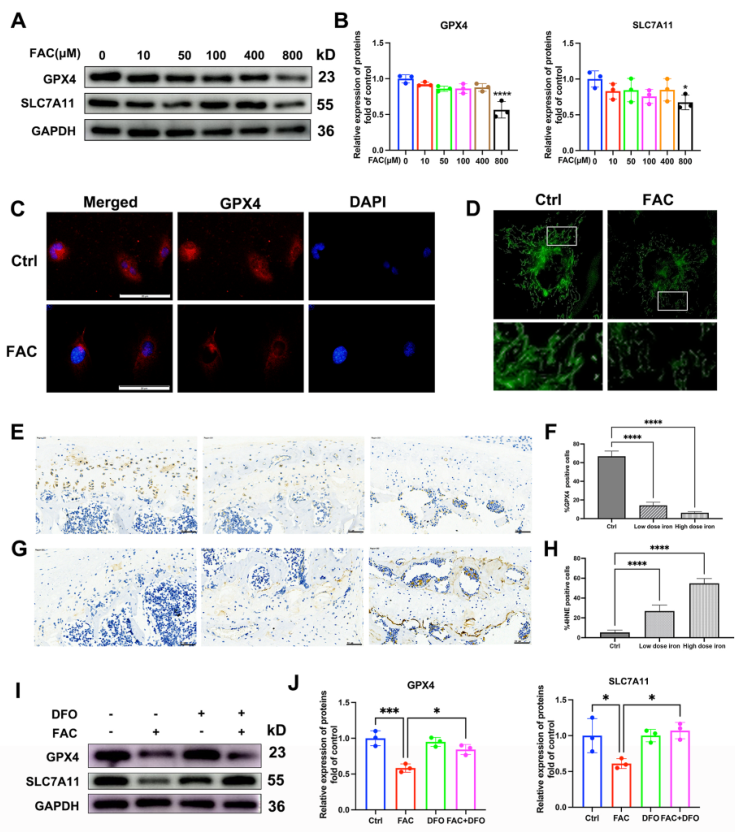
图6铁超载促进终板软骨细胞线粒体功能障碍和铁死亡
为进一步阐明铁死亡在铁超载诱导的终板软骨细胞退化中的作用,引入铁死亡抑制剂Fer-1。结果如图7所示,Fer-1共处理能显著逆转FAC诱导引起的COL2表达抑制、细胞凋亡、GPX4和SLC7A11表达下降、MMP3和MMP13表达升高。这些结果表明铁死亡参与终板软骨细胞退化。
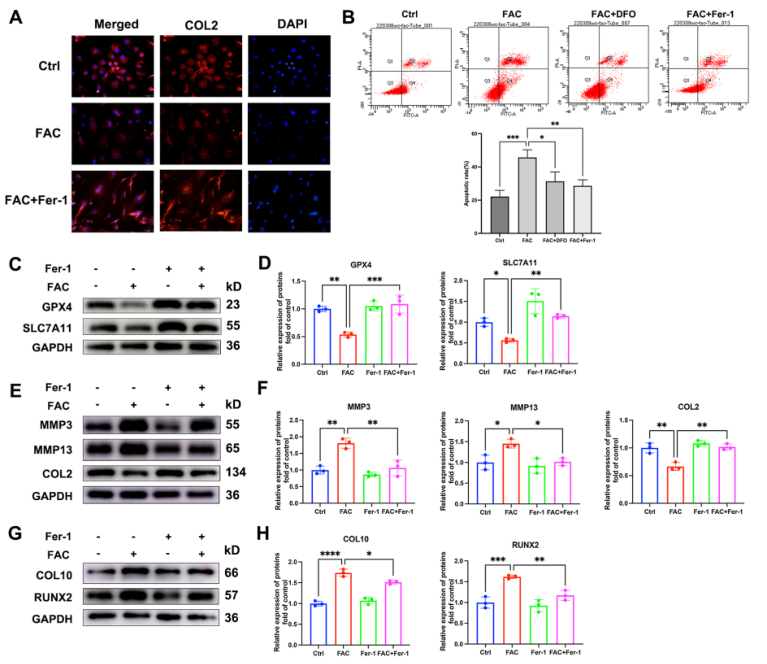
8、铁螯合、抗氧化剂和铁死亡抑制可减轻铁超载引起的椎间盘退化
进一步研究铁螯合剂DFO、抗氧化剂NAC和铁死亡抑制剂Fer-1是否能在小鼠体内抑制铁超载诱导的椎间盘退变。如图8A和8D所示,DFO、NAC和Fer-1处理显著抑制了铁超载诱导的IVDD。micro-CT分析显示DFO、NAC和Fer-1处理可以显著抑制铁超载诱导的终板钙化和椎间盘塌陷(图8B, E-F),也可以逆转铁超载引起的COL2,MMP3和MMP13表达改变(图8C, G-I)。这些体内实验的结果证实了氧化应激和铁死亡在铁超载诱导的椎间盘退化中发挥重要作用。
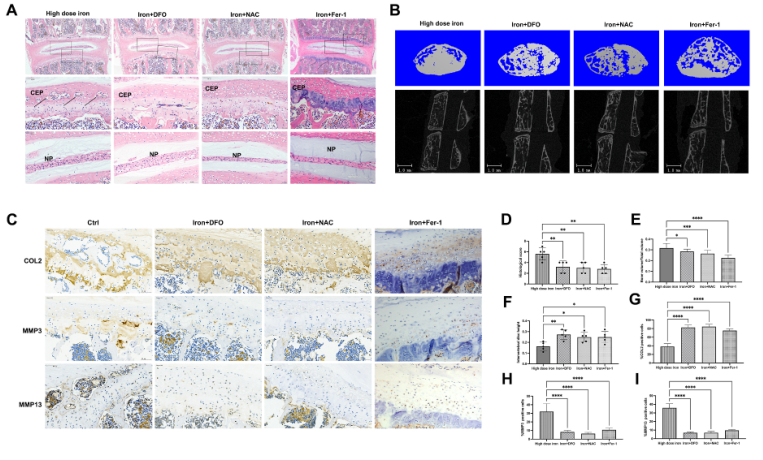
图8铁螯合、抗氧化剂和铁死亡抑制可减轻铁超载引起的椎间盘退化
本研究首次证明了铁超载是IVDD进展的危险因素。作者提出,由铁超载触发的氧化应激和铁死亡可以促进软骨终板退化和钙化,从而导致IVDD的进展。降低铁含量、抑制氧化应激和抑制铁死亡是铁超载诱导IVDD的有效治疗机制。
参考文献:
Wang Wenchao., Jing Xingzhi., Du Ting., Ren Jiabin., Liu Xiaoyang., Chen Feifei., Shao Yuandong., Sun Shengyao., Yang Guihe., Cui Xingang.(2022). Iron overload promotes intervertebral disc degeneration via inducing oxidative stress and ferroptosis in endplate chondrocytes. Free Radic Biol Med, 190(undefined), 234-246. doi:10.1016/j.freeradbiomed.2022.08.018






