一个新的tRNA衍生片段AS-TdR-007333通过HSPB1/MED29和ELK4/MED29轴促进非小细胞肺癌的恶性进展
肺癌是最常见的癌症类型,非小细胞肺癌(non-small cell lung cancer,NSCLC)占所有肺癌病例的85%。尽管近年来诊断和治疗方法取得了长足的进步,但NSCLC患者的总体5 年生存率仍不能令人满意。尽管大量研究表明多种癌基因和抑癌基因参与了NSCLC的发病机制,但NSCLC致癌的分子基础仍未完全阐明。因此,仍有必要探索NSCLC中未知的分子机制,以确定新的诊断和治疗靶点。该研究发表于《Journal of Hematology & Oncology》,IF: 23.168。
技术路线:
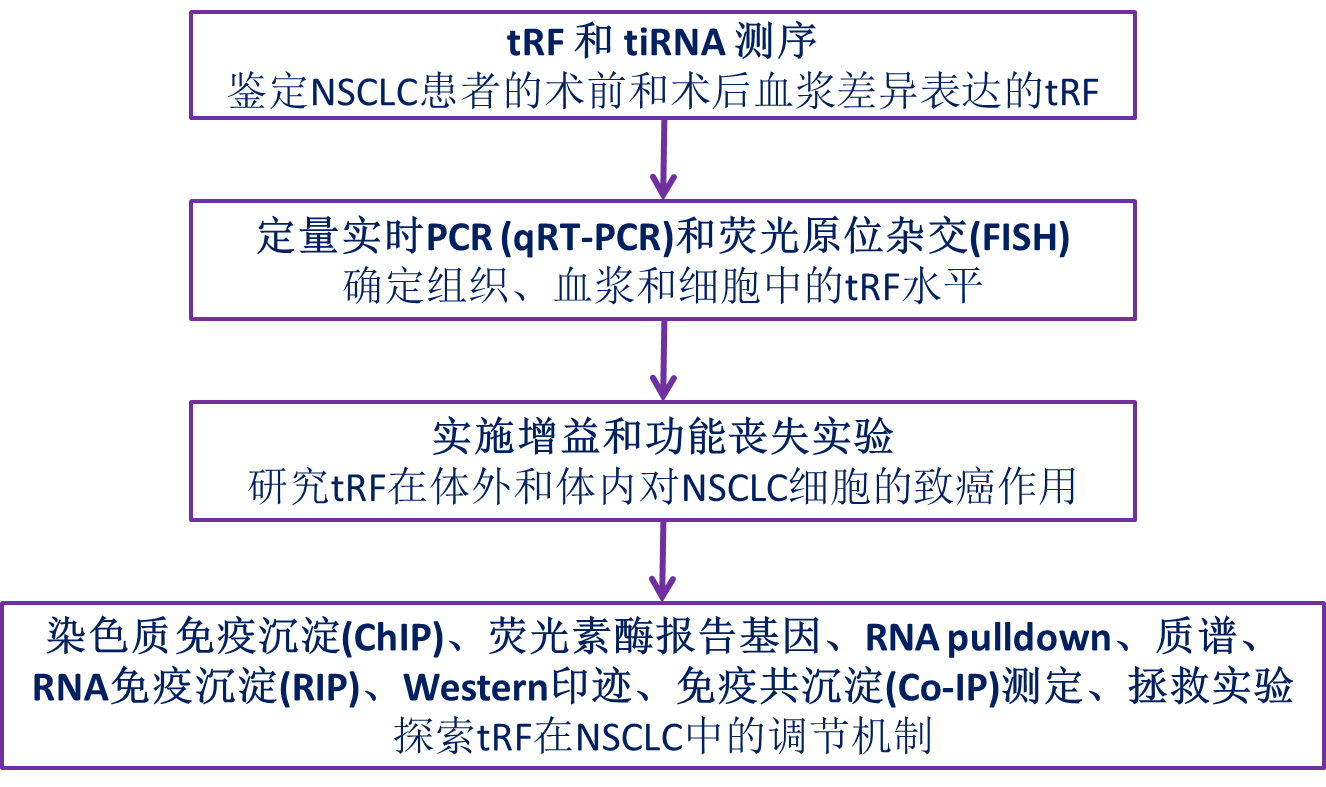
主要研究结果:
1. 循环tRF在NSCLC患者术前和术后血浆样本中的表达差异
为了识别和表征NSCLC中差异表达的循环tRF,作者比较了来自NSCLC患者的9对术前和术后血浆样本之间的tRF表达谱。tRF和tiRNA测序显示tRF表达谱在术前和术后血浆样本之间存在显著差异(图1A)。循环tRFs的长度范围为15至50个核苷酸(nt),其中 53.97%和30.11%的tRFs分别在20至23(nt)和31至33 nt之间(图1B)。值得注意的是,术后血浆中大多数 tRFs 的表达水平显著低于术前血浆样品中的表达水平(图1B),表明上调的血浆tRFs与NSCLC中肿瘤的存在有关。堆叠图表明,通过切割成具有相同序列的片段,可以从不同的tRNA产生一种类型的tRF或tiRNA(图1C, D)。饼图分析显示,大多数血浆tRF来源于tRNA的5'端。同样,tiRNA系列更多地属于tiRNA-5(图1E, F)。
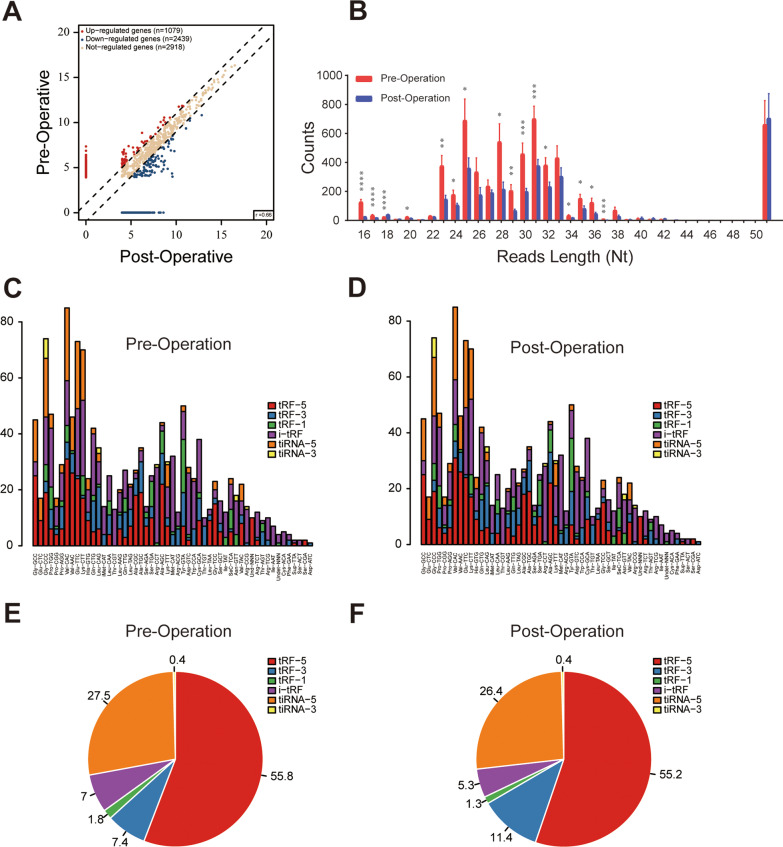
图1 NSCLC患者血浆tRF谱的特征
2. tRF AS-tDR-007333在NSCLC中上调
在倍数变化≥2.0 和P < 0.05 的截止标准下,与手术后血浆样品相比,作者在手术前血浆样品中鉴定出4个上调的tRF和4个下调的tRF。其中AS-tDR-007333是一种新的tRF,以前在tRF数据库中没有报道过。AS-tDR-007333长28 nt,在tRNA-Gly-GCC的5'末端的位点1至28处切割。qRT-PCR检测证实,NSCLC患者术前血浆中AS-tDR-007333的表达水平显著(P =0.0312)高于术后血浆样本(图2A)。在由NSCLC患者 (n=29) 和健康对照 (n=45) 的血浆组成的额外样品组中的qRT-PCR分析显示,NSCLC患者中的血浆 AS-tDR-007333 浓度显著高于健康对照(图2B)。接受者操作特征(ROC)分析表明曲线下面积(AUC)为0.9379(敏感性=97.78%,特异性=79.31%)(图2C),表明血浆AS-tDR-007333 水平具有作为NSCLC诊断生物标志物的高潜力。此外,NSCLC细胞系(PC9、HCC827、NCI-H226和A549)中AS-tDR-007333的表达水平也高于正常人支气管上皮细胞(BEAS-2B)中的表达水平(图2D)。此外,非小细胞肺癌肿瘤组织(n=9)中AS-tDR-007333的表达水平显著(P <0.0001)高于相邻正常组织(n=9)(图2E)。综合来看,多条证据明确表明 AS-tDR-007333在NSCLC中上调,可能在 NSCLC的发病机制中起关键作用。
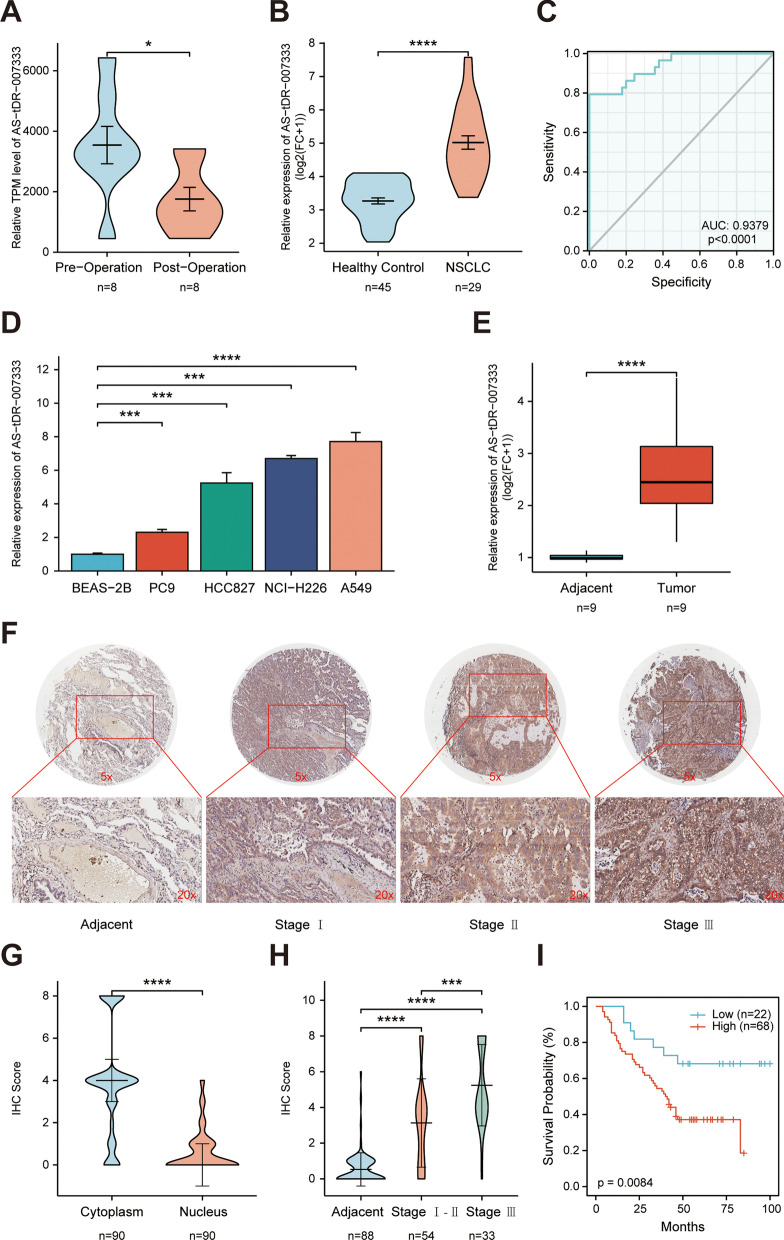
图2 tRF AS-tDR-007333在NSCLC中上调,并与NSCLC患者的较差预后相关
3. AS-tDR-007333的高表达与NSCLC预后不良有关
为了评估AS-tDR-007333在NSCLC患者中的临床意义,作者使用FISH来确定NSCLC 肿瘤组织和邻近组织中的 AS-tDR-007333 表达水平。结果表明,AS-tDR-007333 水平与TNM分期呈正相关(图2F,H),表明 AS-tDR-007333 水平与 NSCLC 的进展有关。此外,AS-tDR-007333 在细胞质中比在细胞核中更丰富(图2G)。因此,使用AS-tDR-007333的细胞质染色评分来评估AS-tDR-007333水平与NSCLC结局之间的关系。当根据 AS-tDR-007333 的细胞质评分将患者分为两组时(评分≥3,高表达;评分 < 3,低表达),Kaplan-Meier生存分析显示,较高的AS-tDR-007333水平与NSCLC患者的总生存期 (OS) 较低(对数秩检验,P=0.008,图2I)。此外,多变量Cox回归分析证实,AS-tDR-007333的较高表达与NSCLC中较短的生存时间显著相关(HR = 2.288;95%CI,1.0203–5.1310;P =0.04)。因此,临床数据强烈表明较高的AS-tDR-007333水平与NSCLC患者的不良预后相关。
4. AS-tDR-007333 促进 NSCLC 细胞的增殖和迁移
为了评估AS-tDR-007333在NSCLC中的生物学功能,作者在NSCLC细胞中进行了功能增益和功能丧失实验。CCK-8检测显示AS-tDR-007333的过表达显著促进细胞增殖,而 AS-tDR-007333的敲低显著抑制NSCLC细胞增殖(图3A-D)。为了检查AS-tDR-007333对NSCLC细胞增殖的影响是否反映了细胞周期转变,进行了流式细胞术分析以研究细胞周期进程。结果表明,通过AS-tDR-007333过表达,PC9 细胞在S期停滞,而AS-tDR-007333 的抑制降低了S期细胞的比率(图3E-H)。为了支持这些,在A549细胞中也观察到了类似的结果(图3I-L)。然后,作者使用transwell测定检查了AS-tDR-007333在NSCLC细胞中的侵袭能力。作者发现AS-tDR-007333过表达组中迁移的细胞数量显著高于对照组,而 AS-tDR-007333 抑制剂逆转了这些作用(图3M-Q)。

图3 AS-tDR-007333促进NSCLC细胞的增殖和迁移能力
5. AS-tDR-007333通过上调MED29增强NSCLC细胞增殖
为了探索受AS-tDR-007333调控的靶基因,作者将AS-tDR-007333转染到NSCLC细胞中。RNA-seq分析显示,过表达AS-tDR-007333的细胞中的转录组谱与NC细胞的转录组谱不同(图4A, B)。在差异表达的基因中,MED29通过AS-tDR-007333过表达显示出最高的上调(图4C)。基因本体(GO)分析表明,差异表达基因显著富集在细胞成分的介体复合物(MED)中(图4D)。基因集富集分析 (GSEA) 还显示MED途径基因,特别是MED29,在AS-tDR-007333过表达的细胞中富集。此外,非小细胞肺癌肿瘤组织中MED29的表达水平显著高于癌旁组织(图4E)。类似地,qRT-PCR 测定和蛋白质印迹分析证实MED29基因和蛋白质在NSCLC细胞中显著上调(图4F)。有趣的是,AS-tDR-007333的表达水平与MED29在NSCLC肿瘤组织中的表达水平呈正相关。总之,这些结果表明AS-tDR-007333诱导的MED29上调可能在NSCLC的发病机制中起重要作用。
为了验证AS-tDR-007333和MED29在NSCLC中的关系,作者将AS-tDR-007333转染到NSCLC细胞中。Western印迹和qRT-PCR分析表明,AS-tDR-007333的过表达显著促进了MED29的表达,而抑制AS-tDR-007333则降低了MED29的表达水平(图4G)。此外,CCK-8分析显示MED29的上调促进了A549和PC9细胞中的细胞增殖(图4H,I),而MED29 的敲低抑制了NSCLC细胞的生长速率(图4J,K)。此外,拯救试验表明,与单独转染 AS-tDR-007333相比,将AS-tDR-007333与si-MED29共转染到NSCLC细胞中导致细胞增殖显著降低,表明AS-tDR-007333的生物学功能部分依赖于MED29。总之,这些结果表明AS-tDR-007333促进了MED29的表达,MED29 随后作为癌基因增强了NSCLC细胞的增殖。

图4 AS-tDR-007333通过上调MED29增强NSCLC细胞增殖
6. AS-tDR-007333与表观遗传增强MED29转录的HSPB1相互作用
为了阐明AS-tDR-007333在NSCLC中发挥其生物学功能的机制,作者进行了RNA pull-down实验,然后在NSCLC细胞中进行了质谱分析(图5A)。作者发现AS-tDR-007333 与几种癌症相关的RNA结合蛋白沉淀,包括HSPB1、DHX9、ACTB、YBX3 和 ILF2(图 5B)。其中,作者对HSPB1特别感兴趣,因为HSPB1具有最高的匹配分数,并且据报道与NSCLC的发展和进展有关。使用抗HSPB1抗体的RIP测定证实 AS-tDR-007333与内源性HSPB1特异性结合(图5C)。计算蛋白质-RNA对接分析还表明HSPB1蛋白中的几个氨基酸残基对AS-tDR-007333结合至关重要(图5D)。这些数据表明,AS-tDR-007333可能通过直接结合NSCLC细胞中的HSPB1发挥其生物学功能。
确定AS-tDR-007333是否可以通过与HSPB1相互作用来调节NSCLC细胞增殖。作者首先检测了HSPB1在NSCLC细胞系和BEAS-2B细胞中的表达水平。qRT-PCR和Western blot 检测均一致显示HSPB1在NSCLC 细胞中的表达水平显著高于BEAS-2B细胞(图 5E、F)。通过将si-HSPB1和AS-tDR-007333 共转染到NSCLC细胞中的拯救实验表明,通过过表达AS-tDR-007333增加的细胞增殖能力可以被si-HSPB1显著降低(图5G-J),表明 AS-tDR-007333对NSCLC细胞增殖的影响在功能上至少部分依赖于HSPB1。
由于AS-tDR-007333可以与HSPB1相互作用并增强MED29的表达,作者假设 AS-tDR-007333可能通过调节HSPB1发挥其生物学功能,从而进一步改变MED29的表达和功能。为了验证作者的假设,作者将AS-tDR-007333及其抑制剂转染到NSCLC细胞中,发现AS-tDR-007333的过表达增加了HSPB1基因和蛋白质的表达水平,而 AS-tDR-007333 的敲低降低了 HSPB1 的表达(图6A-D)。有趣的是,敲低HSPB1不仅抑制了HSPB1 的表达,还抑制了MED29的表达(图6E, G)。Co-IP分析显示HSPB1可以与NSCLC细胞中的MED29结合(图6F),表明HSPB1和MED29之间存在潜在的相互作用。使用荧光素酶测定的救援实验证实,AS-tDR-007333的上调显著增加了MED29的启动子活性,而AS-tDR-007333与si-HSPB1的共转染降低了MED29启动子的活性(图6H)。在功能上,将MED29和si-HSPB1共转染到 NSCLC 细胞中显著抑制了MED29对细胞增殖的影响(图 6I,J)。总之,作者的结果表明AS-tDR-007333可以通过激活HSPB1-MED29相互作用来增强NSCLC细胞增殖。
组蛋白修饰在基因转录的表观遗传调控中起着至关重要的作用。由于UCSC基因组浏览器显示MED29启动子区域包含H3K4me1和H3K27ac,转录激活的组蛋白标记,作者检查了HSPB1表达是否可能影响MED29启动子中的组蛋白标记表达。JASPAR 数据库分析预测,HSPB1的MED29启动子区域有几个推定的结合位点。蛋白质印迹分析显示,与野生型细胞相比,si-HSPB1抑制了H3K4me1和H3K27ac的表达水平(图 6K)。此外,ChIP-qPCR 测定表明 HSPB1 的敲低显著降低了MED29启动子区域中的H3K4me1和 H3K27ac水平(图 6L,M)。因此,这些数据表明,AS-tDR-007333可能至少部分通过HSPB1介导的MED29启动子中的H3K4me1和H3K27ac修饰来促进癌细胞增殖。
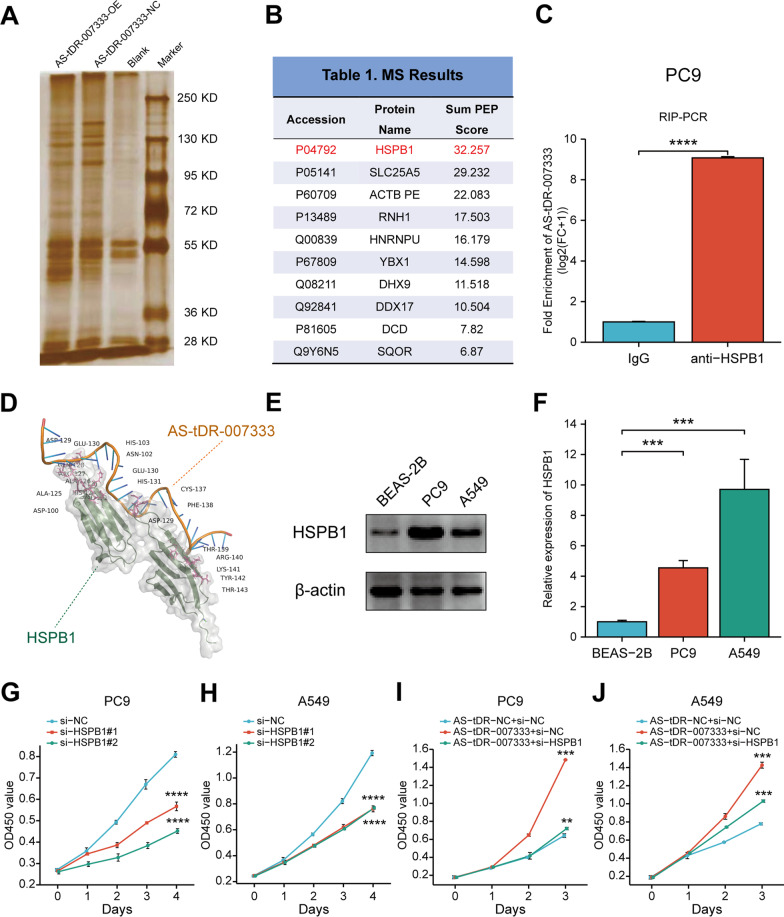
图5 AS-tDR-007333直接与NSCLC细胞中的HSPB1结合并相互作用
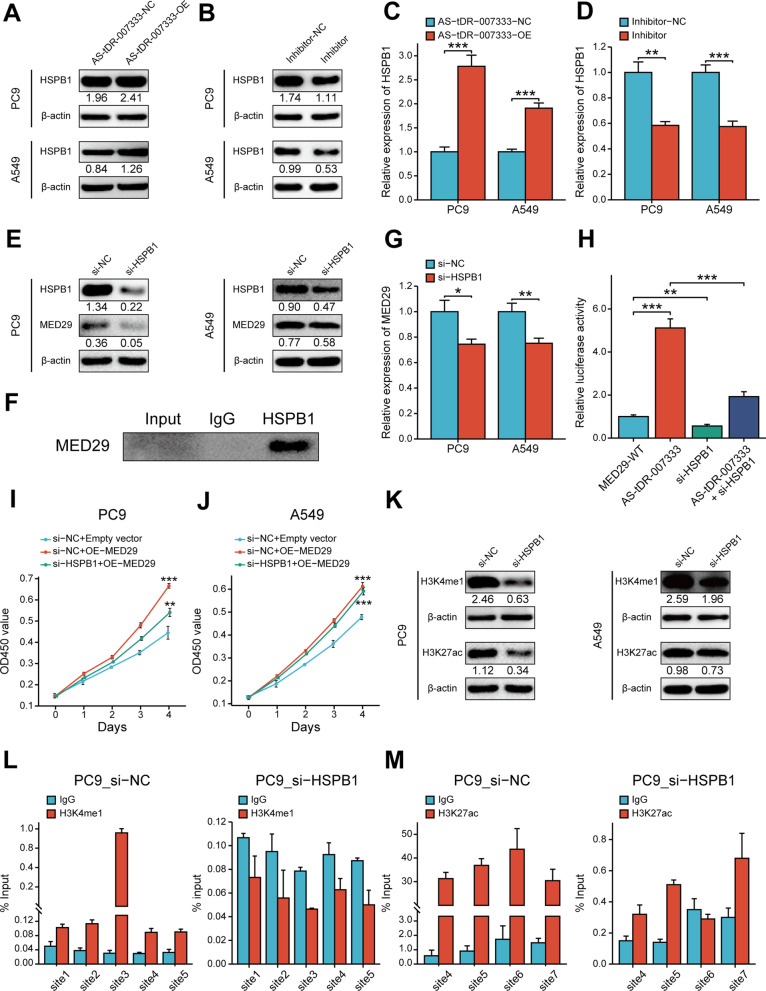
图6 AS-tDR-007333激活HSPB1以调节MED29启动子区域中的H3K4me1和H3K27ac水平
7. AS-tDR-00733 通过激活 ELK4 介导的转录调控上调 MED29
由于HSPB1-MED29相互作用只能部分解释MED29的表达,作者推测在 AS-tDR-007333相关的MED29表达调节中可能存在其他机制。因为有人提出转录因子 (TF) 可以靶向特定的MED亚基以诱导转录反应,作者推断MED29转录可能受特定转录因子的影响。使用JASPAR和UCSC数据库分析,作者发现MED29启动子包含转录因子ELK4的推定结合位点(图7A)。为了评估ELK4对NSCLC的影响,作者将si-ELK4转染到NSCLC 细胞中,发现si-ELK4显著抑制了NSCLC增殖(图7B, C)。为了确定 AS-tDR-007333是否可能影响ELK4的表达,作者将AS-tDR-007333转染到NSCLC细胞中。作者发现AS-tDR-007333的过表达显著促进了NSCLC细胞中ELK4的表达水平(图7D, E); 相反,抑制AS-tDR-007333显著降低了ELK4的表达(图7D, F)。救援实验进一步证实了AS-tDR-007333在NSCLC细胞增殖中与 si-ELK4 功能性相互作用(图7G,H)。为了研究ELK4是否可能直接影响 MED29 表达,作者进行了ChIP-PCR测定,证实ELK4直接与MED29基因的预测启动子区域结合(图7I)。荧光素酶报告基因检测显示,与NC载体细胞相比,ELK4的过表达显著增加了含有野生型结合位点的报告基因的荧光素酶活性(图7J)。然而,在ELK4与MED29的突变启动子的结合上,没有观察到荧光素酶活性的显著变化(图7J)。总的来说,这些发现表明AS-tDR-007333与ELK4相互作用以修改MED29启动子转录。
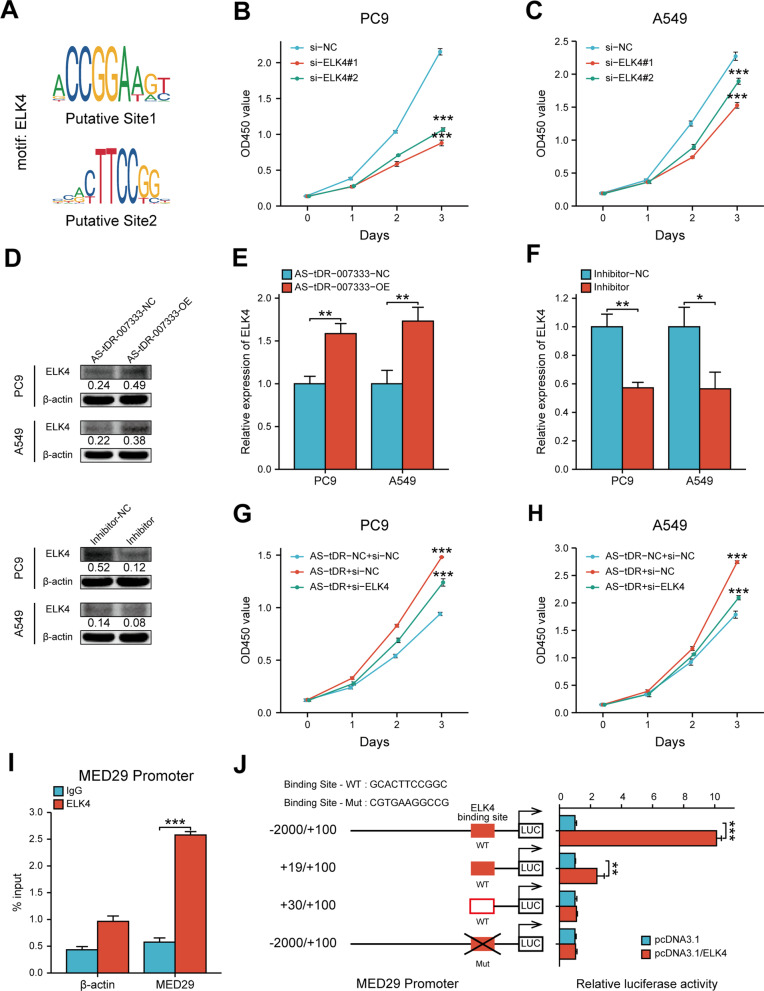
图7 AS-tDR-00733通过ELK4介导的转录激活调节MED29
8. 靶向 AS-tDR-007333 抑制体内 NSCLC 细胞生长
鉴于AS-tDR-007333在NSCLC中充当致癌tRF,作者假设抑制AS-tDR-007333可能对NSCLC具有治疗作用。评估AS-tDR-007333抑制剂在体内的治疗效果(图8A),作者合成了针对体内研究进行了优化修饰的AS-tDR-007333靶向抑制剂, 如图8B、C所示。在整个实验期间,AS-tDR-007333-inhibitor组的肿瘤体积明显小于NC或空白对照组,但在实验组之间没有观察到体重差异。此外,AS-tDR-007333抑制剂组的平均肿瘤重量显著低于对照组(P < 0.01)(图8D,E)。此外,与NC组和对照组相比,AS-tDR-007333抑制剂组异种移植肿瘤组织中AS-tDR-007333、HSPB1、ELK4和MED29的表达水平明显受到抑制(图8F-I)。此外,施用AS-tDR-007333抑制剂还抑制了异种移植肿瘤组织中 MED29 和 Ki-67 蛋白的表达水平(图8J)。因此,这些发现表明 AS-tDR-007333抑制剂可以通过抑制体内MED29的表达来抑制NSCLC肿瘤的生长。
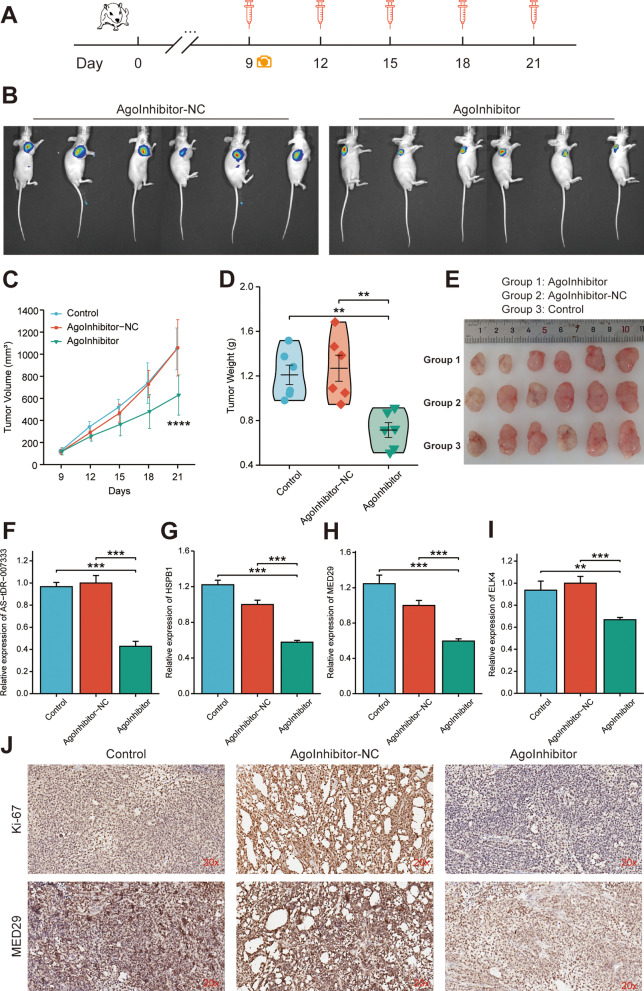
图8 用抑制剂靶向AS-tDR-007333可减少体内NSCLC肿瘤的生长
结论:
研究确定了一种新的致癌tRF,并揭示了AS-tDR-007333通过HSPB1-MED29和 ELK4-MED29轴促进NSCLC恶性肿瘤的新机制。AS-tDR-007333是NSCLC的潜在诊断或预后标志物和治疗靶点。

示意图显示了AS-tDR-007333如何通过HSPB1-MED29和ELK4-MED29轴促进非小细胞肺癌的恶性进展
参考文献:
Yang W, Gao K, Qian Y, Huang Y, Xiang Q, Chen C, Chen Q, Wang Y, Fang F, He Q, Chen S, Xiong J, Chen Y, Xie N, Zheng D, Zhai R. A novel tRNA-derived fragment AS-tDR-007333 promotes the malignancy of NSCLC via the HSPB1/MED29 and ELK4/MED29 axes. J Hematol Oncol. 2022 May 7;15(1):53. doi: 10.1186/s13045-022-01270-y. PMID: 35526007; PMCID: PMC9077895.






