一个新的长链非编码RNA SP100-AS1通过海绵化miR-622和稳定ATG3诱导结直肠癌放射抵抗
虽然放疗是治疗结直肠癌(CRC)的重要手段,但临床上放疗抵抗的发生率仍然很高。长链非编码RNA (lncRNA)通过在转录或翻译后水平调控基因或蛋白在结直肠癌放疗抵抗中发挥重要作用。该研究旨在鉴定与放射抗拒相关的新型lncRNA。该研究发表于《Cell Death & Differentiation》,IF:12.067。
技术路线:
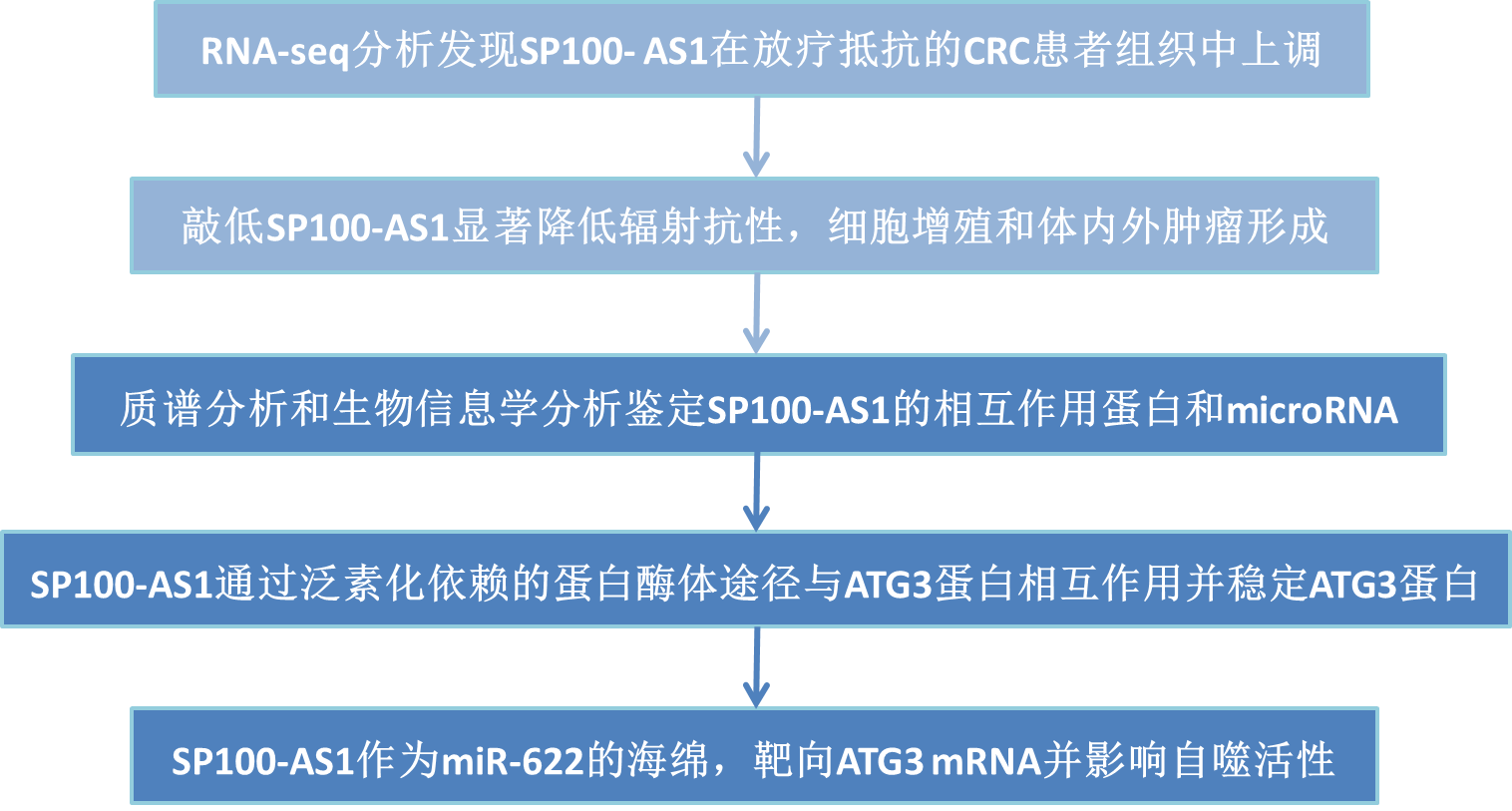
主要研究结果:
1. SP100-AS1表达上调与结直肠癌放疗抵抗相关
采用RNA-seq分析比较8例放疗敏感和8例放疗抵抗患者结直肠癌组织中lncRNA的差异表达(图1A)。结果表明,与辐射敏感样本相比,267个lncRNA在辐射抗拒样本中表达上调(图1B),其中SP100-AS1显著过表达。接下来,RT-qPCR分析表明,SP100-AS1在CRC组织(n = 44)中的表达显著高于癌旁正常组织(图1C)。综上所述,上述结果表明SP100-AS1可能在CRC进展中发挥重要作用。此外,研究者假设SP100-AS1可能通过其在放射抗拒组织中的异常表达调控CRC的放射敏感性。因此,研究者收集了具有放射敏感和放射抗拒临床特征的结直肠癌患者的组织。如图1D所示,放射抗拒的结直肠癌组织中SP100-AS1的表达量较高。综上所述,研究者的研究结果表明,SP100-AS1参与CRC的进展和放射抵抗。采用RT-qPCR检测正常人结肠黏膜上皮细胞NCM460和结直肠癌细胞株LS177T、HCT116、CT26、HCT8、HT29、LoVo和SW480中内源性SP100-AS1的表达(图1E)。结果表明,与正常上皮细胞株相比,CRC细胞中SP100-AS1的表达水平较高,尤其是在HCT116和SW480细胞株中,并用于后续实验。有趣的是,SP100-AS1的高表达与结直肠癌患者的不良生存相关(图1F)。综上所述,这些发现表明lncRNA SP100-AS1的过表达与CRC的放射抵抗和低生存率相关。
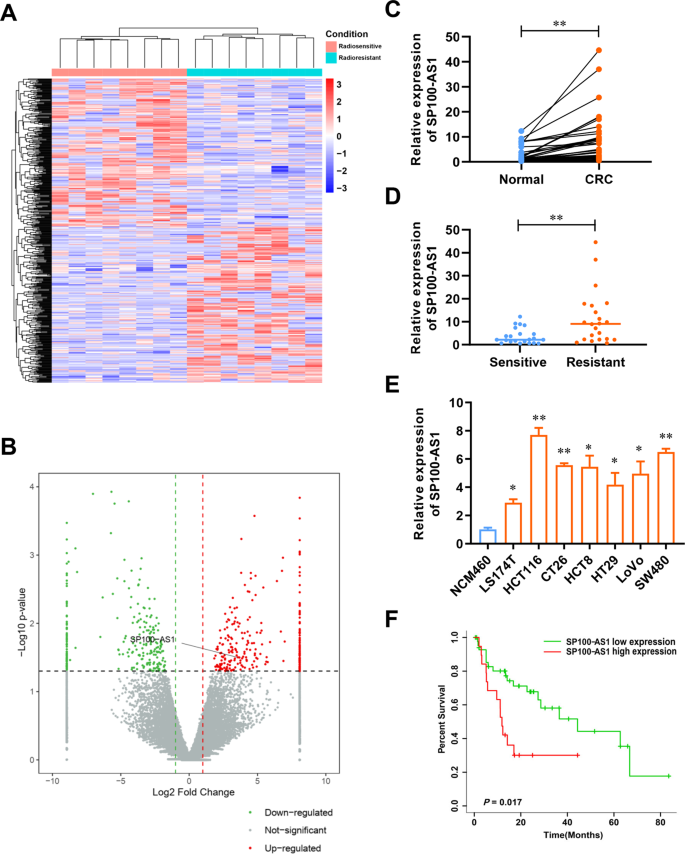
图1 SP100-AS1在CRC中表达上调,且与放疗呈正相关
2. 敲低SP100-AS1可增强结直肠癌的放射敏感性
在建立了SP100-AS1在CRC患者组织和细胞系中的异常表达模式后,研究者研究了这种lncRNA如何调节肿瘤细胞的增殖和生存。如前所述,SP100-AS1在HCT116和SW480细胞中以剂量依赖性方式表达最多(图1E)。克隆形成实验检测SP100-AS1对HCT116和SW480细胞放射敏感性的影响。值得注意的是,当SP100-AS1表达下调时,这两种细胞的放射敏感性显著增加(图2A, C)。此外,研究者对HCT116和SW480细胞在4 Gy剂量下的活力进行了研究,发现沉默SP100-AS1降低了细胞的增殖和活力(图2B, D)。
放射治疗引起的DNA双链断裂是公认的,必须在肿瘤进一步生长之前进行修复。这一发现强调需要开发一种新的方法来阻止DNA修复和阻止肿瘤生长,或至少减缓它们以延长患者的生存期。阻断DNA损伤修复是治疗CRC的一种特别有吸引力的策略,因为CRC对辐射具有高度抵抗力。正如预期的那样,抑制SP100-AS1可以诱导γ-H2AX的表达,γ-H2AX是DNA损伤的显著标志物(图2E)。接下来,作者分析SP100-AS1对细胞凋亡的影响。Annexin V/PI双染色显示,与对照组相比,SP100-AS1缺失显著增加了HCT116细胞的凋亡反应(图2F)。这表明SP100-AS1参与了CRC辐射诱导的DNA损伤和细胞凋亡。因此,敲低SP100-AS1可以增加CRC的放射敏感性。
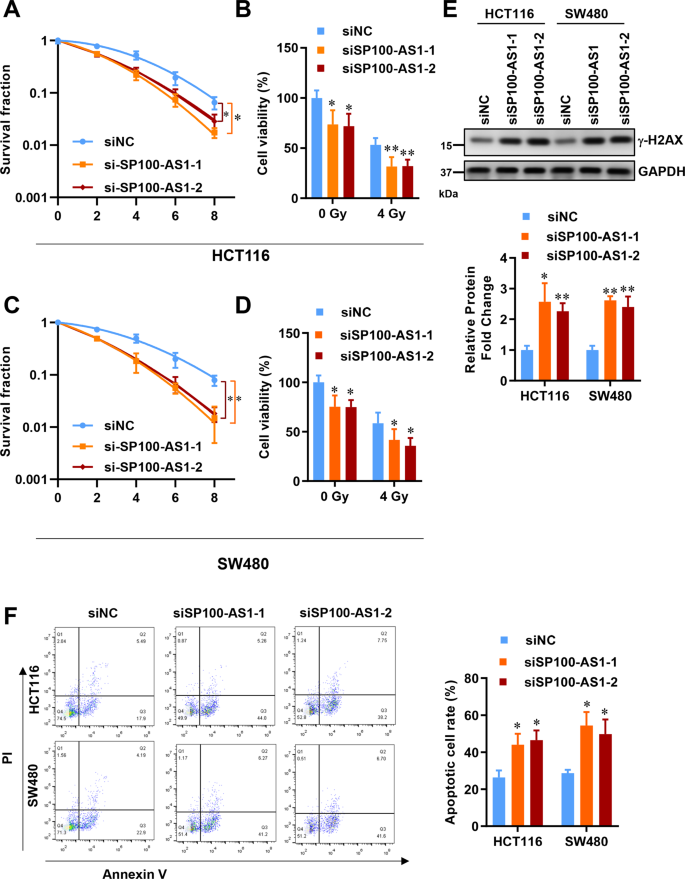
图2 SP100-AS1下调加重了辐射诱导的细胞死亡
通过建立BALB/c裸鼠移植瘤模型,研究SP100-AS1在体内的作用。如图3A所示,通过慢病毒感染HCT116细胞,SP100-AS1被稳定敲低,接种的异种移植瘤比对照组的肿瘤生长减慢。此外,IR后,与对照组相比,SP100 - AS1敲低的HCT116肿瘤细胞生长缓慢(图3A)。分割IR后,沉默SP100-AS1可进一步减缓CRC肿瘤的生长(图3B)。实验结束后,测量肿瘤重量(图3C)。随后,转移酶介导的dUTP缺口末端标记(TUNEL)实验表明,敲低SP100-AS1在2 Gy辐射下引起更多的DNA损伤,并降低Ki67染色,表明SP100-AS1下调抑制CRC的生长速度,尤其是在暴露于辐射时(图3D)。综上所述,这些结果表明,SP100-AS1沉默可以在体内外增强CRC的放射敏感性。
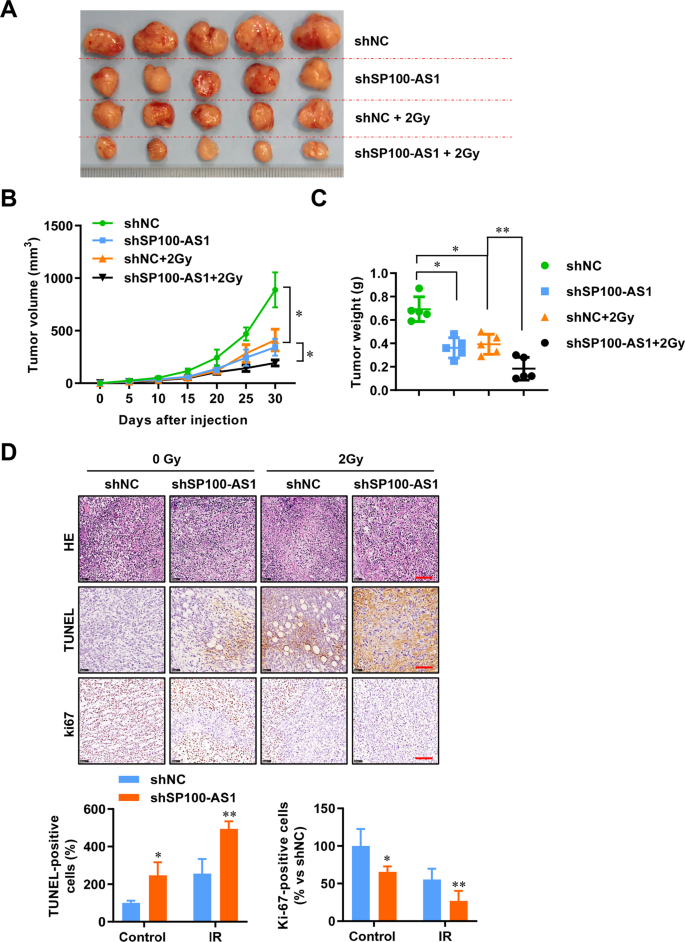
图3 SP100-AS1下调降低了受照结直肠癌细胞的体内生长
4. SP100-AS1通过自噬途径增加结直肠癌细胞的放射抵抗活性
自噬通路的激活在包括结直肠癌在内的多种肿瘤的放射抵抗中发挥重要作用。为了探究自噬通路是否参与HCT116和SW480细胞的辐射抗性,作者定量分析了敲低SP100-AS1后,自噬流标记物LC3-II和p62/SQSTM1的蛋白表达。结果显示LC3-II降低,p62蛋白水平升高(图4A)。此外,作者使用LC3-GFP-RFP报告系统来评估自噬体形成。LC3是一种与绿色和红色荧光蛋白融合的膜结合蛋白。与RFP不同,GFP在酸性环境中不稳定。相应计算RFP点位或RFP/GFP比值来测量自噬通量。敲低SP100-AS1后,用过表达LC3-GFP-RFP的慢病毒感染HCT116细胞,并给予相应水平的辐射处理。与之前的研究结果一致,与对照组相比,放射治疗对自噬的诱导作用要弱得多,自噬流显著减少(图4B)。此外,western blot和IHC分析表明,在IR处理的CRC异种移植瘤中,p62蛋白表达显著降低,LC3-II蛋白水平显著升高,而沉默SP100-AS1可以逆转这一情况。因此,这些结果得出结论,辐射可以诱导HCT116细胞的自噬,沉默SP100-AS1可以缓解这一效应。

图4 SP100-AS1通过自噬途径调控HCT116细胞增殖
5. SP100-AS1通过ATG5和Beclin1调控自噬通路
ATG5和Beclin1是宏观自噬通路的重要上游调控因子,过表达ATG5和Beclin1可直接激活自噬信号通路。因此,作者研究了SP100 - AS1调控的自噬是否可以通过过表达ATG5和Beclin1来拯救。在HCT116和SW480细胞中敲低SP100-AS1后,ATG5和Beclin1表达上调,并检测LC3-II的蛋白表达。如图5A所示,SP100-AS1下调导致的自噬流减少被ATG5或Beclin1上调所恢复。此外,Annexin V/PI双染后采用流式细胞术定量凋亡,表明上调ATG5和Beclin1可减少敲低SP100-AS1诱导的细胞凋亡(图5B)。如前所述,使用LC3-GFP-RFP慢病毒报告检测自噬流密度,并测量每个细胞的红色点状点数量。在HCT116细胞中,上调ATG5或Beclin1可以显著增加SP100-AS1敲低后的点状细胞数量(图5C)。此外,作者研究了ATG5和Beclin1对HCT116和SW480细胞增殖和存活的功能和作用。这些结果表明,在这两个细胞系中,ATG5或Beclin1上调均可挽救SP100-AS1下调导致的细胞增殖下降(图5D),这意味着SP100-AS1通过经典的宏观自噬途径调节自噬。
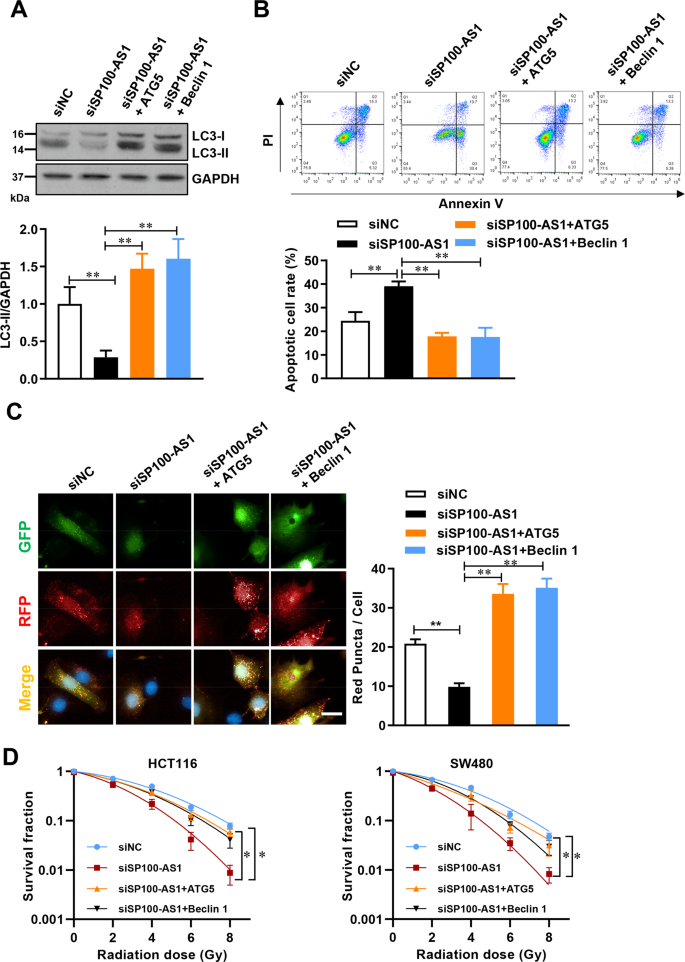
图5 ATG5和Beclin1过表达挽救了SP100-AS1对自噬的调节作用
6. SP100-AS1与ATG3相互作用并调节其蛋白稳定性
lncRNA可以与特定的蛋白质相互作用来发挥其功能。通过荧光原位杂交(FISH)检测SP100-AS1在HCT116和SW480细胞中的亚细胞定位,探讨SP100-AS1是否能通过这一机制发挥作用。令人惊讶的是,SP100-AS1在细胞质中表现出强烈的荧光,这表明该lncRNA可以与细胞质中的蛋白结合并进行相关功能,包括细胞增殖和辐射抗性(图6A, B, C)。接下来,作者进行了RNA下拉实验,以发现与SP100-AS1相互作用的蛋白。如图6D所示,银染法在分子量35 kDa处检测到多条条带(图6D)。质谱分析显示ATG3肽水平显著升高。进一步对SP100-AS1进行RIP实验,western blot结果显示SP100-AS1能与ATG3特异性结合(图6E)。另一方面,使用抗atg3抗体鉴定相关的结合RNA,结果显示,与对照IgG组相比,SP100-AS1在atg3结合的提取液中显著富集(图6F)。严格地说,对SP100-AS1下拉试验中提取的蛋白进行的蛋白质印迹分析证实,ATG3蛋白与SP100-AS1的义序列特异性结合,但与反义对照无特异性结合(图6G)。综上所述,作者发现ATG3是SP100-AS1在体内和体外的特异性结合蛋白。
在确定了SP100-AS1可以与ATG3相互作用之后,作者接下来试图研究SP100-AS1是否可以调节ATG3蛋白的稳定性或功能。首先,作者在HCT116细胞中检测敲低SP100-AS1后ATG3的蛋白水平。下调和过表达SP100-AS1分别可显著降低和升高ATG3蛋白水平(图6H)。蛋白质稳定性受多种途径和机制调控,尤其是泛素化依赖的蛋白酶体降解信号通路。与此一致的是,ATG3可以泛素化。因此,作者评估了SP100-AS1是否可以通过蛋白酶体途径影响ATG3蛋白的稳定性。在HCT116细胞中,转染Flag-tagged ATG3后,HA标记的泛素蛋白过表达,而内源性SP100-AS1 lncRNA被敲低。抗flag抗体免疫沉淀后,用抗HA抗体检测ATG3泛素化水平。作者发现,沉默SP100-AS1增加了ATG3的泛素化水平,表明SP100-AS1介导的ATG3降解参与了泛素化依赖性降解(图6I)。此外,作者还研究了ATG3在放线菌酮(cycloheximide, CHX)(一种成熟的蛋白质合成抑制剂)处理下的降解过程。重要的是,作者发现敲低SP100-AS1可以加速ATG3的降解(图6J)。在HCT116细胞中敲低或过表达SP100-AS1,然后用蛋白酶体抑制剂MG132处理。如图6K所示,敲低SP100-AS1引起的ATG3蛋白降解被挽救。此外,过表达SP100-AS1和MG132处理后,ATG3的表达显著增加。这些结果证实了SP100-AS1与ATG3相互作用并调节其蛋白稳定性。
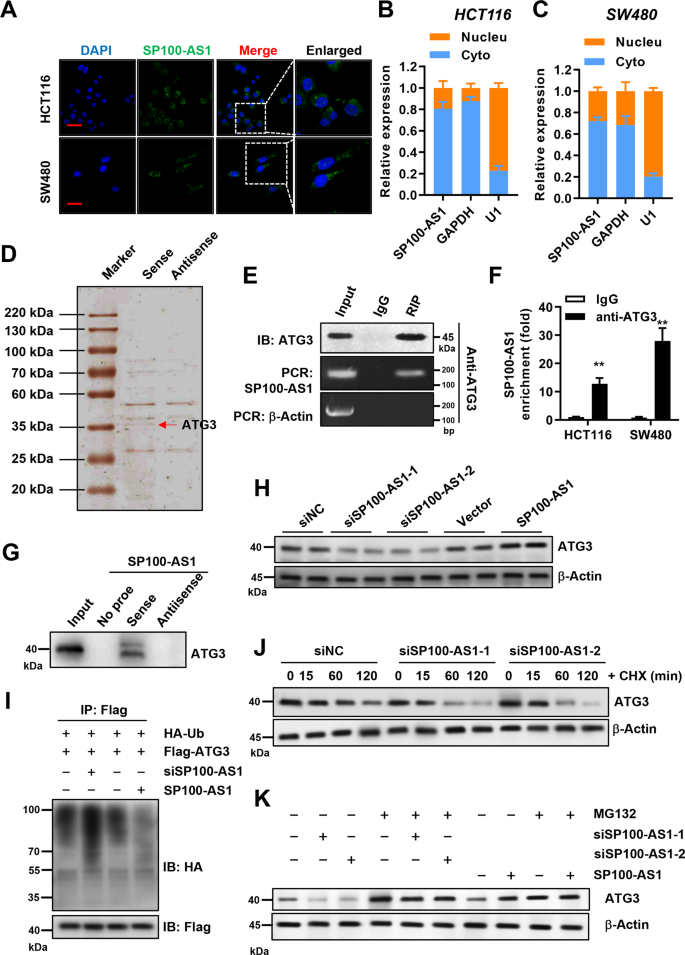
图6 SP100-AS1与ATG3相互作用并调节其蛋白稳定性。
7. SP100-AS1在结直肠癌中可作为miR-622的海绵
为了进一步研究SP100-AS1调控ATG3蛋白表达的机制,作者评估了SP100-AS1是否可以作为ATG3 mRNA的miRNA海绵。通过RIP实验确定AGO2是否与SP100-AS1相关,AGO2在miRNA通路中发挥多种作用,并通过产生pre-miRNA参与miRNA组装过程。有趣的是,在HCT116和SW480细胞系中均检测到AGO2和SP100-AS1之间存在显著的相互作用(图7A, B)。接下来,作者试图确定哪些miRNA可以直接与SP100-AS1结合。作者使用lncRNA探针筛选几个miRNA与SP100-AS1之间的相互作用。采用靶向SP100-AS1的特异性探针,通过pull-down实验纯化与SP100-AS1相关的miRNA。结果显示,SP100-AS1和miR-622的富集最为显著(图7C)。这些发现证实了miR-622和SP100-AS1在HCT116细胞中的相互作用。如图7D所示,SP100-AS1可以与miR-622显著结合。综上所述,这些发现表明SP100-AS1在CRC中扮演了miR-622海绵的角色。
生物信息学分析发现SP100-AS1的3'UTR区含有miR-622的靶向基序。构建荧光素酶实验系统检测miR-622对SP100-AS1 mRNA的调控作用(图7D)。萤火虫荧光素酶盒连接到野生型或突变的SP100-AS1 3'UTR区域。作者发现,突变的SP100-AS1 3'UTR不能与miR-622相互作用(图7E)。荧光素酶质粒转染HCT116细胞。过表达miR-622时,携带野生型区域的荧光素酶强度低于突变型(图7F)。相反,抑制miR-622 (miR-622-in)诱导荧光素酶活性显著增加,这一活性也被结合位点突变所抑制(图7G)。综上所述,作者证实了miR-622可以直接结合SP100-AS1并影响其在CRC细胞中的mRNA稳定性。

图7 SP100-AS1在结直肠癌中充当miR-622的海绵
8. miR-622靶向ATG3 mRNA调控自噬流
考虑到SP100-AS1海绵化miR-622并下调自噬流,作者试图研究miR-622是否影响自噬通路。在HCT116细胞中过表达miR-622或SP100-AS1。有趣的是,在SP100-AS1过表达的HCT116细胞中,异位表达miR-622可以恢复p62和LC3-11的表达(图8A, B)。因此,作者假设SP100-AS1可以作为miR-622的海绵,阻止其对ATG3 mRNA的影响,从而稳定ATG3,促进自噬流。采用计算机模拟方法分析ATG3的3'UTR区域以验证这一假设。出人意料的是,作者检测到了miR-622的一个靶向基序。接下来,作者进行了荧光素酶测定,将萤火虫荧光素酶盒插入野生型和突变的ATG3 3'UTR区域的前面(图8C)。如图8D所示,过表达miR-622可以降低野生型荧光素酶的表达,而共转染SP100-AS1可以挽救荧光素酶的活性。相反,共转染携带突变ATG3 3'UTR区域的质粒不能恢复荧光素酶的活性(图8D)。然后研究HCT116细胞中ATG3的内源性表达,结果显示miR-622在mRNA和蛋白水平显著降低ATG3的表达,而与SP100-AS1共表达可以恢复ATG3的表达。正如预期的那样,使用siRNA敲低SP100-AS1也可以降低ATG3 mRNA水平(图8E、F、G)。
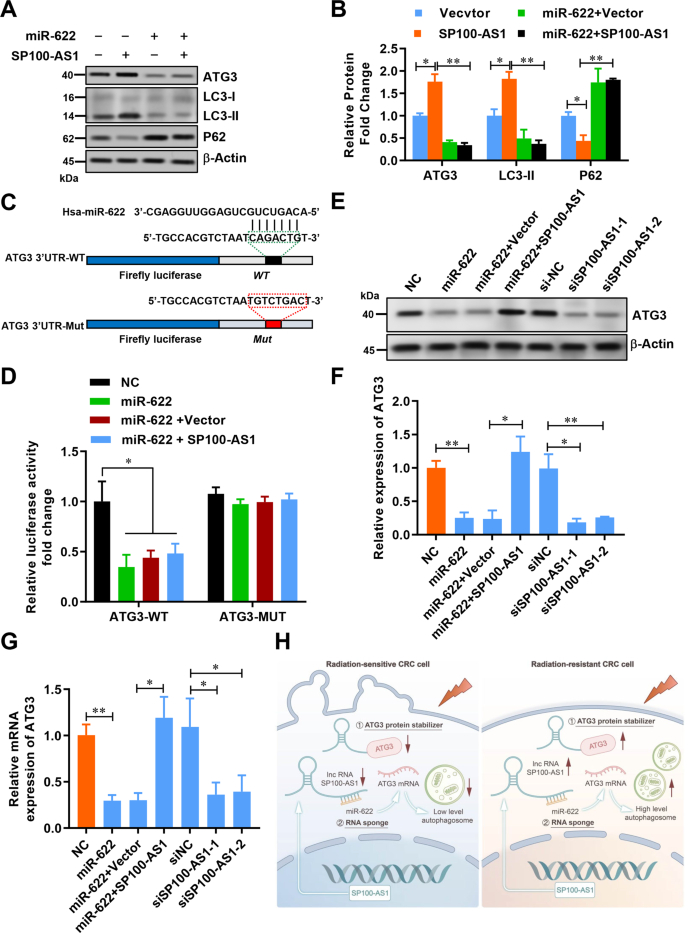
图8 SP100-AS1通过与miR-622相互作用调控ATG3表达
结论:
该研究表明SP100-AS1/miR-622/ATG3轴有助于CRC患者的放射抵抗和自噬活性,提示其作为改善CRC放射治疗反应的治疗靶点具有巨大的前景。
参考文献:
Zhou Y, Shao Y, Hu W, Zhang J, Shi Y, Kong X, Jiang J. A novel long noncoding RNA SP100-AS1 induces radioresistance of colorectal cancer via sponging miR-622 and stabilizing ATG3. Cell Death Differ. 2022 Aug 17. doi: 10.1038/s41418-022-01049-1. Epub ahead of print. PMID: 35978049.






