PHB2通过对抗PKM2剪接维持VSMCs的收缩表型
血管平滑肌细胞(VSMCs)的表型转变是多种血管疾病早期的发病机制。代谢重编程可能参与VSMC表型转变。然而,将能量代谢与不同VSMC表型联系起来的确切分子仍然难以捉摸。我们利用基因本体注释收集细胞能量调节基因,并对转化生长因子-β或血小板衍生生长因子BB刺激的VSMCs进行RNA-Seq分析。prohibitin2缺乏的VSMCs失去了可收缩的表型,这可以通过减少可收缩蛋白来证明。与Phb2flox/flox小鼠相比,Phb2SMCKO小鼠更容易损伤后VSMC增殖和新内膜形成。进一步的蛋白质相互作用组分析、免疫共沉淀和哺乳动物2-杂交实验显示,prohibitin 2通过其C端直接与丙酮酸激酶M1/2 (PKM) mRNA拼接的关键调节因子hnRNPA1相互作用,促进PKM2表达和糖酵解。Prohibitin2缺失促进PKM1/2 mRNA剪接和PKM1向PKM2的逆转,并增强VSMCs的糖酵解。阻断2-hnRNPA1相互作用导致PKM2表达增加,糖酵解增强,VSMCs中收缩标记基因表达抑制,以及体内损伤后新内膜形成加剧。总之,Prohibitin 2通过与hnRNPA1相互作用来抵消hnRNPA1介导的PKM选择性剪接和葡萄糖代谢重编程来维持VSMC的收缩表型。本文于2022年10月发表于Circulation Research (IF=23.213)。
技术路线:

结果:
(1) RNA序列分析预测新的将能量稳态与VSMCs收缩表型联系起来的候选基因
为了识别连接细胞能量代谢和VSMC表型的新候选基因,我们首先进行了RNA-seq分析,以揭示转化生长因子-β (TGF-β)处理增强收缩表型相关基因表达或血小板衍生生长因子BB (PDGF-BB)处理降低收缩表型相关基因表达的原发性大鼠VSMC的转录组变化。在这1893个基因中,有6个基因与细胞能量调节基因数据库重叠,包括prohibitin 2 (PHB2)、瞬时受体电位阳离子通道亚家族V成员4 (TRPV4)、ALK酪氨酸激酶受体(ALK)、组蛋白赖氨酸n-甲基转移酶PRDM16(PRDM16)、乙酰辅酶a羧化酶2 (ACACB)和载脂蛋白C-III (APOC3)(图1A)。接下来,我们验证了mRNA水平,发现原发性大鼠VSMCs中PHB2、TRPV4和ALK的表达确实受到TGF-β和PDGF-BB的相互调节(图1B)。接下来,我们使用靶向Phb2、Trpv4和Alk的特异性小干扰RNA (siRNAs)检测VSMC收缩标志物(ACT A2、CNN1和SM22α)的mRNA水平。如图1C所示,沉默Phb2、Trpv4和Alk可导致VSMC收缩标志物的表达显著降低,提示这3个基因可能是连接VSMC能量代谢与收缩表型的候选基因。在这3个基因中,有报道称prohibitin 2与prohibitin 1共同调控线粒体中的细胞色素-c氧化酶组装和线粒体呼吸。然而,prohibitin 2在VSMC身份和血管稳态中的确切作用仍然未知。另外的免疫荧光分析显示,prohibitin2主要定位于人动脉介质层(图1D)。因此,我们探讨了prohibitin 2是否调控VSMC表型。
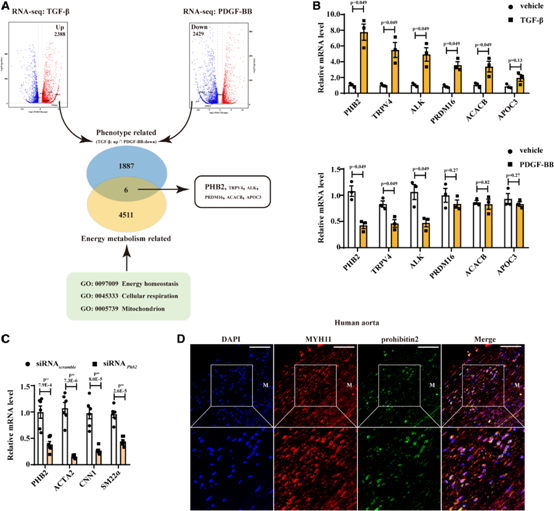
图1:RNA序列分析预测了连接血管平滑肌细胞(VSMC)能量稳态和收缩表型的新候选基因
(2) Prohibitin2减少与VSMCs转分化相关
进一步的Western blotting分析显示,在原发大鼠VSMCs中,PDGF-BB刺激后,prohibitin 2蛋白水平与VSMCs收缩标记物同时降低(图2A)。相反,TGF-β刺激的VSMCs表现出更高水平的prohibitin 2和收缩标志物(图2B)。血清饥饿是触发VSMC表型从去分化状态向分化状态转变的典型刺激。血清饥饿VSMCs中prohibitin 2水平升高(图2C)。RT-qPCR分析证实,在人类VSMCs中也观察到类似的改变(补充图未展示)。值得注意的是,在VSMCs表型转化过程中,prohibitin-1蛋白水平无统计学差异(图2A-2C)。同样,与假手术动脉相比,球囊损伤后3、7和14天,大鼠颈动脉中prohibitin 2的表达显著降低,同时VSMCs收缩标记物减少,内膜面积增加(图2D)。因此,western blotting分析、RT-qPCR和免疫荧光分析表明,与对照组乳腺内动脉相比,颈动脉内膜切除术患者动脉中prohibitin2的表达明显降低(图2E-2G)。
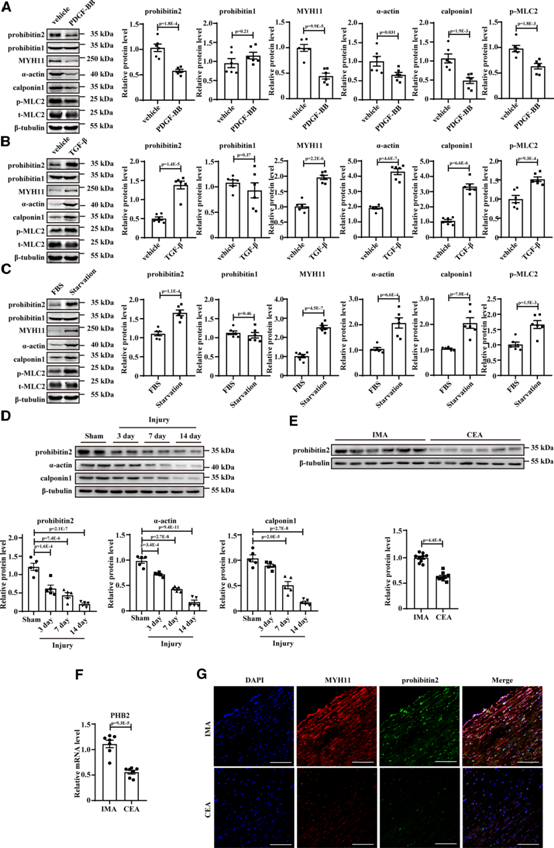
图2:Prohibitin 2减少与血管平滑肌细胞(VSMC)去分化相关
(3) Prohibitin 2在体外维持VSMCs的收缩表型
我们探讨了prohibitin2表达的干扰是否会影响VSMC表型切换。siRNA介导的人VSMCsprohibitin 2沉默可导致收缩标记物水平降低(补充图未展示)。因此,TGF-β促进VSMCs收缩蛋白表达的上调通过prohibitin 2沉默被取消(图3A)。为了进一步确定prohibitin 2在体内VSMC表型中的确切作用,将Phb2flox/flox小鼠与Tagln-Cre小鼠杂交,构建VSMC特异性Phb2缺失小鼠(Phb2SMCKO小鼠)(补充图未展示)。与Phb2flox/flox小鼠(WTVSMCs)相比,Phb2SMCKO小鼠的原发性VSMCs (Phb2 KO VSMCs)中的VSMCs收缩标记物的mRNA和蛋白质水平明显降低(图3B)。F-actin染色显示,prohibitin 2沉默导致原发大鼠VSMCs从细长收缩形态转变为多边形合成形态(图3C)。此外,经Phb2siRNA转染的VSMCs与经siRNA打乱转染的VSMCs相比,收缩能力降低,胶原凝胶收缩试验证明了这一点(siRNA打乱与siRNAPhb2: 46.3±3.86% vs 71.2±4.35%,P<0.05)(图3D)。从Phb2SMCKO小鼠中分离出的主动脉环对苯肾上腺素的反应表现出收缩力减弱(图3E)。在siRNAPhb2转染的VSMCs中,细胞迁移活性也增加了,划伤实验和Boyden室实验证明了这一点(图3F和3G)。相反,prohibitin 2过表达2可挽救PDGF-BB诱导的VSMC收缩标记物减少和VSMC迁移(补充图未展示)。综上所述,这些数据表明禁用2是维持VSMCs收缩表型的关键。
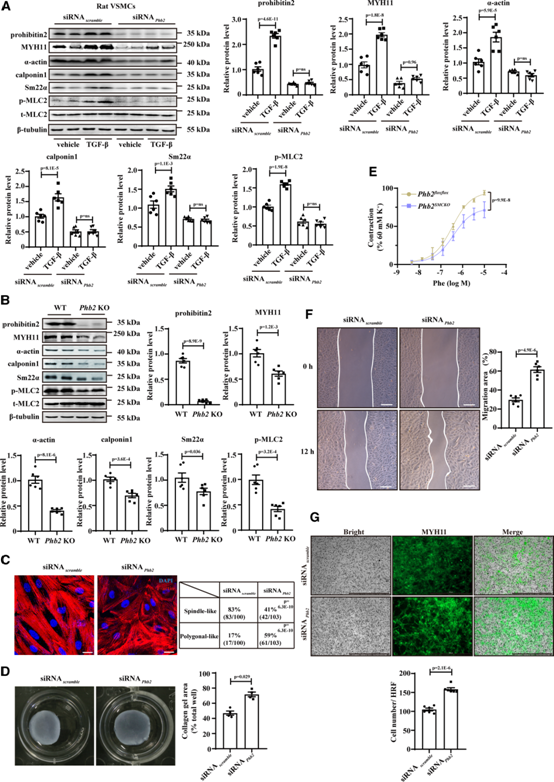
图3:Prohibitin 2在体外维持血管平滑肌细胞(VSMCs)的收缩表型
(4) VSMCs中Prohibitin 2的缺乏加剧体内损伤后新生内膜形成
对12周大的雄性Phb2SMCKO小鼠和Phb2flox/flox小鼠进行颈动脉钢丝损伤。颈动脉MYH11 (VSMC标记物)和CD31 (EC标记物)免疫染色显示,术后第0天,Phb2SMCKO小鼠和Phb2flox/flox小鼠的钢丝损伤程度相同(补充图未展示)。与Phb2flox/flox动脉相比,钢丝损伤后第3、5和7天,Phb2SMCKO动脉中VSMC收缩标记物的表达减少,尽管新内膜形成没有那么明显的诱导(图4A)。相反,损伤后14天,通过BrdU染色观察到Phb2SMCKO动脉细胞增殖活性增强(图4B)。结果,Phb2SMCKO小鼠的新内膜明显大于Phb2SMCKO小鼠(图4C)。此外,Phb2SMCKO动脉新内膜与中膜的比例远高于Phb2flox/flox动脉,而中膜面积和外弹性层周长在两组间无统计学差异。此外,为了排除taglncre介导的Phb2敲除可能引起的胚胎发育影响,我们将Phb2floxflox小鼠与Myh11-CreERT2小鼠杂交(补充图未展示)。然后,8周龄雄性Phb2flox/flox小鼠和Phb2flox/floxMyh11-CreERT2小鼠用他莫西芬诱导出生后VSMCs的抑制性2耗尽。两组小鼠(Phb2flox/flox+他莫西芬和Phb2flox/floxMyh11-CreERT+他莫西芬)颈动脉钢丝损伤。与他莫昔芬处理的Phb2flox/floxMyh11-CreERT2小鼠相比,他莫昔芬处理的Phb2flox/flox/flox小鼠线损伤诱导的新内膜形成显著增加(图4D)。因此,prohibitin 2在体内维持VSMCs的收缩表型。

图4:体内血管平滑肌细胞(VSMCs)的Prohibitin 2缺乏加剧损伤后新内膜的形成
(5) HnRNPA1是一种新的Prohibitin2结合蛋白
我们使用原发大鼠VSMCs来探索连接prohibitin 2和VSMCs表型调制的潜在结合伙伴。3个蛋白条带被抗prohibitin 2抗体特异性免疫沉淀,而不是对照IgG。14个被抗prohibitin 2抗体免疫沉淀而非对照IgG免疫沉淀的蛋白被鉴定为潜在的prohibitin 2结合伙伴,包括prohibitin1 (PHB1)、异质核核糖核蛋白A1 (hnRNPA1)、颗粒蛋白(GRN)、PRMT1蛋白染色质靶蛋白(CHTOP)、14-3-3蛋白zeta (YWHAZ)、srsf1、膜联蛋白A2 (ANXA2)等(图5A)。我们首先分析了prohibitin2缺乏是否会导致hnRNPA1表达的改变。在钢丝损伤小鼠颈动脉中,hnRNPA1的表达减少。因此prohibitin 2对hnRNPA1的表达没有调控作用。接下来我们评估了prohibitin 2和hnRNPA1的潜在相互作用。在原代大鼠VSMCs的细胞裂解液中,内源性prohibitin 2与抗hnRNPA1抗体共免疫沉淀,但不与对照IgG共免疫沉淀,反之亦然(图5B)。进一步的共免疫沉淀分析显示,prohibitin 2与抗hnRNPA1抗体共免疫沉淀,但与对照IgG未在原代大鼠VSMCs的核部分共免疫沉淀,但在细胞质部分不共免疫沉淀,这表明prohibitin 2-hnRNPA1相互作用发生在细胞核(图5C)。hnRNPA1和prohibitin2一致地共定位于原发性大鼠VSMCs的细胞核(图5D)。HEK293A细胞分别转染hnRNPA1 FL/ΔM9/ΔRGGbox-M9质粒旁的pcDNA3.1-6×his-prohibitin 2质粒和flag-CMV质粒(图5E),然后使用抗flag抗体进行共免疫沉淀分析。hnRNPA1 FL和hnRNPA1ΔM9突变体均通过标志抗体特异性免疫沉淀出prohibitin 2,而不是对照IgG(图5F)。hnRNPA1的RGG-box结构域与prohibitin 2结合(图5G)。接下来,我们亚克隆了prohibitin 2的不同结构域(图5H)。Flag-hnRNPA1通过抗flag抗体特异性免疫沉淀prohibitin 2的C端,但不通过对照IgG,反之亦然(图5I)。通过哺乳动物2-杂交实验验证了prohibitin 2与hnRNPA1的C端相互作用(图5J)。总之,通过其C端,prohibitin 2直接与hnRNPA1的RGG-box结构域相互作用。

图5:异质核核糖核蛋白A1 (HnRNPA1)是一种新型的prohibitin 2结合蛋白
(6) HnRNPA1-Prohibitin 2相互作用对维持VSMC体内外收缩表型至关重要
我们研究核内prohibitin 2和hnRNPA1的相互作用是否对VSMC的收缩表型至关重要。将带有C端M9结构域的hnRNPA1的RGG-box结构域亚克隆到腺病毒pAdT机架-CMV载体中,重组腺病毒(Ad-Flag-RGG-M9)用于阻断hnRNPA1和prohibitin2的核相互作用。免疫共沉淀实验显示,Ad-Flag-RGG-M9感染显著阻断了原发大鼠VSMCs中prohibitin 2-hnRNPA1相互作用(图6A)。Ad-FlagRGG-M9感染抑制了α-actin和SM22α的转录活性,从而导致VSMCs去分化和细胞迁移增加(图6B-6E)。Ad-Flag-RGG-M9感染加剧了球囊损伤后第7天VSMC收缩标记物的减少和新内膜形成的诱导(图6F)。Ad-Flag-RGG-M9感染加重了大鼠球囊损伤模型28天新生内膜的形成(图6G),而不会导致体重或血压等显著变化。免疫染色实验证明,与假手术Ad-GFP感染大鼠颈动脉相比,球囊损伤Ad-GFP感染大鼠颈动脉VSMCs中prohibitin 2水平显著降低(补充图未展示)。在Ad-Flag-RGG-M9感染的大鼠颈动脉中,与Ad-GFP感染的大鼠颈动脉相比,prohibitin 2的水平没有改变,这表明prohibitin 2-hnRNPA1相互作用不可能调控prohibitin 2的表达(补充图未展示)。综上所述,这些数据揭示了prohibitin 2-hnRNPA1相互作用对VSMC收缩表型维持的重要作用。

图6:HnRNPA1-prohibitin 2相互作用对于维持血管平滑肌细胞(VSMCs)在体内外的收缩表型至关重要
(7) Prohibitin 2抑制hnRNPA1介导的pre-PKM mRNA剪接、PKM2表达和有氧糖酵解
hnRNPA1是pre-PKM mRNA剪接的主调控因子。PKM2是PKM的首选剪接异构体,调节糖酵解的最终限速步骤,而PKM1促进OXPHOS。这两种异构体来自于PKM前mRNA的互排性选择性剪接,反映了外显子9 (PKM1)或外显子10 (PKM2)的包含。hnRNPA1抑制外显子9的序列侧翼,导致外显子10的包含和PKM2的表达。我们研究prohibitin 2是否影响hnRNPA1介导的pre-PKM mRNA剪接、PKM2的产生和有氧糖酵解。与Phb2flox/flox小鼠(WTVSMCs)相比,从Phb2SMCKO小鼠分离的原发性小鼠VSMCs (Phb2 KO VSMCs)中PKM2的mRNA水平升高,而PKM1的mRNA水平下降(补充图未展示)。相比之下,pre-PKM mRNA水平没有显著改变,表明存在另一种剪接。PstI和NcoI酶切扩增子后进一步RTPCR显示Phb2缺失促进PKM1向PKM2的反式表达(图7A)。在Phb2 KO原发小鼠VSMCs(图7B)、Ad-Flag-RGG-M9感染的大鼠VSMCs(图7C)以及感染Ad-Flag-RGG-M9的球囊损伤大鼠颈动脉中使用western blotting也观察到了类似的结果。Phb2 KO VSMCs糖酵解活性增强,OXPHOS活性降低,细胞糖酵解和有丝分裂应激试验证明(图7D)。PDGF-BB刺激的原发大鼠VSMCs中prohibitin 2被抑制的转分化通过PKM2过表达被取消(图7E)。为了进一步阐明prohibitin2是否在体内通过抑制PKM2的表达来维持VSMC的收缩表型和对抗新生内膜的形成,我们使用带有SM22α启动子的AAV9载体选择性下调VSMC中的PKM2。在Phb2SMCKO小鼠颈动脉钢丝损伤后第7天,VSMC特异性PKM2耗损挽救了VSMC收缩标记物的减少(补充图未展示)。Phb2SMCKO小鼠钢丝损伤后血管收缩力下降和新生内膜形成增强均因VSMC特异性PKM2耗损而得到挽救(图7F-7G)。综上所述,prohibitin2与核hnRNPA1直接相互作用,抑制hnRNPA1介导的pre-PKM mRNA剪接和PKM2的产生,从而调节葡萄糖代谢重编程,在体外和体内维持VSMCs的收缩表型。

图7:Prohibitin2抑制hnRNPA1介导的pre-PKM mRNA剪接、丙酮酸激酶异构体M2 (PKM2)表达和葡萄糖代谢重编程
结论:
Prohibitin2通过直接与核hnRNPA1相互作用,抑制hnRNPA1介导的pre-PKM mRNA剪接、PKM2的产生,从而调节葡萄糖代谢重编程(图8),维持VSMCs的收缩表型,抑制损伤后新内膜的形成。Prohibitin2是维持VSMCs稳态的内源性糖酵解调节剂。以prohibitin2-hnRNPA1-PKM2轴为靶点调节VSMC能量代谢可能有助于心血管疾病的治疗。
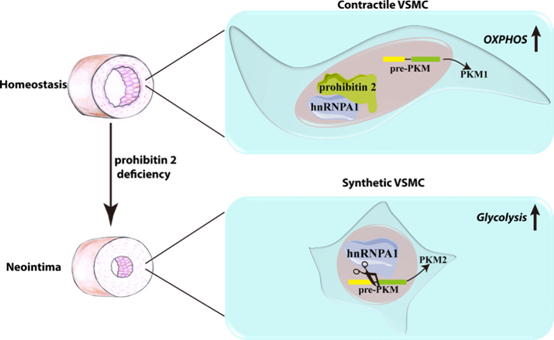
图8:Prohibitin2在血管平滑肌细胞(VSMC)表型测定的示意图
参考文献:
Jia, Y., Mao, C., Ma, Z., Huang, J., Li, W., Ma, X., Zhang, S., Li, M., Yu, F., Sun, Y., Chen, J., Feng, J., Zhou, Y., Xu, Q., Zhao, L., Fu, Y., & Kong, W. (2022). PHB2 Maintains the Contractile Phenotype of VSMCs by Counteracting PKM2 Splicing. Circulation research, 131(10), 807–824. https://doi.org/10.1161/CIRCRESAHA.122.321005.






