脑类器官研究专题之脑类器官构建
人脑是一个高度组织的结构,由各种细胞类型组成,包括神经元、神经胶质细胞和血管细胞。模拟人类大脑发育具有挑战性,因为它需要对不同的生化和物理事件进行协调调节。类器官(Organoids)是一种基于3D体外细胞培养系统建立的与体内组织或器官高度相似的一种模型,能最大程度模拟人体器官,是促进个体疾病研究和个性化治疗的强大系统。人脑类器官是干细胞衍生的三维培养物,概括了人脑的细胞和结构特征,使其成为移植疗法的有希望的来源。人类大脑类器官可以表现出渐进的神经元成熟和功能,以及强大的宿主介导的血管形成。这些发现为使用脑类器官移植治疗神经系统疾病的前景提供了光明。
今天我们讲的是脑类器官构建的构建方法,该结果刊登在International Journal of Molecular Sciences。该文章主要讲述的是3中脑类器官构建方法对于类器官模型的影响,是一篇片十分基础的研究。

在文章中作者使用了三种方法构建脑类器官:(1)衍生于Lancaster, Madeline A et al. “Cerebral organoids model human brain development and microcephaly.” Nature vol. 501,7467 (2013): 373-9.的方法,这一类器官命名为PC1;(2)衍生于Lancaster, Madeline A et al. “Cerebral organoids model human brain development and microcephaly.” Nature vol. 501,7467 (2013): 373-9.的方法,这一类器官命名为PC2,该方法应用SMAD、GSK3、TGFβ抑制剂和WNT激活剂;(3)衍生于Paşca, Anca M et al. “Functional cortical neurons and astrocytes from human pluripotent stem cells in 3D culture.” Nature methods vol. 12,7 (2015): 671-8.的方法,这一类器官命名为PC3,该方法应用SMAD抑制剂和EGF和FGF处理。
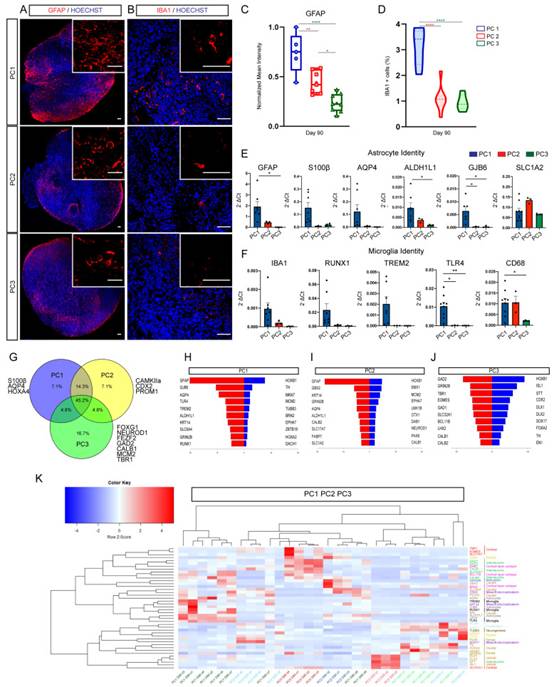
免疫荧光检测和qRT-PCR检测发现,这三个方案产生的类器官具有神经元祖细胞和喙神经识别标记物以及神经元基因的整体表达,表明在所有条件下都有有效的神经外胚层获取和神经发生,正如预期的那样。
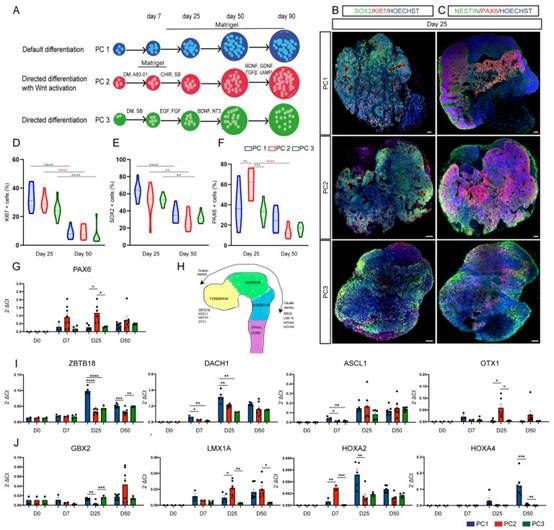
所有皮质类器官模型都模拟发育中的胚胎皮层的体内细胞极性和整体细胞结构,其中PC1类器官在长期基质胶嵌入和默认非定向条件后在体外显示出最保守的细胞极性。如前所述,方案之间的这些差异可能表明Matrigel对神经上皮和细胞极性的生长有影响和/或神经诱导形态生成对神经上皮生长和细胞极性的影响。
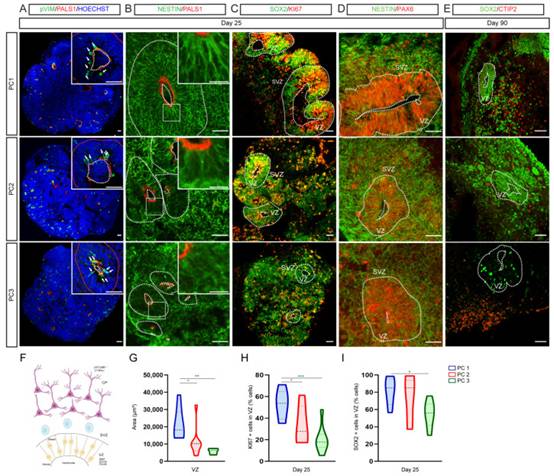
在第50天和第90天观察到神经元标志物的广泛表达,来自所有方案的类器官中NEUN+和MAP2+神经元的数量随时间增加。参与神经元成熟的基因和参与突触建立的基因的表达水平同样以时间依赖性方式上调。这些结果表明,脑类器官显示出时间依赖性成熟,神经元功能所必需的基因(如AMPA和NMDA受体的亚基以及突触后密度蛋白)的表达增加
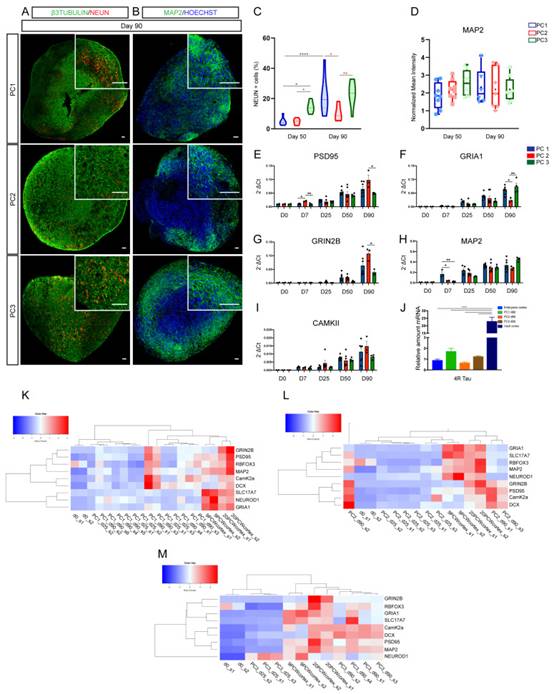
发现PC1衍生类器官中TBR3+深层皮质神经元的比例更高,PC2和PC2衍生类器官中CTIP1+(深层)和SATB3+(上层)神经元的比例更高。此外, PC3衍生的类器官在第1天显示出更高水平的谷氨酸能标志物VGLUT1和更高的VGLUT90点密度,表明谷氨酸能同一性更高。还在PC3类器官中检测到更高百分比的GAD67+抑制神经元。Biomark分析确认了这些结果。端脑、皮质和谷氨酸能特异性标志物(如 FOXG1、EMX1、TBR2、NEUROD1、TBR1 和 VGLUT1)在3个月(第90天)在 PC3 来源的类器官中表达更多。这些数据表明,在没有WNT激活的情况下,引导分化显示出皮层、谷氨酸能和GABA能抑制性神经元祖细胞的最高富集,这表明在双重SMAD抑制和没有WNT活化等尾状化因子的情况下具有更高的头侧皮层同一性