ZNF460介导的circRPPH1促进TNBC进展
环状RNA是高度稳定的调控RNA,与肿瘤发生和进展的关系日益密切。然而,许多环状RNA在三阴性乳腺癌(TNBC)中的作用及其相关机制尚未阐明。TNBC中circRPPH1的上调与不良预后呈正相关。此外,在体内和体外,circRPPH1都促进了TNBC细胞的生物学恶性行为。此外,circRPPH1可能作为miR-326的分子海绵,控制ITGA5的表达,激活FAK/PI3K/AKT通路。我们的研究表明,ZNF460可以促进circRPPH1的表达,circRPPH1/miR326/ITGA5轴可以激活FAK/PI3K/AKT通路,促进TNBC的进展。因此,circRPPH1可作为TNBC的治疗或诊断靶点。本文于2024年2月发表于“Molecular Cancer”(IF=37.3)上。
技术路线

结果:
1)circRPPH1的鉴定及临床特征
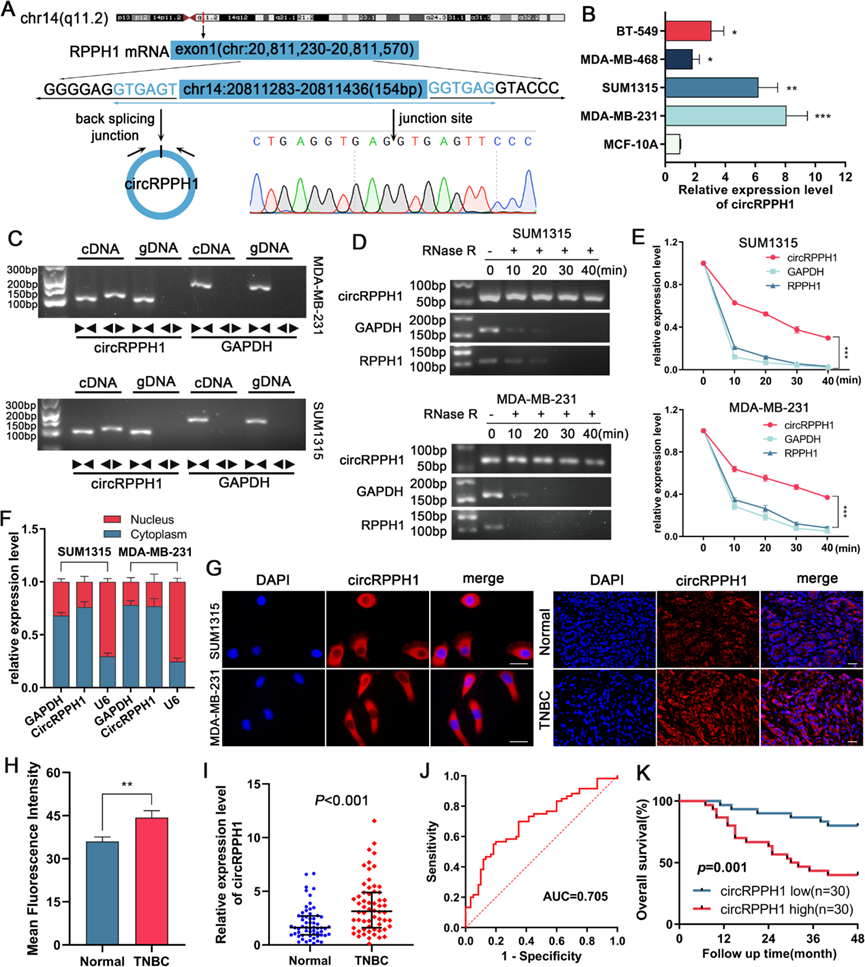
我们通过检查来自GSE101123数据集的TNBC组织和正常乳腺组织的RNA测序阵列,筛选出了20个表达变化最显著的circRNAs。在鉴定的circRNAs中,hsa_circRNA_000166与TNBC之间的关系尚不清楚。本文将重点研究其在TNBC中的生物学活性及其相关机制。Hsa_circRNA_000166(本研究中简称circRPPH1)是由RPPH1基因编码的mRNA通过反向剪接产生的,Sanger测序证实了其反向剪接位点的存在(图1A)。然后,我们通过qRT-PCR验证,与MCF10A细胞相比,SUM1315和MDA-MB-231细胞中的circRPPH1表达明显上调(图1B)。为了验证circRPPH1是一个环状的头尾连接,我们从TNBC细胞中提取cDNA和gDNA,然后使用收敛引物和发散引物进行PCR扩增。结果表明,circRPPH1可以利用发散引物从cDNA扩增。这表明circRPPH1是一个环状结构,是由头尾连接的转录后剪切产生的(图1C)。RNase R分析表明,circRPPH1比亲本基因和GAPDH表现出更高的降解抗性。这表明circRPPH1是一种比线性RNA更稳定的环状RNA(图1D和E)。核细胞质分离和FISH检测显示circRPPH1主要存在于细胞质中,平均荧光强度显示TNBC组织比正常乳腺组织表达更多的circRPPH1(图1F-H)。为了探索circRPPH1的应用价值,我们检测到TNBC组织中circRPPH1的表达增加(图1I)。ROC曲线显示,特异性为0.8,敏感性为0.567,曲线下面积为0.705(图1J)。我们随后根据TNBC患者随访数据绘制了Kaplan-Meier生存曲线,结果显示circRPPH1高表达患者的总生存期比circRPPH1低表达患者短(图1K)。根据这些发现,circRPPH1可以用于诊断和预后。
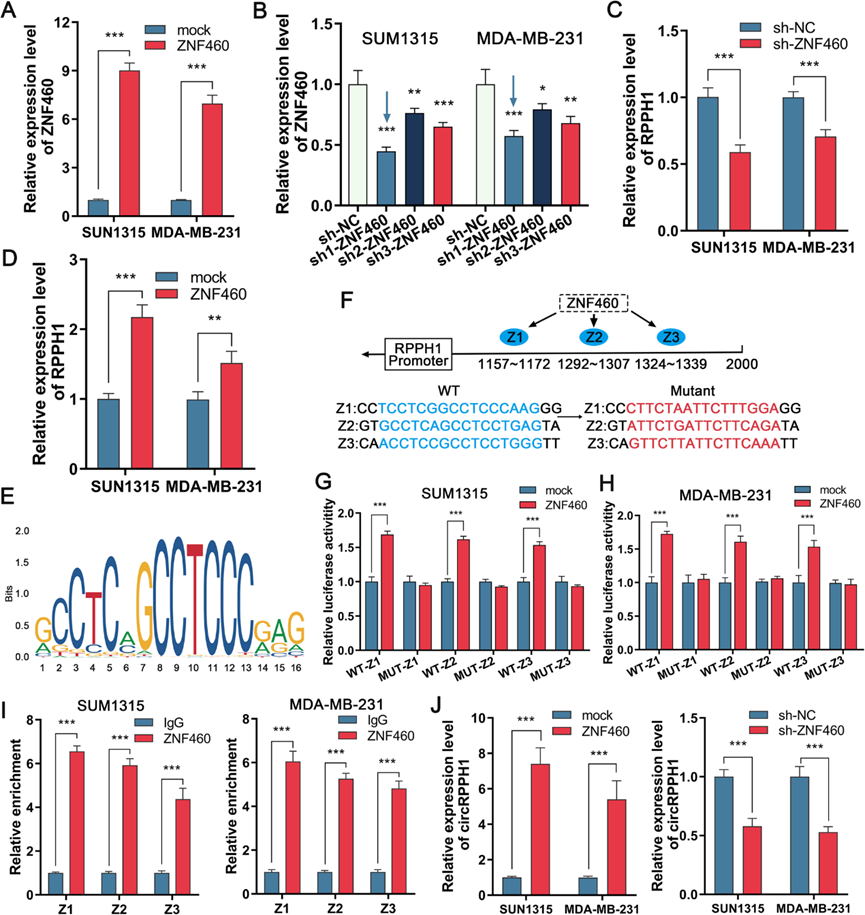
2)ZNF460增加了RPPH1和circRPPH1的表达
为了探究是否存在影响RPPH1和circRPPH1表达的转录因子,我们通过NCBI查找了RPPH1启动子可能的序列,发现了3个转录因子ZNF460与RPPH1启动子的结合位点。我们假设ZNF460可能影响RPPH1表达的转录调控。为了进一步研究ZNF460的作用,我们设计了ZNF460过表达载体(pcDNA3.1-ZNF460)、敲低载体(sh1-ZNF460、sh2-ZNF460、sh3-ZNF460)和相应的阴性对照载体,并通过qRT-PCR验证了它们的有效表达(图2A和B)。转染sh1-ZNF460后,RPPH1在TNBC细胞中的表达显著降低。但转染过表达载体pcDNA3.1-ZNF460后,RPPH1在TNBC细胞中的表达显著升高(图2C和D)。根据ZNF460与RPPH1启动子的结合序列,我们构建了带有野生型或突变型RPPH1启动子序列的荧光素酶报告质粒(图2E和F)。研究结果显示,ZNF460增强了野生型RPPH1启动子质粒的荧光素酶活性,而突变型质粒则保持不变(图2G和H)。ChIP-qPCR实验显示,与阴性对照IgG相比,ZNF460与RPPH1启动子结合(图2I)。最后,我们通过RT-qPCR验证,转染pcDNA3.1-ZNF460后,TNBC细胞内circRPPH1表达升高,而转染sh1-ZNF460后,circRPPH1表达降低(图2J)。根据上述发现,ZNF460可能附着在RPPH1启动子区域,从而调控其和circRPPH1的表达。
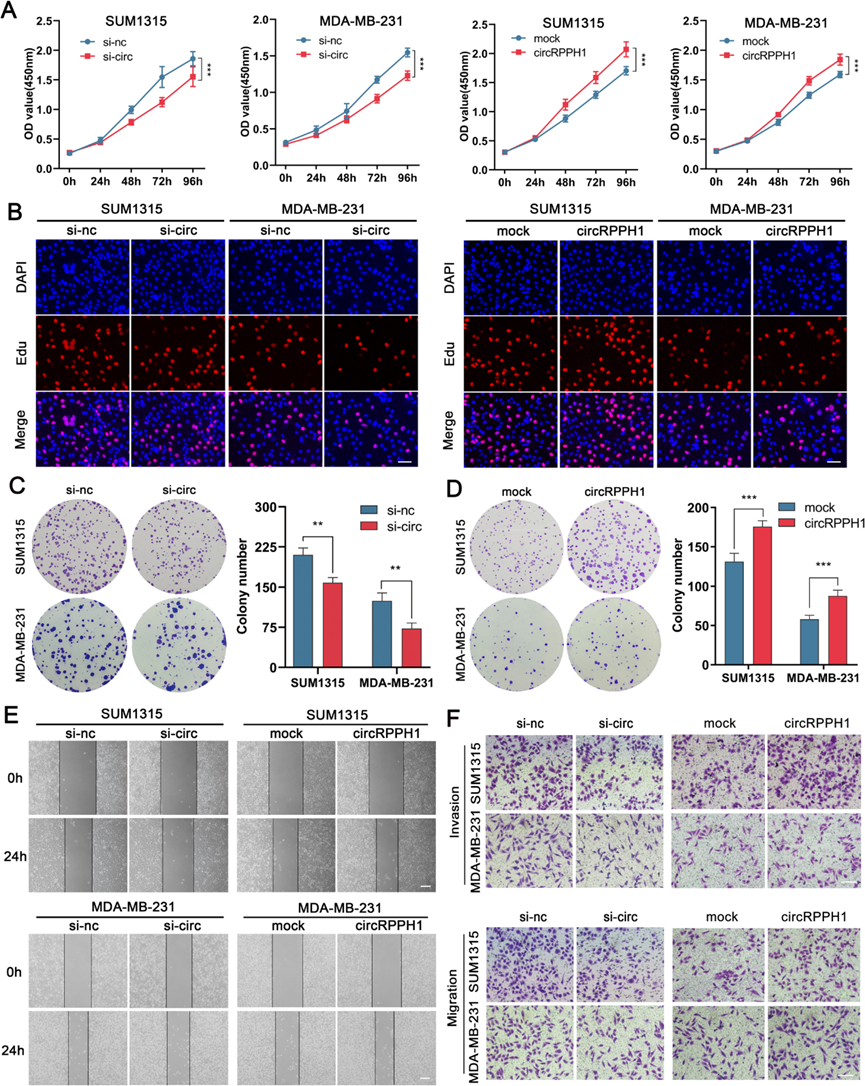
3)CircRPPH1促进TNBC细胞生长、迁移和侵袭
我们通过集落形成实验、EdU和CCK-8实验验证了circRPPH1的敲低抑制了TNBC细胞的增殖,而circRPPH1的过表达促进了细胞增殖(图3A-D)。此外,Transwell和伤口愈合实验表明,干扰circRPPH1可降低TNBC细胞的迁移和侵袭能力,而过表达circRPPH1则相反(图3E和F)。根据上述发现,circRPPH1在TNBC细胞中发挥了促癌作用。
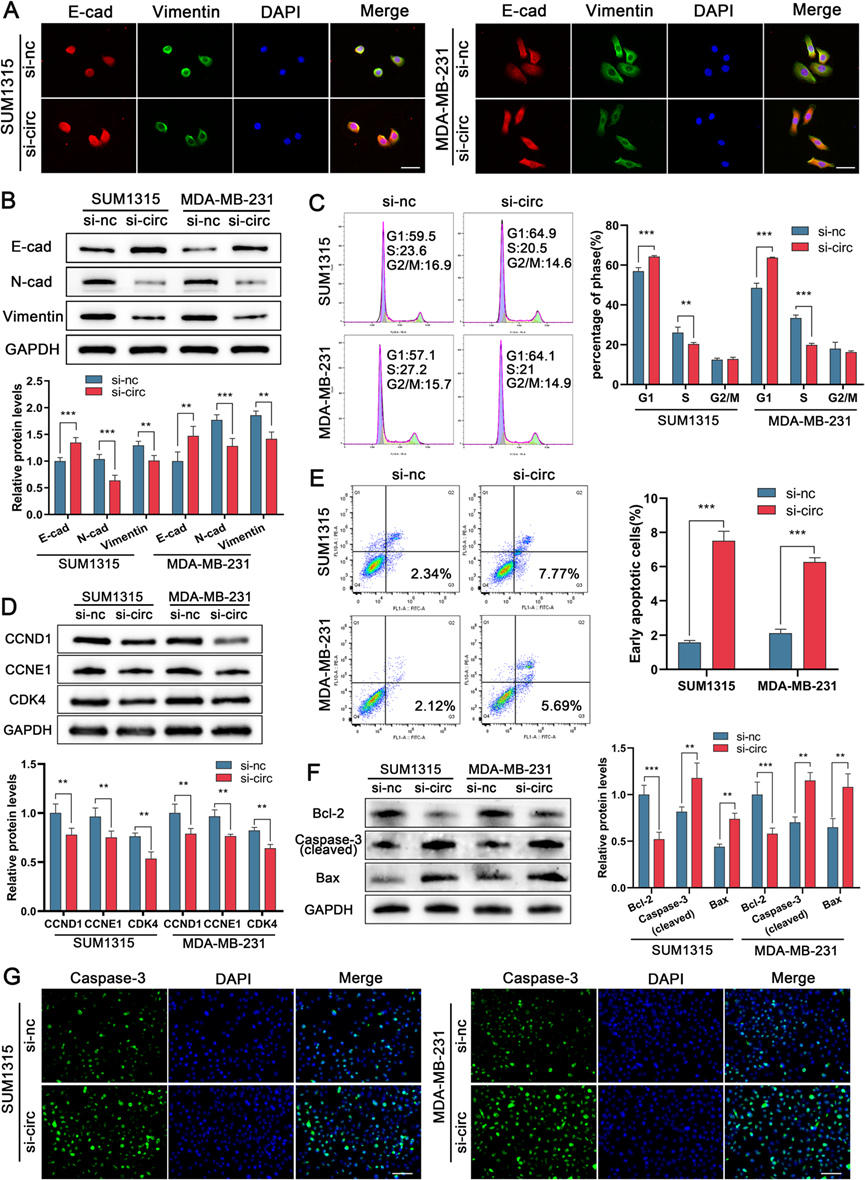
4)CircRPPH1促进TNBC细胞EMT,调节细胞周期,抑制细胞凋亡
考虑到EMT机制也有助于肿瘤细胞转移,我们利用免疫荧光法来确定相关蛋白的水平。我们的研究结果显示,沉默circRPPH1后,TNBC细胞中E-cadherin表达增加,而N-cadherin和vimentin表达减少(图4A)。Western blot实验结果与IF实验结果一致(图4B)。接下来,我们使用流式细胞术检测细胞周期,我们的数据显示,沉默circRPPH1后,TNBC细胞处于G1期的比例增加,处于S期的比例减少(图4C)。我们还通过Western blot检测到沉默circRPPH1后细胞周期相关蛋白的表达减少(图4D)。这表明沉默circRPPH1后细胞周期被阻断。之后,我们进行Annexin V/PI染色流式细胞术研究,发现敲低circRPPH1显著提高了细胞的早期凋亡率(图4E)。同样,我们使用Western blot发现,敲低circRPPH1后,Bcl-2表达降低,而cleaved caspase-3和Bax表达升高(图4F)。此外,免疫荧光实验显示,敲低circRPPH1后caspase-3表达增加(图4G)。综上所述,circRPPH1在TNBC细胞中具有促进EMT、加速细胞周期、抑制细胞凋亡的生物学功能。
5)CircRPPH1通过直接结合miR-326起到分子海绵的作用
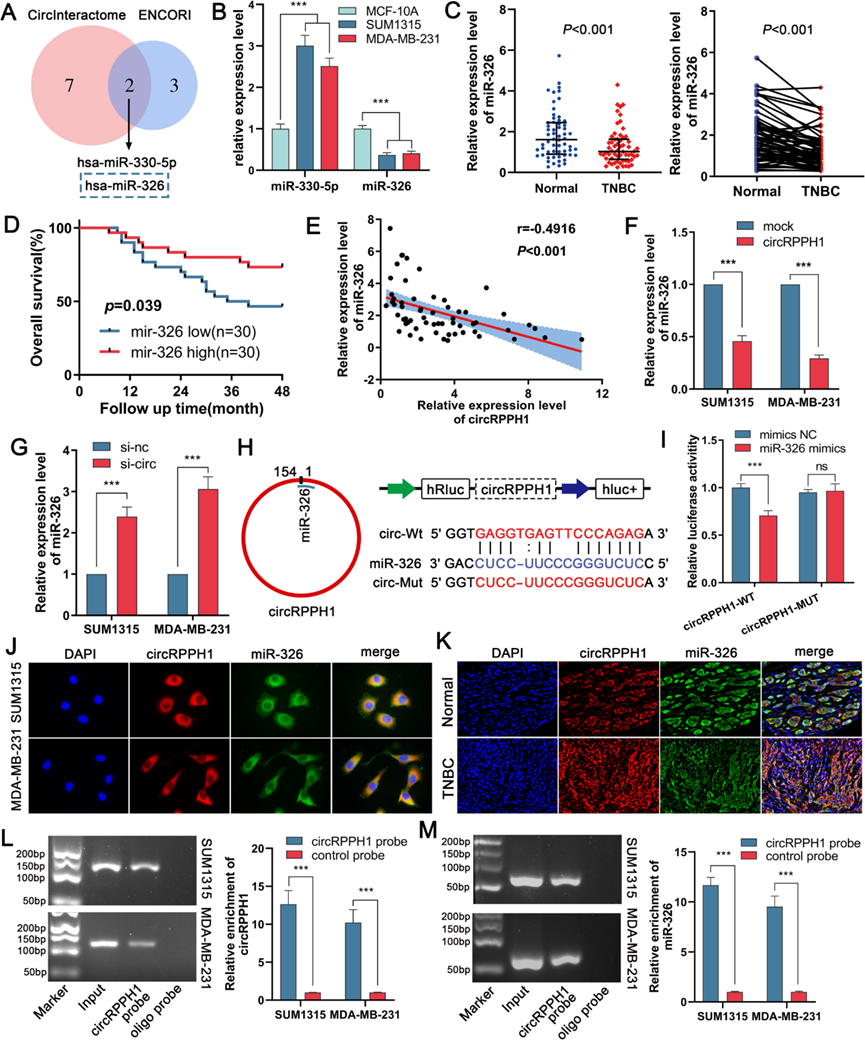
为了进一步了解circRPPH1在TNBC中的功能,我们使用ENCORI数据库和CircInteractome数据库预测hsa-miR-330-5p和hsa-miR-326可能与circRPPH1相互作用(图5A)。我们检测到TNBC细胞中miR-326和miR-330-5p表达下调和上调(图5B)。同样,miR-326在TNBC组织中的表达明显降低(图5C)。根据Kaplan-Meier生存分析(图5D),miR-326表达较高的患者总生存时间也更长。通过Pearson相关分析,我们发现TNBC组织中circRPPH1的表达水平与hsa-miR-326呈负相关(图5E)。因此,我们预测circRPPH1可以在TNBC中与miR-326结合,从而发挥分子海绵的作用。我们验证了circRPPH1敲低或过表达对miR-326表达的影响。结果表明,circRPPH1过表达会降低miR-326的表达,而circRPPH1敲低则会产生相反的效果(图5F和G)。根据ENCORI数据库的circMIR软件,我们根据circRPPH1与miR-326结合得分最高的区域,创建了具有野生型和突变型circRPPH1序列的双荧光素酶报告质粒。miR-326模拟物降低野生型质粒的荧光素酶活性(图5H和图I)。根据FISH检测(图5J和K),CircRPPH1和miR-326主要存在于细胞质中。此外,我们使用生物素标记的circRPPH1探针在TNBC细胞中进行了RNA pull-down实验,结果显示生物素标记的circRPPH1探针组中circRPPH1和miR-326的富集量大幅增加(图5L和M)。综上所述,circRPPH1可能起到分子海绵的作用,直接与miR-326结合。
6)MiR-326部分逆转了circRPPH1的促肿瘤作用
为了进一步了解miR-326和circRPPH1如何相互作用,我们使用miR-326模拟物或抑制物与si-circ或过表达载体circRPPH1进行了拯救实验。集落形成、EdU和CCK-8检测表明,miR-326模拟物阻断了circRPPH1过表达对TNBC细胞生长的影响,而miR-326抑制剂恢复了circRPPH1敲低对TNBC细胞增殖的影响(图6A-E)。此外,关于miR-326对TNBC细胞侵袭和迁移的影响,我们发现miR-326模拟物可以抑制过表达circRPPH1对其的促进作用,而miR326抑制剂可以部分逆转敲低circRPPH1对其的抑制作用(图6F-I)。上述实验表明,miR-326作为一种致癌因子,可以抵消circRPPH1的促癌活性。

7)CircRPPH1通过miR-326/ITGA5轴刺激FAK/PI3K/AKT通路
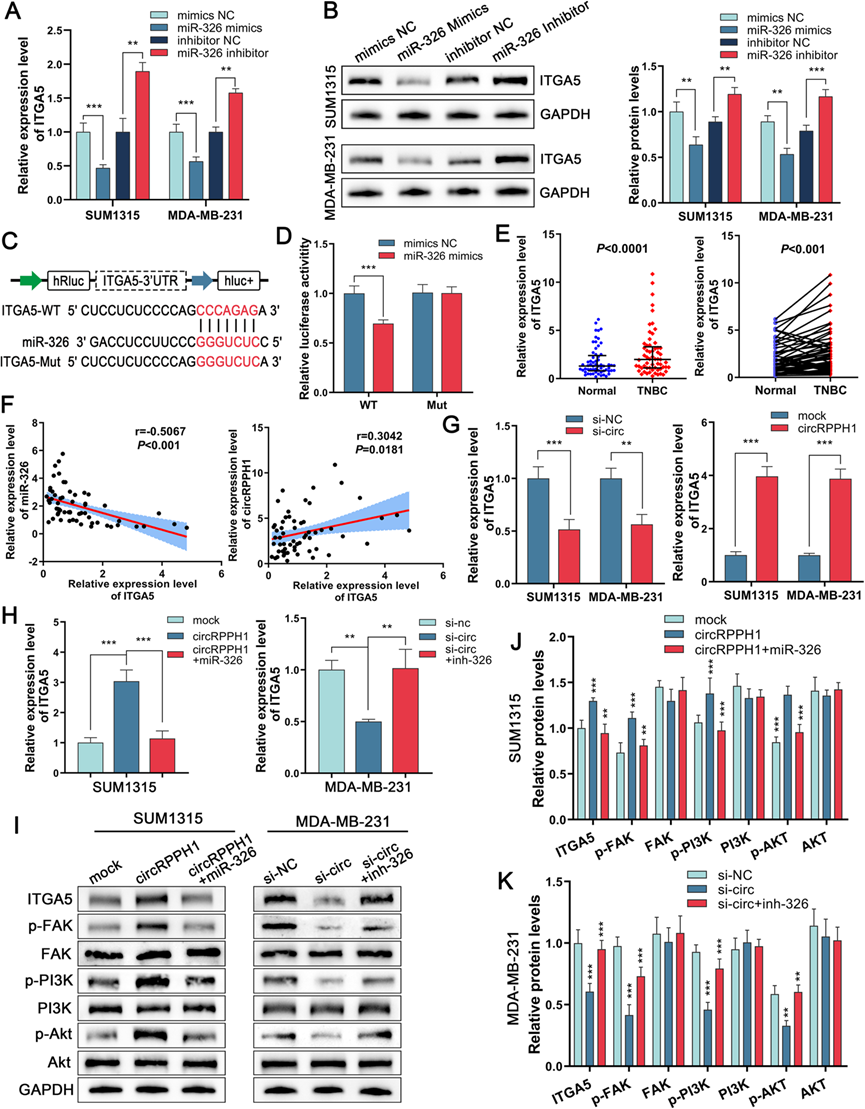
为了完善circRPPH1/miR-326轴并探索其下游调控机制,我们利用miRTarBase数据库、miRBD数据库和TargetScan数据库预测ITGA5可能是miR-326的下游基因。通过Western blot和qRT-PCR,我们能够证明miR-326模拟转染SUM1315细胞和MDA-MB-231细胞可降低ITGA5的表达而当使用miR-326抑制剂时,ITGA5的表达增加(图7A和B)。为了证实ITGA5和miR-326之间的相互作用,我们创建了具有野生型和突变型ITGA5 3 ' UTR的双荧光素酶报告质粒。根据研究结果,转染miR326模拟物显著降低了野生型质粒的荧光素酶活性,但对突变型质粒没有显著影响(图7C和D)。我们随后证实ITGA5在TNBC组织中上调(图7E)。Pearson相关研究显示circRPPH1与ITGA5呈正相关,但miR-326与ITGA5表达水平呈负相关(图7F)。然后,我们在敲低或过表达circRPPH1后检测ITGA5的表达。研究结果表明,circRPPH1过表达可改善ITGA5的表达,而敲低后结果则相反(图7G)。随后,我们通过拯救实验发现,miR-326模拟物或抑制剂可以撤销circRPPH1过表达或敲低导致的ITGA5表达的改变(图7H)。根据KEGG通路分析,ITGA5是PI3K/AKT通路的相关基因。因此,我们分析了TNBC细胞中circRPPH1上调或下调后ITGA5及其下游基因的表达情况。在TNBC细胞系中,我们发现过表达circRPPH1可显著增加ITGA5、p-FAK、p-PI3K和p-AKT的表达,而转染si-circRPPH1则具有相反的效果。此外,miR-326模拟物或抑制剂可能会抵消这些作用(图7I-K)。这些发现表明,miR-326/ITGA5轴介导的circRPPH1激活FAK/ PI3K/AKT通路可促进TNBC细胞的侵袭性。
8)CircRPPH1促进TNBC细胞在体内的生长和转移
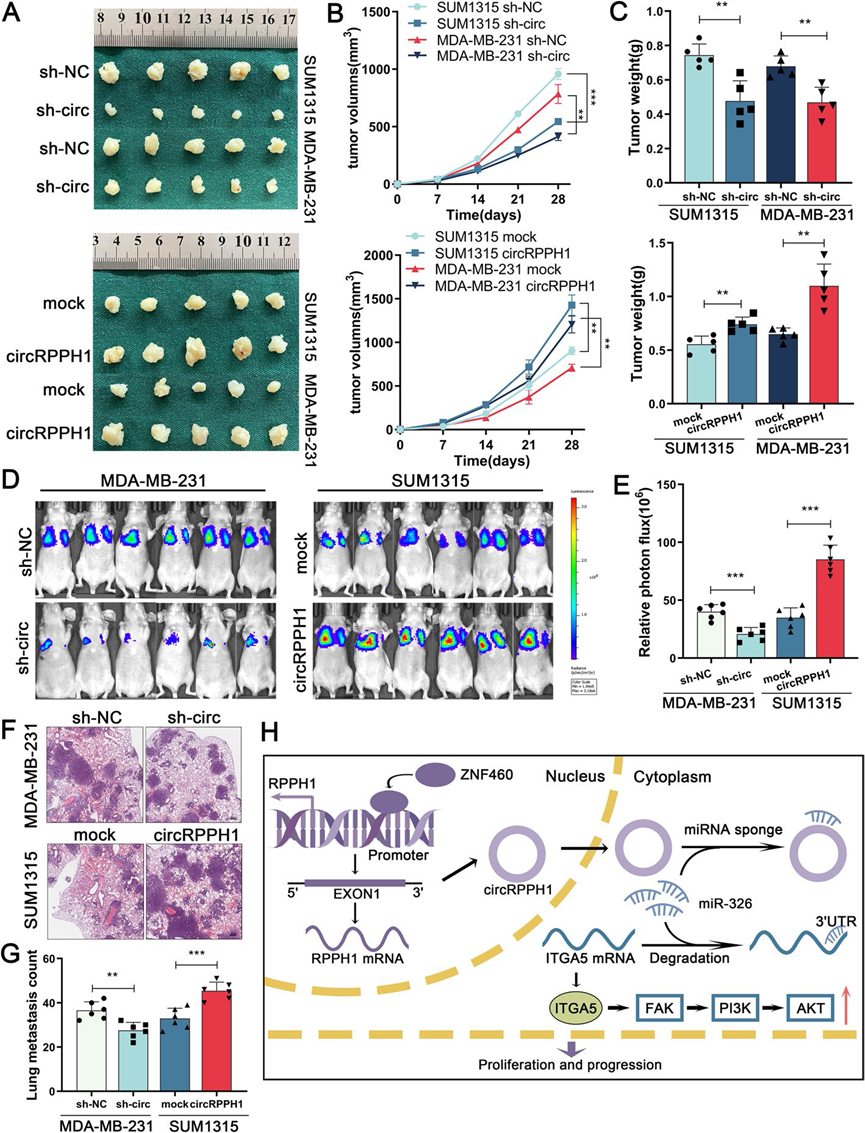
我们构建了稳定敲低或过表达circRPPH1的TNBC细胞系,以验证circRPPH1在体内的生物学功能。然后,我们将上述细胞系皮下注射到裸鼠体内,观察肿瘤的生长和大小。与对照组相比,circRPPH1敲低组的肿瘤大小和重量显著减小,而过表达circRPPH1后结果相反(图8A-C)。我们将感染荧光素酶质粒的TNBC细胞注射到裸鼠尾静脉,研究circRPPH1对转移的影响。生物发光成像和H&E染色分析显示,circRPPH1敲低后,肺转移灶的数量和大小显著减少,而circRPPH1过表达的影响则相反(图8D-G)。以上结果提示,在体内,circRPPH1诱导ITGA5促进TNBC细胞生长和转移。
结论:
我们发现了一种名为circRPPH1的新circRNA,它在TNBC中过表达,预示着预后不良。机制上,circRPPH1可以结合miR-326控制ITGA5的表达,激活FAK/PI3K/AKT通路,导致TNBC的发展。因此,circRPPH1可能为TNBC提供有用的诊断工具和潜在的治疗靶点。
实验方法:
qRT-PCR,Western blot,FISH,双荧光素酶报告分析,EdU,CCK-8,
参考文献:
Zhang C, Yu Z, Yang S, Liu Y, Song J, Mao J, Li M, Zhao Y. ZNF460-mediated circRPPH1 promotes TNBC progression through ITGA5-induced FAK/PI3K/AKT activation in a ceRNA manner. Mol Cancer. 2024 Feb 14;23(1):33. doi: 10.1186/s12943-024-01944-w.






