揭示卵巢癌耐药之谜—组蛋白乳酸化与超级增强子
卵巢癌是一种具有最高复发率和死亡率的妇科恶性肿瘤。尽管尼拉帕利可以有效影响其进展,但药物耐药性的挑战仍然存在。在此,我们构建了尼拉帕利耐药的卵巢癌细胞系,通过RNA原位构象测序识别异常激活的增强子和相关靶基因。值得注意的是,靶基因RAD23A在尼拉帕利耐药细胞中显著上调,抑制RAD23A恢复了它们的敏感性。此外,尼拉帕利耐药细胞中糖酵解的异常激活诱导了乳酸积累,促进了组蛋白H4K12赖氨酸残基的乳酸化。相关性分析显示,关键的糖酵解酶如丙酮酸激酶M和乳酸脱氢酶A在卵巢癌中与RAD23A表达显著正相关。此外,H4K12la通过MYC转录因子激活了尼拉帕利和RAD23A表达的超增强子(SE),从而增强了DNA损伤修复能力,促进了卵巢癌细胞的药物耐药性。总的来说,本研究的结果表明,乳酸积累导致组蛋白H4K12la的乳酸化,从而上调SE介导的异常RAD23A表达,促进卵巢癌细胞对尼拉帕利的耐药性,提示RAD23A可能是尼拉帕利耐药卵巢癌的潜在治疗靶点。本文于2025年3月发表于“Molecular Cancer”(IF=27.7)上。
技术路线:

结果:
1)尼拉帕利耐药卵巢癌细胞中超增强子与靶基因启动子之间的相互作用图谱
为了获得与卵巢癌尼拉帕利耐药相关的超增强子(SEs)及其靶基因之间的相互作用图谱,我们使用卡铂(10 μM)处理A2780/Nira和HO8910/Nira细胞48小时来模拟药物诱导的DNA损伤,然后通过药物浓度梯度法诱导尼拉帕利耐药性(图1A)。CCK-8实验揭示了尼拉帕利的IC50值(图1B–E)。将A2780/Nira和HO8910/Nira细胞的RIC-seq数据与公共增强子数据相结合,获得了与尼拉帕利耐药性相关的SEs及其靶基因之间的相互作用图谱(图1F)。RIC-seq测序检测到SE区域在chr19:13004808–13,072,187(命名为Nira-SE)与靶基因的启动子区域频繁相互作用,包括RAD23A、RNU2-2P、WDR74和RP11-424C20.2。其中,Nira-SE与RAD23A启动子区域的相互作用最为显著(图1G)。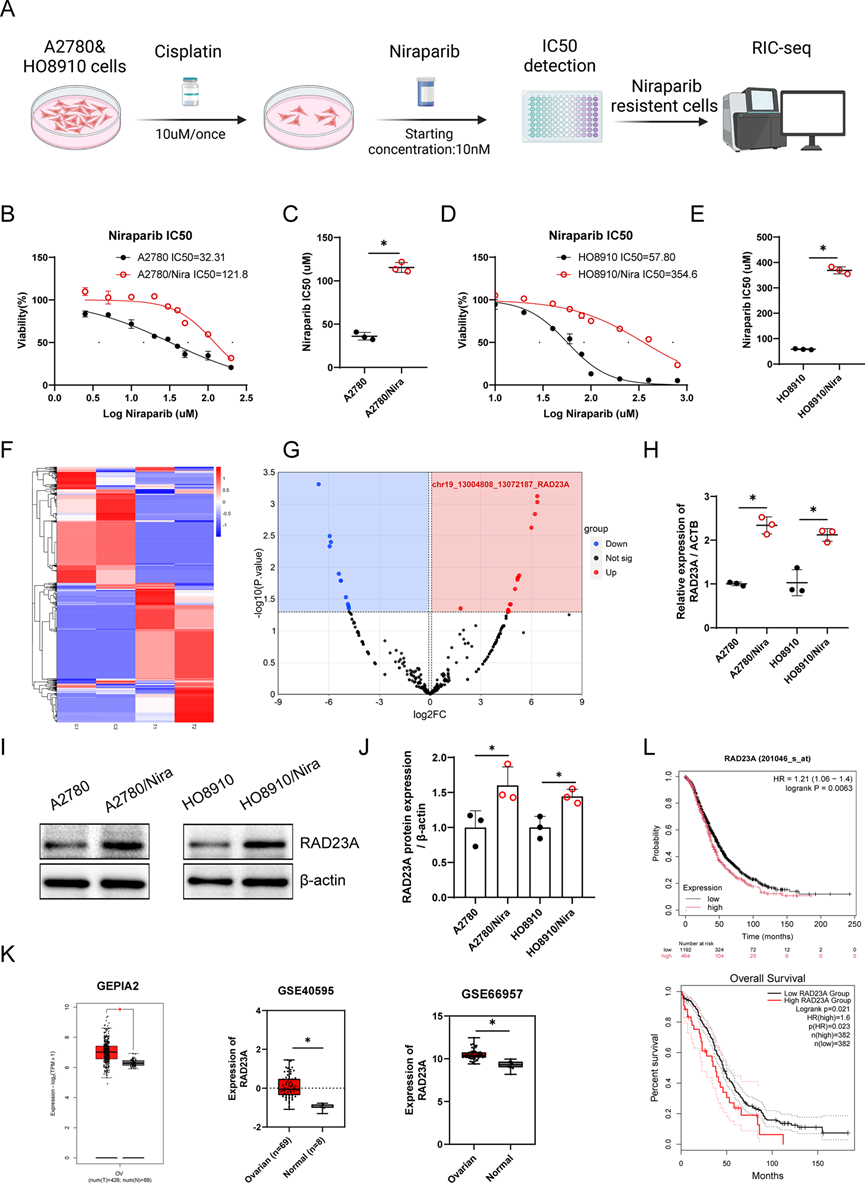
2)靶向RAD23A逆转了卵巢癌对尼拉帕利的耐药性
为了阐明RAD23A在卵巢癌尼拉帕利耐药性中的作用,分析了卵巢癌细胞系A2780、A2780/Nira、HO8910和HO8910/Nira中RAD23A的表达。值得注意的是,尼拉帕利耐药细胞中的RAD23A mRNA和蛋白质水平高于非耐药细胞(图1HJ)。对GSE40595、GSE66957数据集和GEPIA2网站的分析显示,RAD23A在卵巢癌组织中的表达增加(图1K),并且KMplot生存分析和GEPIA2数据集将RAD23A的高表达与卵巢癌的不良预后相关联(图1L)。为了评估RAD23A在尼拉帕利耐药卵巢癌细胞中的功能,我们转染了siRAD23A来敲减RAD23A的表达(图2A和B)。CCK-8实验显示,敲减RAD23A增加了卵巢癌细胞对尼拉帕利的敏感性(图2C和D)。此外,集落形成和EdU实验揭示,尼拉帕利耐药细胞的增殖能力在RAD23A敲减后显著降低(图2E和F)。另外,RAD23A的过表达在预先用铂类药物处理的A2780和HO8910细胞中增加了尼拉帕利耐药性和细胞增殖能力(图2G-J)。构建了尼拉帕利耐药细胞的异种移植肿瘤模型和来自卵巢癌患者的类器官模型,以验证RAD23A的体内治疗效果。值得注意的是,与siNC组相比,siRAD23A组在皮下肿瘤形成方面表现出显著的抑制作用;siRAD23A与尼拉帕利联合治疗组在皮下肿瘤形成方面的抑制作用显著高于siNC+尼拉帕利组(图2K)。同样,对类器官的分析显示,与siNC组相比,siRAD23A组在类器官生长方面表现出显著的抑制作用;siRAD23A与尼拉帕利联合治疗组在类器官生长方面的抑制作用也显著高于siNC+尼拉帕利组(图2L和M)。 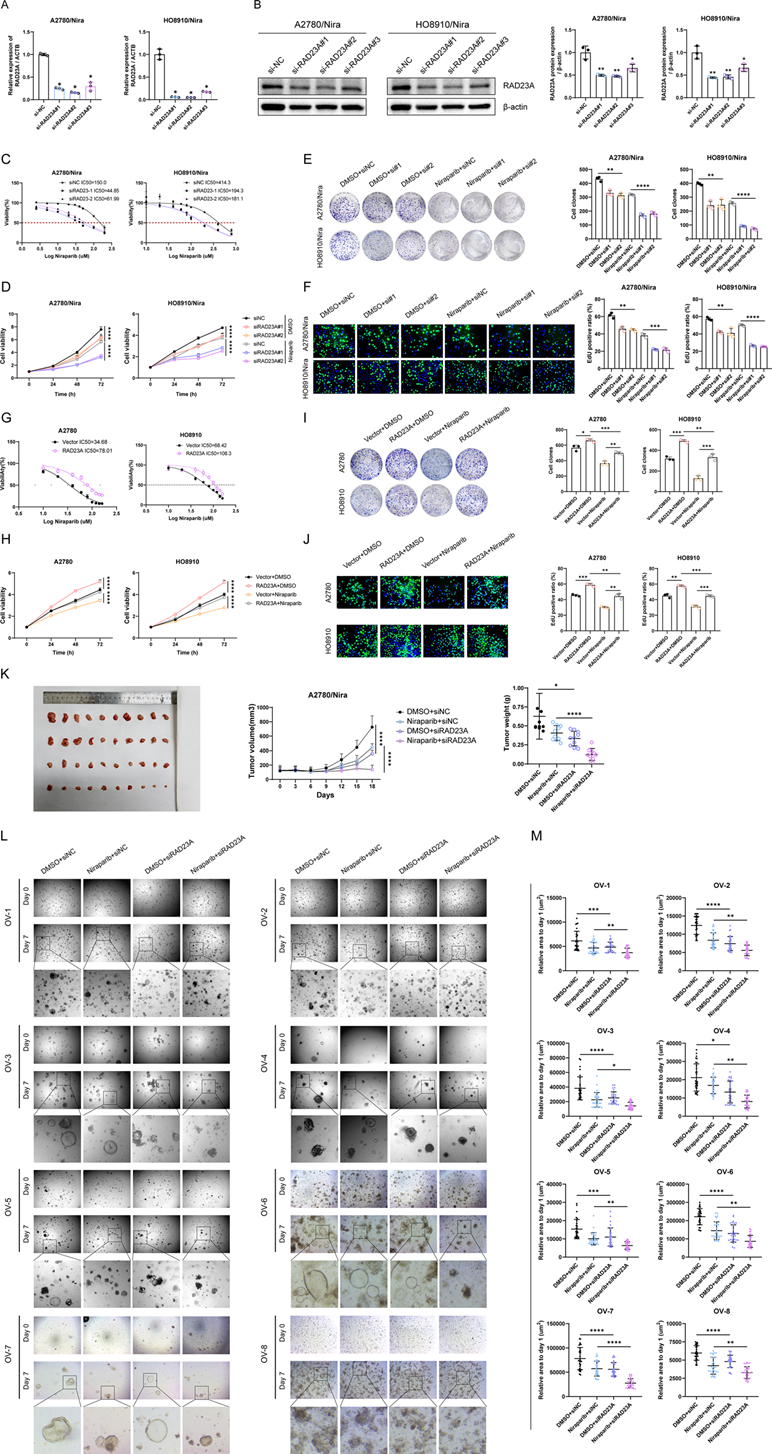
3)RAD23A通过调节DNA损伤修复参与卵巢癌的尼拉帕利耐药
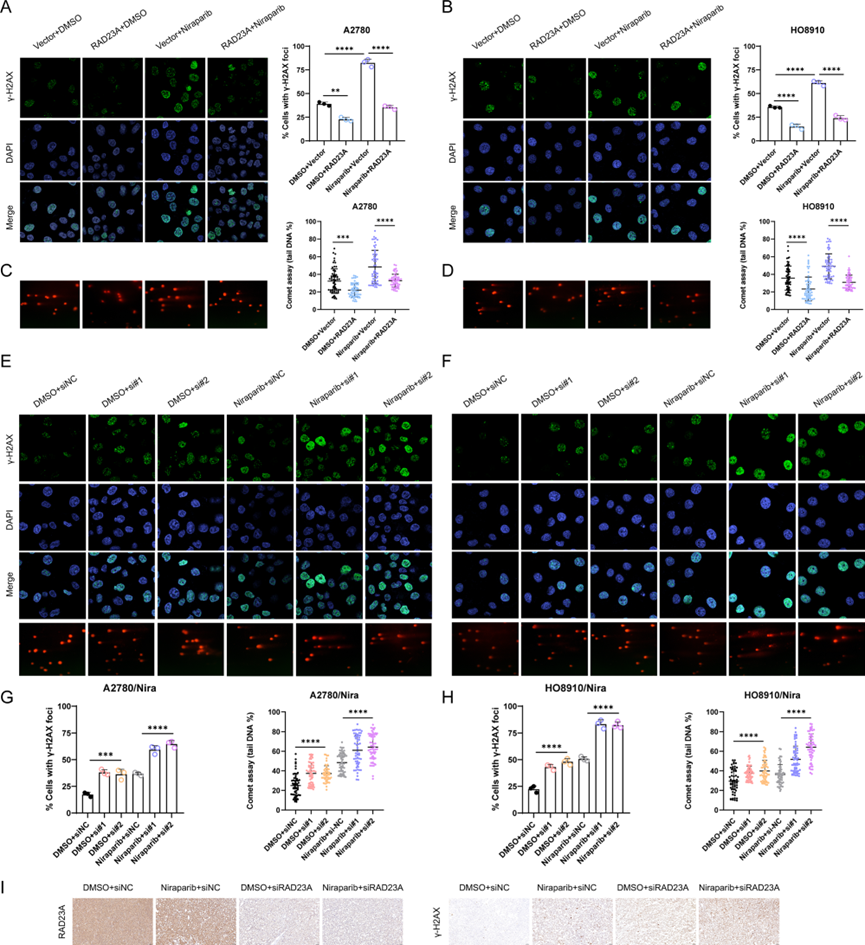
RAD23A是NER途径的重要组分,能够修复由紫外线辐射和化学药物等多种因素引起的DNA损伤。因此,在尼拉帕利耐药卵巢癌细胞中评估了其修复DNA损伤的能力。免疫荧光实验显示,RAD23A的过表达可以减少预先用铂类药物处理的A2780和HO8910细胞中γ-H2AX的表达,γ-H2AX是双链DNA损伤的标志物(图3A-B)。此外,彗星实验确认了RAD23A过表达后DNA损伤程度的降低,这表明RAD23A高水平可以增加DNA损伤修复(图3C-D)。此外,下调RAD23A显著增加了DNA损伤(图3E-H)。类似地,小鼠异种移植肿瘤组织的免疫组化结果显示,siRAD23A+尼拉帕利组在γ-H2AX表达上出现了显著增加(图3I)。这些结果提示,RAD23A通过调节DNA损伤修复参与卵巢癌对尼拉帕利的耐药性。
4)阻断超增强子逆转了卵巢癌对尼拉帕利的耐药性
为了阐明RAD23A在卵巢癌化疗耐药性中的表观遗传重塑机制,进行了生物信息学分析。值得注意的是,在FANTOM5门户网站上,Nira-SE区域鉴定出了两个增强子,分别命名为E1(chr19:13023589–13,024,232)和E2(chr19:13048278–13,048,689)(图4A)。接下来,利用CRISPR-Cas9技术敲除了E1和E2(图4B和C),以评估它们对RAD23A转录活性的影响。qPCR和western blotting的结果显示,敲除E1或E2中的任何一个都显著降低了RAD23A的表达,而在E1和E2联合敲除后,RAD23A的表达进一步下调(图4D和E)。为了评估阻断Nira-SE对卵巢癌尼拉帕利耐药性的影响,特别在A2780/Nira和HO8910/Nira细胞中敲除了E1和E2。CCK-8实验显示,敲除E1或E2增加了耐药细胞对尼拉帕利的敏感性(图4F和G)。此外,集落形成和EdU实验表明,敲除E1或E2后,尼拉帕利耐药细胞的增殖能力显著降低(图4H和I)。此外,敲除E1或E2后,γ-H2AX的表达显著增加(图4J),DNA损伤程度加剧(图4K)。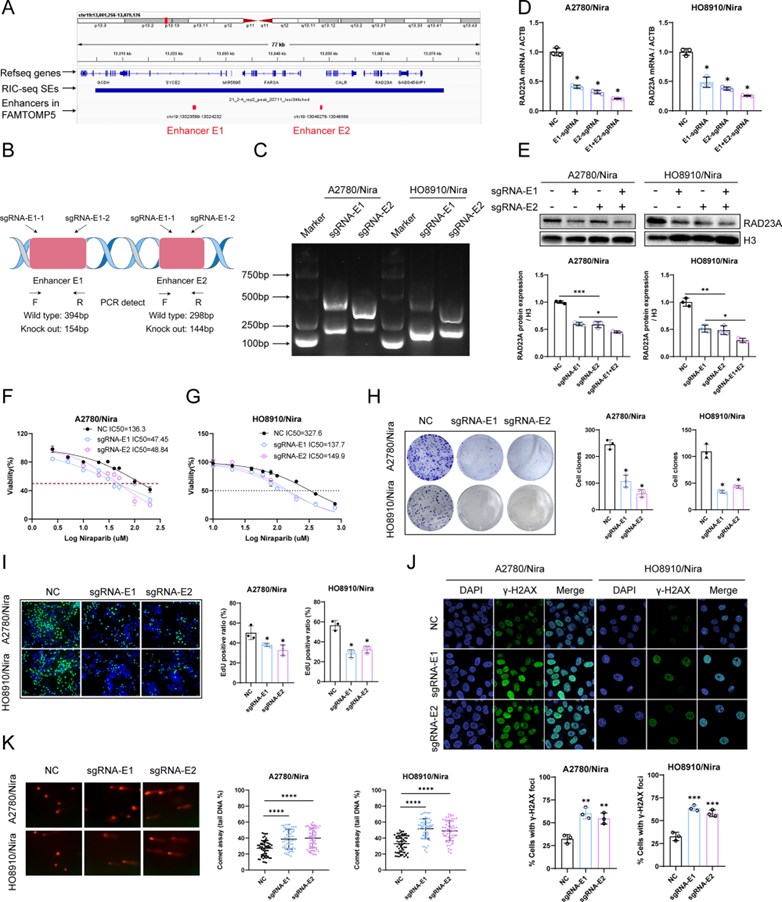
5)Nira-SE促进致癌TF MYC向启动子的募集
TFs介导SE调控网络并以基因特异性的方式启动转录。因此,通过交叉比对JASPAR、PROMO、Cistrome和ENCODE数据库的预测结果,识别了与RAD23A相关的TFs。总共鉴定出了七个TFs,分别是YY1、USF2、MYC、E2F1、RELA、GATA1和USF1(图5A),并验证了它们在卵巢癌中的作用。值得注意的是,敲减MYC显著降低了RAD23A的mRNA水平(图5B和C)和蛋白质水平(图5D–F)。ChIP-qPCR分析显示,MYC富集于A2780和HO8910细胞的RAD23A启动子(图5G和H)、增强子E1和E2区(图5I和J),且在其相对耐尼帕尼细胞(图5K-M)中富集更为显著,表明MYC是参与耐尼帕尼卵巢癌中RAD23A转录调控的关键TF。接下来,评估了SEs对MYC介导的RAD23A基因转录激活的影响。ChIP-qPCR分析显示,在E1和E2敲除后,MYC在RAD23A启动子区域的富集显著减少(图5N),表明E1和E2敲除有效地抑制了MYC在RAD23A启动子区域的富集,从而影响了其转录活性。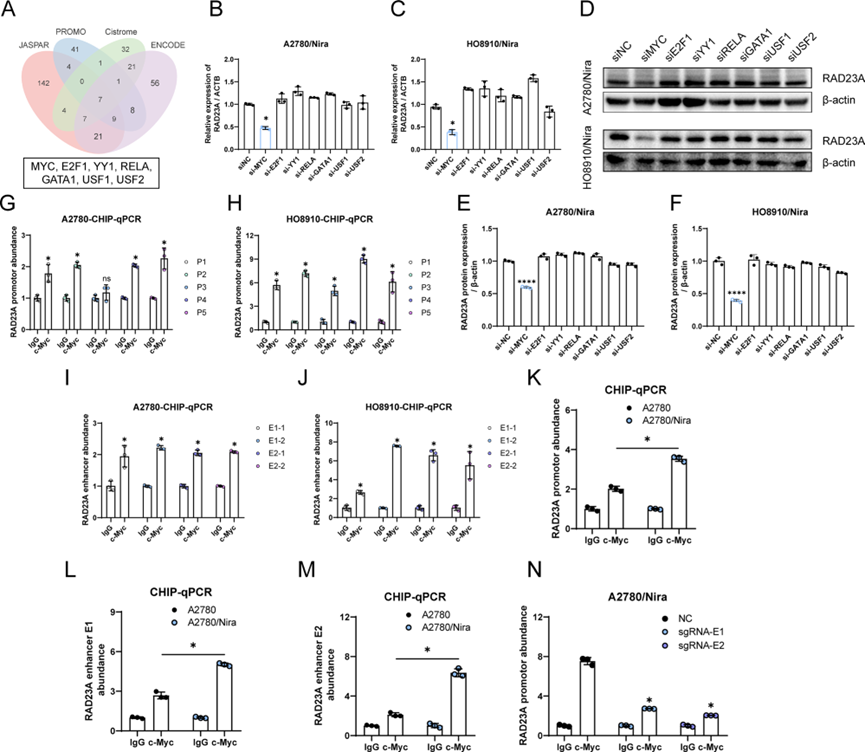
6)在尼拉帕利耐药的卵巢癌细胞中糖酵解过程显著激活
糖酵解可以驱动肿瘤细胞的恶性进展和药物耐药性。因此,本研究评估了糖酵解和组蛋白乳酸化在卵巢癌获得尼拉帕利耐药性过程中RAD23A超增强子的形成和激活中的作用。因此,检测了尼拉帕利耐药细胞的糖酵解指标,包括耗氧率(OCR)、细胞外酸化率(ECAR)和乳酸生成。值得注意的是,与非耐药细胞相比,A2780/Nira和HO8910/Nira细胞的OCR显著降低(图6A),而ECAR增加(图6B);耐药细胞的乳酸产生显著增加(图6C)。进一步的体外实验显示,敲减糖酵解相关关键酶丙酮酸激酶M(PKM)或乳酸脱氢酶A(LDHA)显著提高了它们对尼拉帕利的敏感性(图6D),抑制了尼拉帕利耐药细胞的增殖(图6E),并增加了DNA损伤水平(图6F)。相反,添加外源性乳酸增强了卵巢癌细胞的增殖和尼拉帕利耐药性,并降低了DNA损伤水平。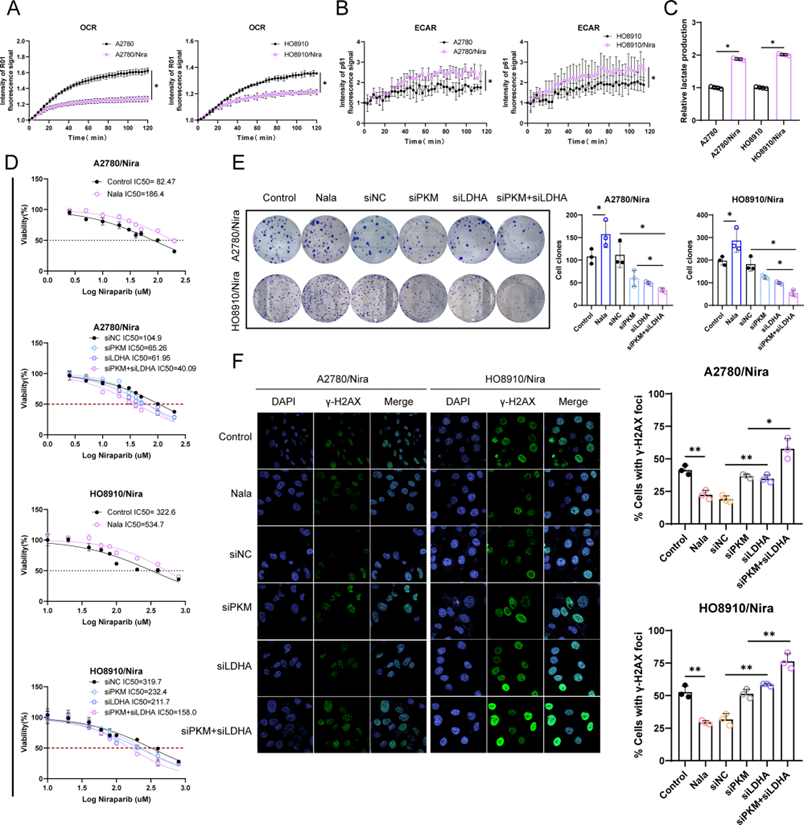
7)组蛋白乳酸化促进RAD23A的表达
尽管耐药细胞中糖酵解的激活导致乳酸积累,但其对RAD23A基因表达的影响尚不清楚。因此,在GEPIA2和ICGC数据集中分析了己糖激酶2、PKM、LDHA与RAD23A的表达相关性。值得注意的是,PKM、LDHA和RAD23A的表达呈正相关(图7A和B),并且在卵巢癌组织中PKM和LDHA的表达显著增加(图7C)。为了阐明糖酵解途径通过组蛋白乳酸化对RAD23A转录和表达的调控作用,使用了一种泛乳酸化抗体来检测乳酸化的整体水平。值得注意的是,尼拉帕利耐药细胞中组蛋白位置的乳酸化水平显著增加(图7D),在添加外源性乳酸(乳酸钠,Nala)后,乳酸化水平进一步增加,同时RAD23A的表达也增加(图7E-F)。相反,当卵巢癌细胞用糖酵解抑制剂2-DG处理时,组蛋白乳酸化和RAD23A的表达显著降低(图7G)。在耐药细胞中敲减PKM或LDHA显著降低了RAD23A的mRNA和蛋白质水平,而添加外源性乳酸恢复了RAD23A的表达(图7H和I)。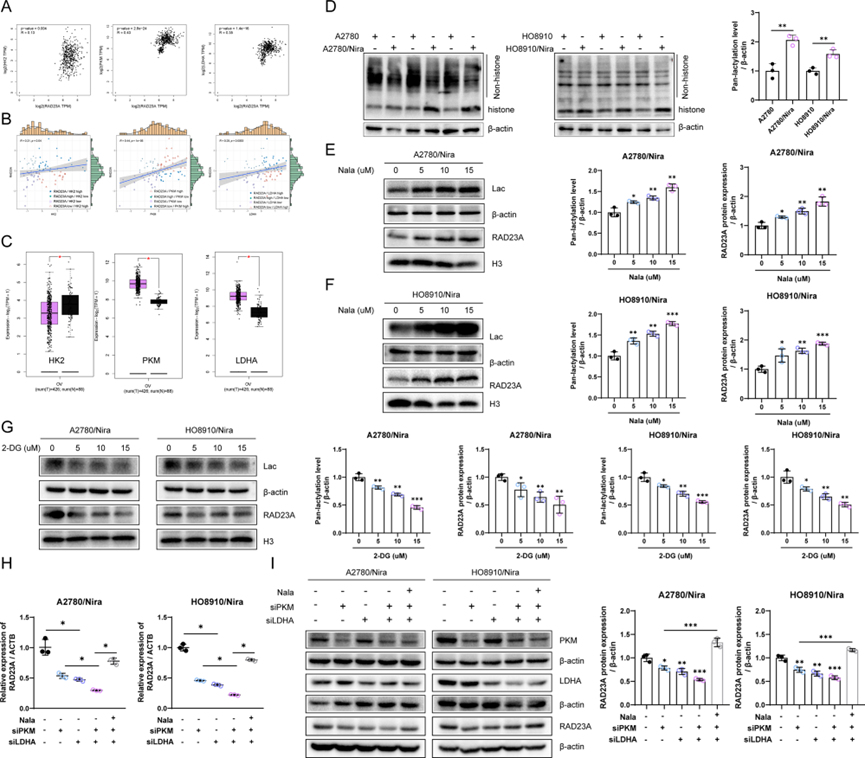
8)组蛋白H4K12la通过激活Nira-SE促进RAD23A的转录
为了验证组蛋白修饰位点在转录调控中的作用,检测了尼拉帕利耐药细胞中四种核心组蛋白(即H2A、H2B、H3和H4)的乳酸化情况。CO-IP结果显示,尼拉帕利耐药细胞中H4的乳酸化显著增加(图8A-B)。此外,在H4中识别出了多种常见的乳酸化赖氨酸残基位点,包括H4K5la、H4K8la、H4K12la和H4K16la。值得注意的是,H4K12la在耐药细胞中的增加最为显著(图8C-D)。同样,外源性乳酸和2-DG分别显著增加了和降低了H4K12la的水平(图8E-F)。此外,在耐药细胞中敲减PKM或LDHA导致H4K12la水平下降,而外源性乳酸逆转了这一效果(图8G-H)。这些结果表明,H4K12la乳酸化是调控尼拉帕利耐药卵巢癌细胞的关键组蛋白修饰位点。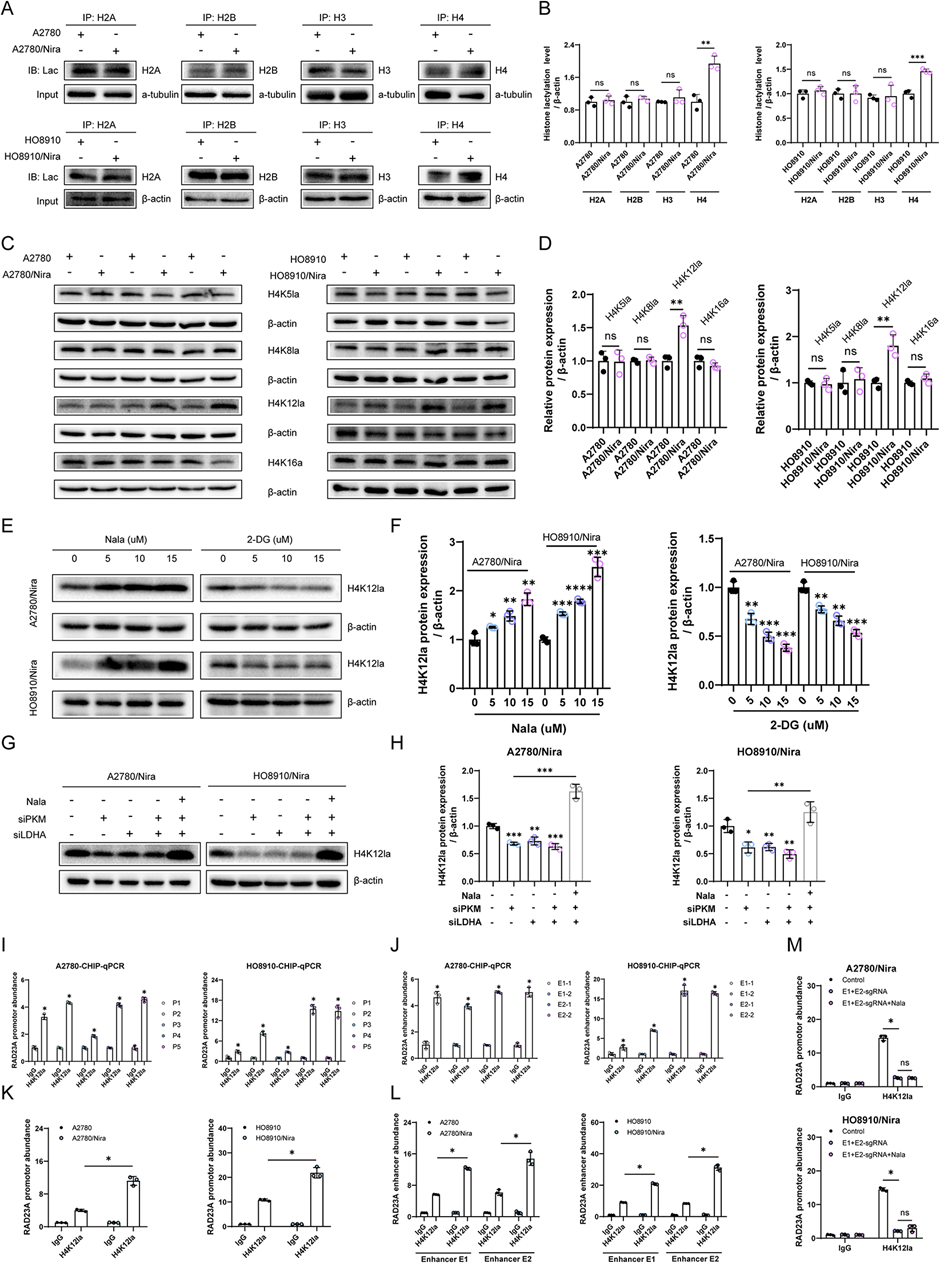
结论:
本研究阐明了糖酵解和组蛋白乳酸化在调节卵巢癌尼拉帕利耐药中基因表达的机制,提示NER途径相关的RAD23A作为解决卵巢癌尼拉帕利耐药的新治疗靶点。
实验方法:
异种移植肿瘤实验,CRISPR-cas9技术,CCK-8,EdU,集落形成试验,免疫荧光,彗星试验,qPCR,Western blotting,CO-IP,ChIP,RIC-seq
参考文献:
Lu B, Chen S, Guan X, Chen X, Du Y, Yuan J, Wang J, Wu Q, Zhou L, Huang X, Zhao Y. Lactate accumulation induces H4K12la to activate super-enhancer-driven RAD23A expression and promote niraparib resistance in ovarian cancer. Mol Cancer. 2025 Mar 19;24(1):83. doi: 10.1186/s12943-025-02295-w






