POM121 O-GlcNAc糖基化通过增强c-MYC核输入和ECM重编程促进非小细胞肺癌骨转移
非小细胞肺癌(NSCLC)的骨转移是一种破坏性的并发症,严重损害患者的生存。然而,驱动这一侵袭过程的基础分子机制仍未完全阐明。为了系统研究这些机制,我们将高度骨转移的NSCLC亚群与其亲本细胞进行了比较。值得注意的是,我们在该转移亚群中发现了OGT的表达升高。我们进一步证实,核孔蛋白POM121 Ser199位点的O-GlcNAc糖基化显著增加,并驱动了NSCLC的骨转移。在机制上,POM121的O-GlcNAc糖基化减弱了其与E3泛素连接酶TRIM21的相互作用,从而拮抗泛素化并稳定POM121。积聚的POM121增强了致癌转录因子c-MYC的核输入。随后,细胞核内的c-MYC协调下游细胞外基质(ECM)相关基因的转录激活。总之,我们阐明了一条此前未被识别的、关键驱动NSCLC骨转移的OGT-POM121-c-MYC-ECM轴。至关重要的是,临床分析显示,OGT、POM121和c-MYC的高水平表达与不良临床预后呈正相关。这些发现确立了OGT-POM121-c-MYC-ECM轴作为NSCLC骨转移的潜在诊断生物标志物和有前景的治疗靶点。本文于2026年2月发表于Oncogene(IF=7.3)上。
技术路线:

结果:
1)POM121在骨转移H460-BM亚系中表现出明显的O-GlcNAc糖基化
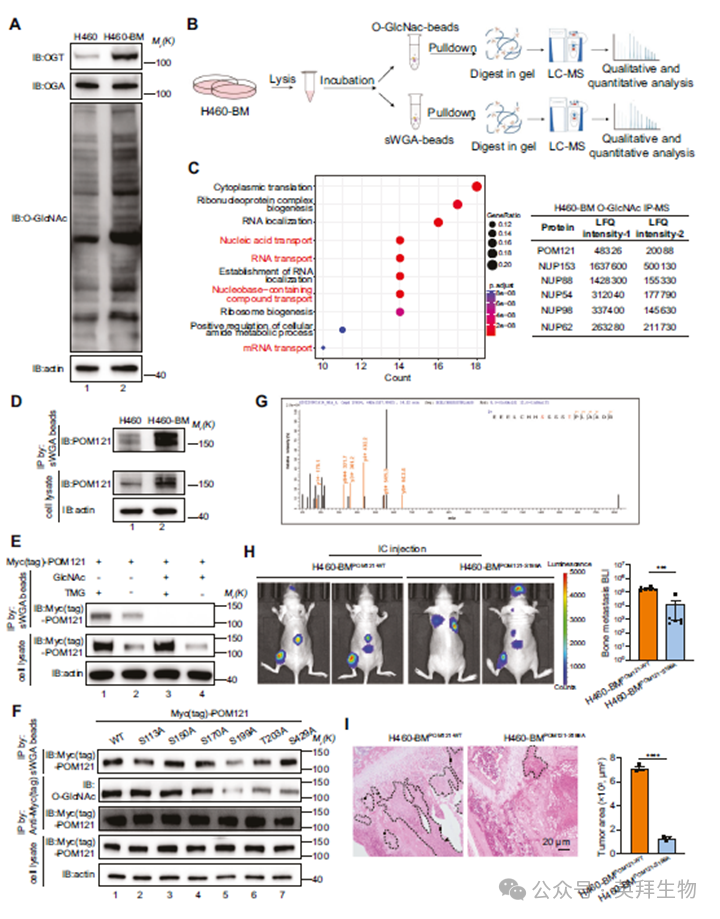
我们试图确定O-GlcNAc糖基化是否驱动非小细胞肺癌的骨转移。我们检测了H460细胞和骨转移亚系H460-BM中的O-GlcNAc糖基化水平。我们发现H460-BM细胞的O-GlcNAc糖基化水平明显高于亲本细胞系(图1A)。为了鉴定H460-BM细胞中驱动骨转移的特异性O-GlcNAc糖基化蛋白,我们使用O-GlcNAc抗体偶联珠和sWGA珠与H460-BM裂解物孵育,然后进行LC-MS/MS分析(图1B)。有趣的是,通路分析显示,这些O-GlcNAc糖基化蛋白在核细胞质运输途径中显著富集,核孔复合物(NPC)蛋白显著富集(图1C)。在这些核孔蛋白中,POM121在H460-BM和亲本H460细胞之间表现出明显不同的O-GlcNAc糖基化:在转移细胞中表现出强烈的修饰,而在亲本细胞中表现出最低水平的修饰(图1D)。OGA抑制提高了H460-BM细胞中POM121的O-GlcNAc糖基化(图1E),而用GlcNAc预先阻断sWGA,消除了POM121的下拉,证实了O-GlcNAc特异性结合(图1E)。为了验证POM121 O-GlcNAc糖基化在骨转移中的功能作用,我们对H460-BM细胞裂解液进行了抗POM121免疫沉淀,随后进行了LC-MS分析。由此鉴定出POM121上的六个候选O-GlcNAc糖基化位点:S113、S150、S170、S199、T203和S429。定点突变实验表明,与野生型POM121相比,S199A突变显著降低了O-GlcNAc糖基化水平,从而确定S199为主要修饰位点(图1F),LC-MS/MS直接证实了S199位点的O-GlcNAc糖基化(图1G)。为了评估其功能意义,我们构建了表达POM121S199A突变体的H460-BM细胞(称为H460-BMPOM121-S199A)。H460-BMPOM121-S199A亚系在裸鼠体内的骨转移负荷低于亲本H460-BM组(图1H),组织病理学检查证实其转移灶数量更少且体积更小(图1I)。综上所述,这些结果确立了POM121在S199位点的特异性O-GlcNAc糖基化是驱动H460细胞骨转移的关键因素。
2)O-GlcNAc糖基化稳定POM121促进NSCLC骨转移
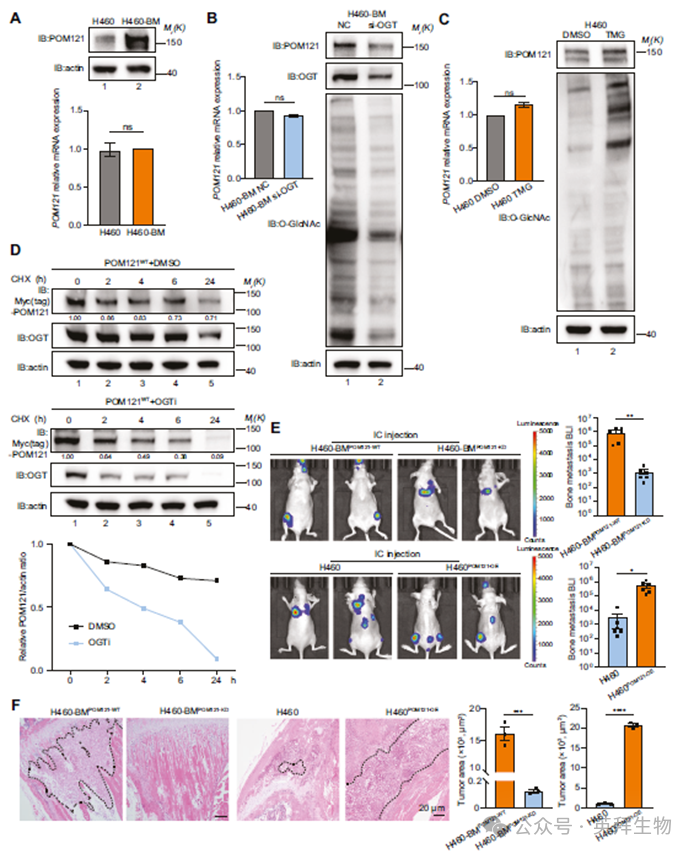
为了确定POM121 O-GlcNAc糖基化如何促进NSCLC骨转移,我们评估了其对蛋白质稳定性的影响。免疫印迹显示,H460-BM中POM121蛋白显著升高,mRNA水平不变(图2A)。与此一致的是,在H460-BM细胞中通过si-OGT或OGT抑制剂(OGTi)降低O-GlcNAc糖基化水平,显著降低了POM121蛋白水平,但未改变其mRNA水平(图2B)。相反,在H460细胞中过表达OGT或TMG处理增加POM121蛋白水平(图2C)。为了最终确认O-GlcNAc修饰在增强POM121蛋白稳定性中的作用,我们进行了CHX追逐实验,证实了抑制OGTi介导的O-GlcNAc糖基化会加速POM121的降解(图2D)。综上所述,这些发现证实O-GlcNAc糖基化在翻译后水平增强了POM121的稳定性。为了验证O-GlcNAc糖基化介导的POM121稳定化驱动NSCLC骨转移,我们构建了POM121敲低的H460-BM细胞(H460-BMPOM121-KD)和过表达POM121的H460细胞(H460POM121-OE)。与H460POM121-OE组显著增加的骨转移发生率和负荷相比,H460-BMPOM121-KD细胞的骨转移定植能力显著降低(图2E)。骨切片的组织病理学检查显示,注射H460-BMPOM121-KD细胞的小鼠肿瘤负荷极小,表现为几乎检测不到的转移灶和稀疏的肿瘤细胞浸润。与此形成鲜明对比的是,H460POM121-OE细胞形成了广泛的转移病灶,伴有密集的肿瘤细胞簇(图2F)。这些发现确立了O-GlcNAc糖基化介导的POM121稳定化是驱动NSCLC骨转移的关键因素。
3)Ser199的O-GlcNAc糖基化通过拮抗TRIM21介导的泛素化来稳定POM121
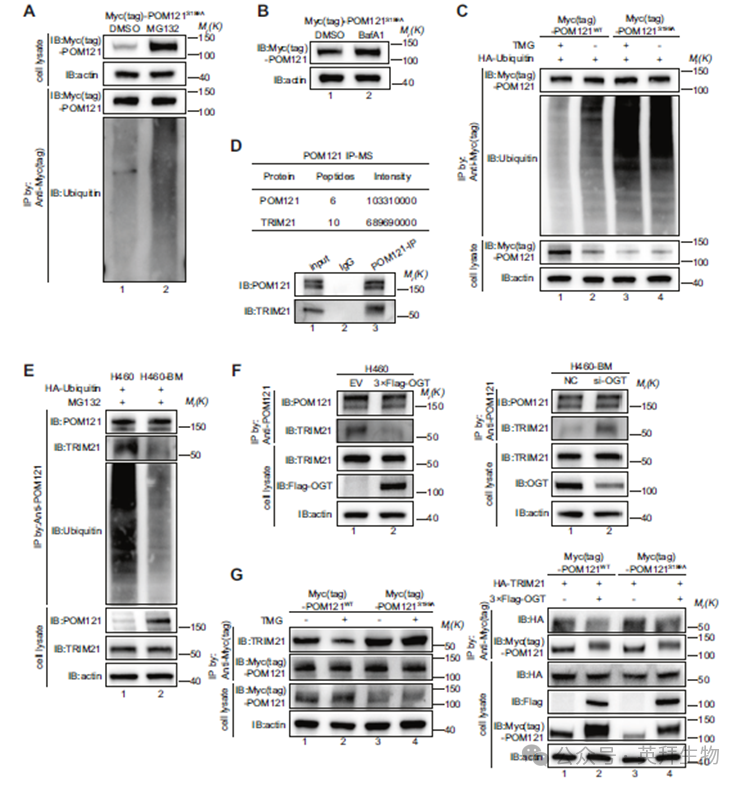
为了阐明O-GlcNAc糖基化如何稳定POM121,我们通过用泛素-蛋白酶体抑制剂MG132或自噬-溶酶体抑制剂巴弗洛霉素A1(BafA1)处理POM121S199A突变体细胞(易降解型),表征了其降解途径。MG132显著增加了POM121S199A的蛋白丰度和泛素化水平(图3A),而BafA1的作用微乎其微(图3B),表明其主要通过泛素-蛋白酶体途径介导降解。关键的是,通过TMG增强O-GlcNAc糖基化抑制了POM121的泛素化,同时增加了其蛋白表达和O-GlcNAc修饰,但未能减少缺失O-GlcNAc糖基化的POM121S199A突变体的泛素化(图3C)。这些数据证明,O-GlcNAc糖基化通过拮抗POM121的泛素化来稳定该蛋白。为了从机制上阐明O-GlcNAc糖基化如何拮抗POM121泛素化,我们进行了免疫沉淀-质谱分析(IP-MS),鉴定出E3泛素连接酶TRIM21为主要相互作用蛋白,并通过免疫共沉淀(co-IP)验证了POM121与TRIM21的直接结合(图3D)。比较分析显示,与亲本H460细胞相比,骨转移性H460-BM细胞中的POM121-TRIM21相互作用显著减弱,这与转移细胞中泛素化减少和POM121丰度增加相关(图3E)。相反,在H460细胞中过表达OGT会削弱POM121-TRIM21的结合,而在H460-BM细胞中敲低OGT则增强这种相互作用(图3F)。关键的是,TMG处理或OGT过表达破坏了野生型POM121(POM121WT)与TRIM21的相互作用,但未能减少缺失O-GlcNAc糖基化的POM121S199A突变体与TRIM21的结合(图3G)。综上所述,这些数据证明S199位点的O-GlcNAc糖基化阻碍了TRIM21的识别,从而抑制泛素化并稳定POM121。
4)POM121促进c-MYC核易位驱动骨转移
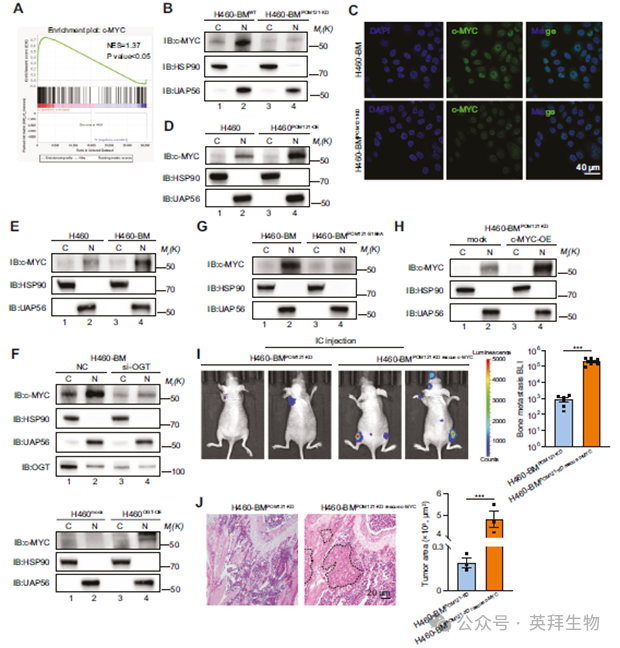
在明确了O-GlcNAc糖基化稳定的POM121驱动NSCLC骨转移之后,我们研究了POM121丰度增加如何促进转移。作为促进核输入的核孔组分,我们通过对比H460-BM与H460-BMPOM121-KD细胞的RNA测序探究了POM121的作用。转录组分析揭示了一个依赖POM121的基因特征,基因集富集分析(GSEA)显示,与POM121敲低对照组相比,表达POM121的转移细胞中c-MYC致癌程序显著富集(图4A)。为了验证POM121依赖性的c-MYC核输入,核质分离实验显示POM121耗竭严重损害了c-MYC的核积累(图4B),免疫荧光实验也独立证实了POM121缺陷细胞中的核输入效率降低(图4C)。相反,在低POM121水平的H460细胞中过表达POM121显著增强了c-MYC的核易位(图4D)。关键的是,该调控轴具有生理相关性:与亲本H460细胞相比,骨转移性H460-BM细胞表现出主要的c-MYC核定位(图4E)。这些数据确立了POM121是调控NSCLC中c-MYC核输入的关键核孔组分。基于O-GlcNAc糖基化介导的POM121稳定化作为核质运输调控因子这一发现,我们采用了药理学和遗传学方法进行研究。在H460-BM细胞中通过si-OGT或OGTi减少O-GlcNAc糖基化,显著减弱了c-MYC的核输入(图4F);而在H460细胞中过表达OGT或经TMG处理则增强了O-GlcNAc糖基化并促进了c-MYC的核积累(图4F)。关键的是,与野生型相比,缺失O-GlcNAc糖基化的POM121S199A突变体表现出c-MYC核易位减少(图4G)。为了研究c-MYC核易位是否驱动NSCLC骨转移,我们在POM121敲低的H460-BM细胞中重建了c-MYC的表达,恢复了核c-MYC的积累(图4H),并在裸鼠心脏内注射模型中基本恢复了POM121缺失引起的骨定植缺陷(图4I,J)。这些研究结果表明,在非小细胞肺癌中,POM121通过c-MYC核易位作为关键的骨转移调节因子。
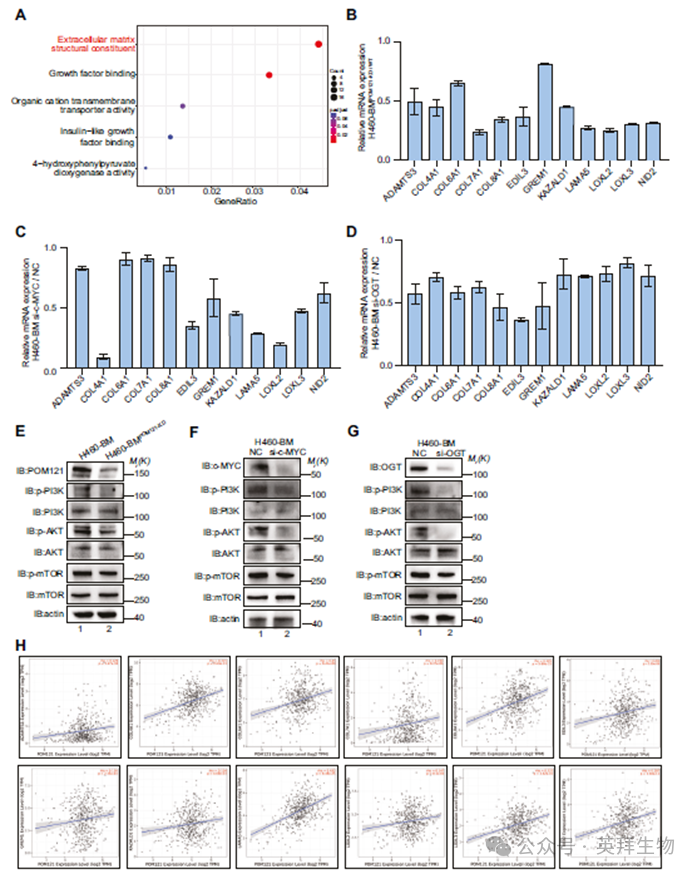
5)c-MYC促进NSCLC中ECM相关基因的转录和PI3K-AKT-mTOR的激活
为了明确POM121促进的c-MYC如何驱动骨转移,我们对POM121敲低(POM121KD)与野生型POM121(POM121WT)细胞进行了RNA测序,鉴定出细胞外基质(ECM)相关通路是与骨转移功能相关的关键c-MYC转录靶点(图5A)。RT-qPCR证实这些基因在H460-BMPOM121-KD细胞中显著下调(图5B)。与此互补的是,在H460-BM细胞中敲低c-MYC同样抑制了ECM基因的表达(图5C)。敲低OGT减少了POM121的O-GlcNAc糖基化并下调了ECM基因(图5D)。免疫印迹分析显示,与H460-BMPOM121-KD细胞相比,骨转移性H460-BM细胞中PI3K-AKT-mTOR组分的磷酸化激活增强(图5E),这证实了c-MYC驱动的ECM上调激活了PI3K-AKT-mTOR级联反应。一致地,在H460-BM细胞中敲低c-MYC抑制了通路激活(图5F)。在机制上,降低POM121的O-GlcNAc糖基化水平减少了PI3K/AKT/mTOR的磷酸化(图5G)。NSCLC患者数据显示,ECM基因表达与POM121及c-MYC水平均呈正相关(图5H),从而证实了POM121-c-MYC-ECM轴在通过ECM介导的PI3K-AKT-mTOR信号通路驱动NSCLC骨转移中的临床相关性。
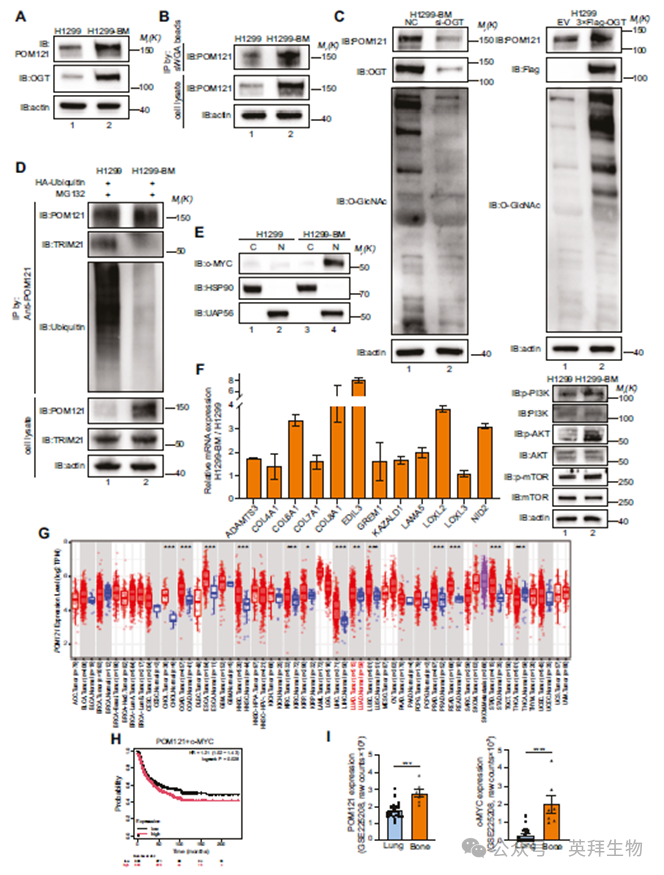
6)OGT-POM121-c-MYC-ECM轴驱动异质性NSCLC骨转移
为了验证O-GlcNAc糖基化POM121-c-MYC-ECM轴在NSCLC中的普遍相关性,我们通过向裸鼠心内注射H1299/H1437细胞,经体内迭代筛选构建了骨转移亚群(H1299-BM、H1437-BM)。免疫印迹分析显示,与亲本细胞系相比,骨转移亚群中的OGT和POM121蛋白水平显著升高(图6A)。值得注意的是,sWGA pull down实验显示骨转移谱系中POM121的O-GlcNAc糖基化水平大幅增加(图6B)。此外,功能获得和缺失实验证实OGT直接调节POM121的O-GlcNAc糖基化(图6C)。在机制上,增强的O-GlcNAc糖基化减弱了POM121与TRIM21的结合,从而减少了泛素化并稳定了转移变异株中的POM121(图6D)。另外,核质分离实验证明,在转移谱系中,增强的POM121介导了c-MYC的核易位(图6E),驱动了ECM基因的转录激活和PI3K-AKT-mTOR磷酸化(图6F)。为了验证OGT-POM121-c-MYC轴的临床相关性,对NSCLC数据库的分析显示,与癌旁正常组织相比,肿瘤组织中的POM121显著上调(图6G)。POM121和c-MYC的高共表达与这些患者队列中总生存期的缩短密切相关(图6H)。GSE225208 RNA测序队列证实,骨转移组织中POM121和c-MYC表达升高(图6I)。这些结果证实了OGT-POM121-c-MYC-ECM调控轴在NSCLC发病机制中既是具有前景的预后生物标志物,也是潜在的治疗靶点。
结论:
我们的研究结果描绘了一个此前未被认识的信号轴——OGT 介导的 O-GlcNA 糖基化稳定了包括 POM121在内的核孔蛋白,这促进了c-MYC的核输入以及随之而来的细胞外基质重编程,从而在非小细胞肺癌的骨转移中起到了关键的促进作用。这一机制不仅加深了我们对癌症进展中翻译后修饰与核运输之间功能相互作用的理解,还突显了针对 OGT-NPC-c-MYC-ECM 轴进行治疗的潜力。
参考文献:
Ren YZ, Zhao MN, Du FL, Wu L, Wang L, Lou JT. POM121 O-GlcNAcylation facilitates bone metastasis in non-small cell lung cancer through enhanced c-MYC nuclear import and ECM reprogramming. Oncogene. 2026 Mar;45(7):728-743. doi: 10.1038/s41388-026-03687-y.






