这年头纯纯scRNA还能发7分?!
近年来,单细胞测序(scRNA-seq)不断推动肿瘤微环境研究向更精细的层面发展。经典霍奇金淋巴瘤(CHL)一直被认为是一个“肿瘤细胞很少、免疫细胞很多”的肿瘤类型——恶性HRS细胞通常只占肿瘤组织的约1%,但却能够操控整个免疫微环境。
然而,一个长期被忽视的问题是:在复发的CHL中,B细胞究竟发挥了什么作用?
近期发表的一项研究通过对配对的初诊与复发CHL样本进行单细胞RNA测序(scRNA-seq)分析,发现B细胞群体发生显著变化:与晚期复发及初诊样本相比,早期复发CHL中初始B细胞显著富集,而记忆B细胞减少。在独立验证队列中,通过scRNA-seq和免疫组化均证实了早期复发样本中初始B细胞增加的现象。进一步分析发现,这些初始B细胞高表达免疫抑制基因LGALS9(编码Galectin-9)。Galectin-9可与调节性T细胞(Treg)上的HAVCR2(TIM-3)结合。细胞通讯分析显示:LGALS9⁺初始B细胞与HAVCR2⁺Treg之间存在显著相互作用;空间蛋白组学分析进一步证实:Galectin-9⁺初始B细胞;TIM-3⁺CD4⁺T细胞;HRS肿瘤细胞;在组织中呈空间邻近分布。这些结果提示:Galectin-9⁺初始B细胞可能通过构建免疫抑制微环境促进CHL早期复发。本研究揭示了一种此前未被认识的B细胞亚群,并为理解CHL复发的空间与转录组结构提供了新的见解。本文于2026年1月发表在《Blood Advances》IF:7.1杂志上。
技术路线:
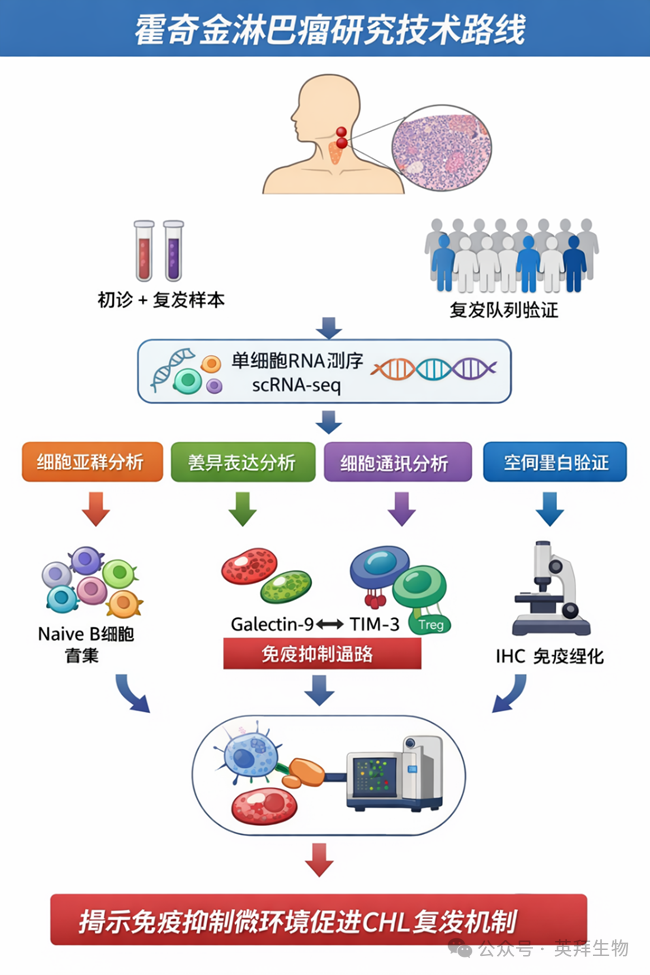
主要实验结果:
1、单细胞测序解析cHL肿瘤微环境的免疫细胞组成
研究者首先对cHL肿瘤样本进行了scRNA-seq,结果显示,cHL肿瘤组织中主要由多种免疫细胞组成,包括T细胞、B细胞、浆细胞、髓系细胞以及其他免疫相关细胞亚群。与许多实体瘤类似,真正的肿瘤细胞在组织中所占比例极低,而免疫细胞构成了肿瘤微环境的主体。
进一步的细胞类型注释表明,T细胞是肿瘤微环境中最主要的细胞群体,其次为B细胞和髓系细胞。该结果再次印证了cHL是一种高度免疫依赖型肿瘤,其发生发展很大程度上受到肿瘤微环境免疫细胞的调控。
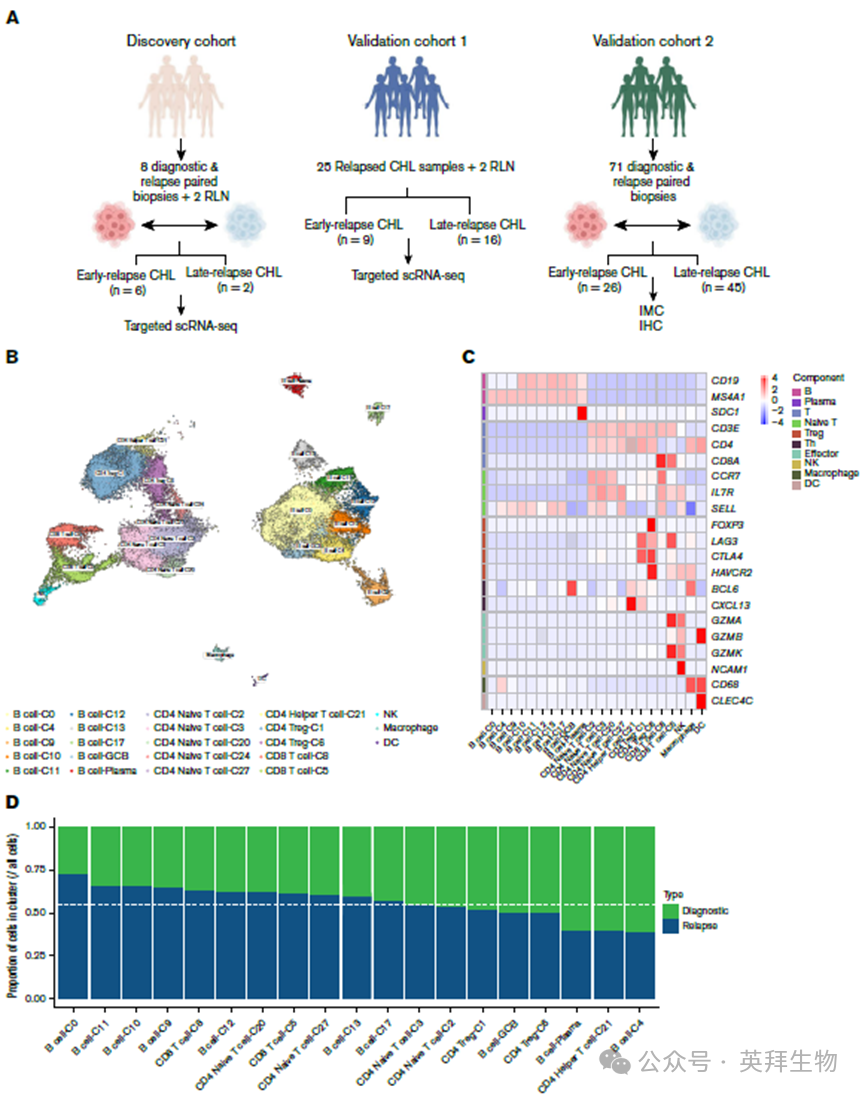
图1初诊和复发CHL的scRNA-seq表达谱
2、早复发与晚复发患者的免疫微环境存在显著差异
在明确肿瘤微环境总体细胞组成后,研究者进一步比较了早复发与晚复发患者之间的免疫细胞分布差异。结果显示,不同复发时间的患者在免疫细胞组成上存在明显差别,其中B细胞群体的变化尤为突出。
具体而言,早复发患者肿瘤组织中的B细胞总体比例明显低于晚复发患者,这提示B细胞可能在疾病控制中发挥保护性作用。然而,进一步分析发现,虽然B细胞总体比例下降,但某些特定B细胞亚群(如BC1)在早复发患者中却显著增加,而BC2显著减少,这一现象提示B细胞内部的亚群重塑可能在疾病复发过程中发挥关键作用。
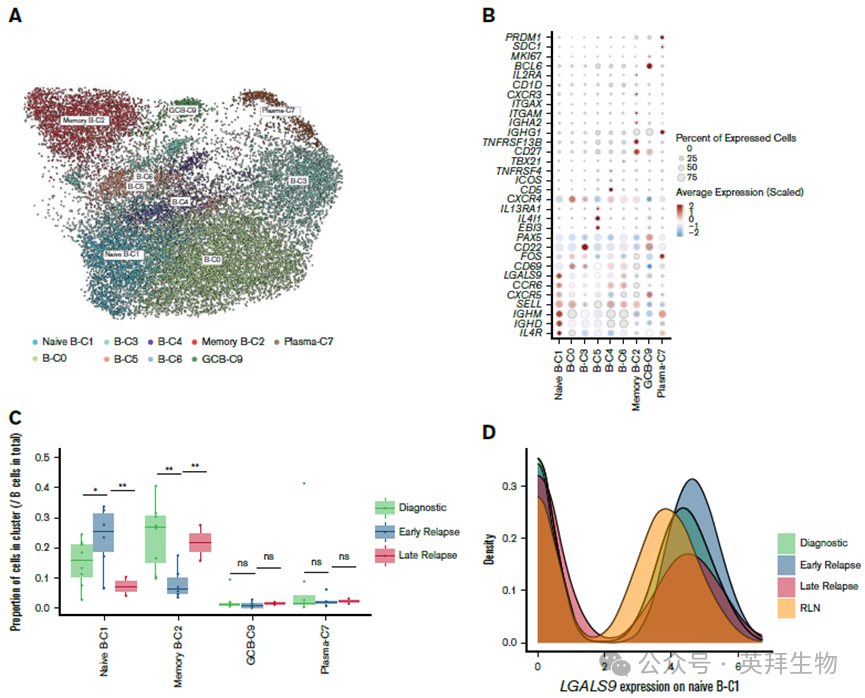
图2 scRNA-seq解释揭示初诊和复发CHL的B细胞差异
3、早复发患者中 naïve B细胞显著富集
为了进一步明确B细胞内部亚群的变化,研究者对B细胞进行了更精细的亚群划分,并鉴定出多个B细胞类型,包括 naïve B细胞、memory B细胞和浆细胞等。分析结果显示,早复发患者的肿瘤微环境中naïve B细胞比例显著升高,而晚复发患者则更倾向于富集memory B细胞。由于naïve B细胞通常代表尚未经历抗原刺激和类别转换的未成熟B细胞,这一结果提示,在早复发患者中,B细胞免疫反应可能处于较低成熟状态,从而削弱了抗肿瘤免疫能力。
在分子层面,研究者进一步发现免疫调控分子LGALS9(galectin-9)在naïve B细胞中显著上调。LGALS9是一种已知参与免疫抑制和免疫逃逸的关键分子,其高表达提示这些naïve B细胞可能不仅数量增加,同时还具备免疫调节功能,从而可能帮助肿瘤细胞逃避免疫监视。
为了验证单细胞测序的发现,研究者在独立患者队列中通过IgD免疫组织化学染色对naïve B细胞进行了蛋白水平验证。结果显示,早复发患者肿瘤组织中IgD⁺ B细胞比例显著高于晚复发患者,这一结果从组织学层面进一步证实了单细胞分析的结论。
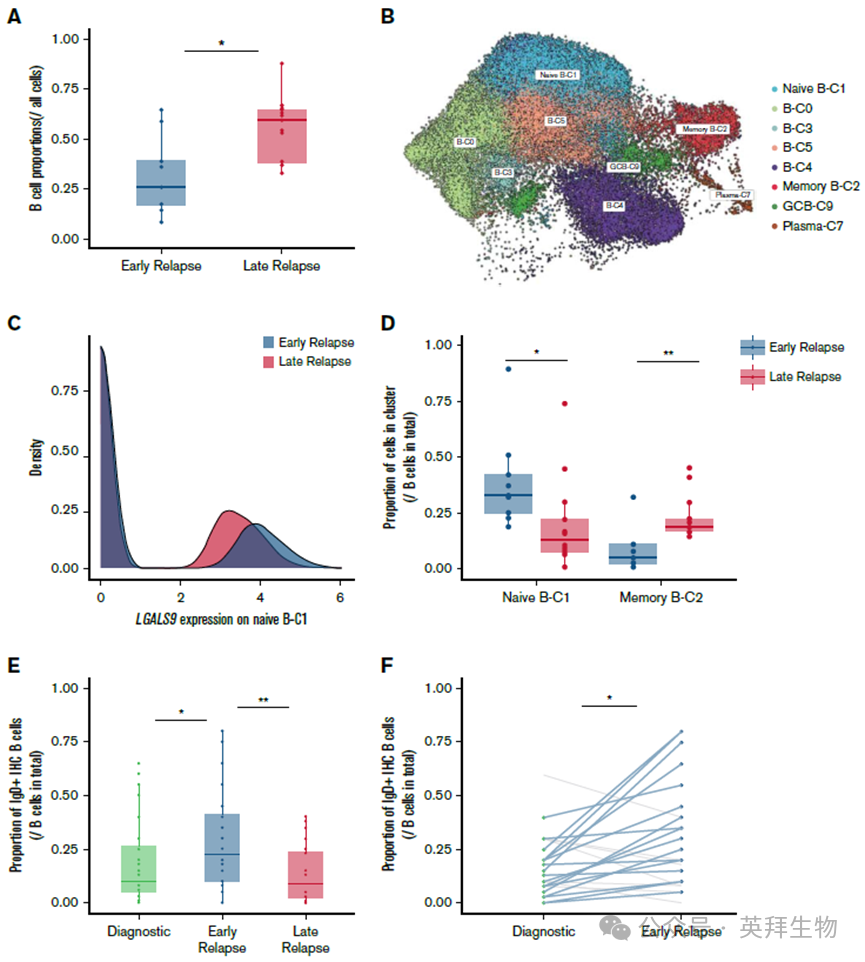
图3 在独立CHL队列中验证naïve B细胞富集
4、细胞互作分析揭示 naïve B细胞可能通过LGALS9参与免疫调控
为了进一步理解早复发患者中naïve B细胞富集可能带来的功能影响,研究者对肿瘤微环境中的细胞通讯进行了系统分析。通过配体–受体互作网络分析发现,B细胞与多种免疫细胞之间存在复杂的信号交流,其中naïve B细胞与T细胞及其他免疫细胞之间的相互作用尤为显著。这些结果提示,naïve B细胞不仅在数量上发生变化,还可能通过分子信号传递参与肿瘤微环境的免疫调控。
进一步分析发现,在早复发患者中,LGALS9相关的配体–受体互作信号明显增强。LGALS9编码的Galectin-9是一种重要的免疫调节分子,已被证实可以与T细胞表面的受体相互作用,从而调节T细胞功能并促进免疫抑制环境的形成。在本研究中,naïve B细胞被发现是LGALS9信号的重要来源之一,提示这一细胞亚群可能通过分泌Galectin-9参与肿瘤免疫微环境的重塑。
此外,细胞互作网络分析还显示,naïve B细胞与T细胞之间的通讯在早复发患者中更为活跃,特别是在涉及免疫调节和免疫抑制相关信号通路方面。该结果提示,在cHL肿瘤微环境中,naïve B细胞不仅是被动存在的免疫细胞群体,还可能通过与T细胞等免疫细胞的信号交流,影响抗肿瘤免疫反应。
总体而言,Figure 4 的分析进一步表明,早复发患者中富集的naïve B细胞可能通过LGALS9相关信号通路参与细胞间通讯,从而促进免疫抑制性微环境的形成。这一发现为理解cHL早期复发的免疫机制提供了新的线索,并提示naïve B细胞及其相关信号轴可能成为潜在的治疗靶点。
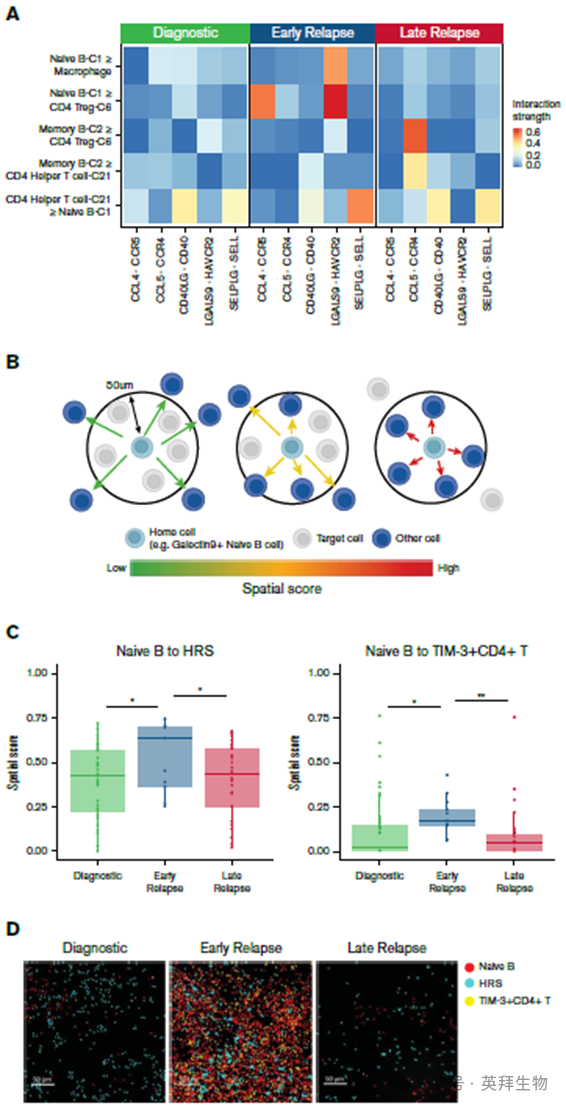
图4 在早期复发CHL中naïve B细胞和Treg细胞的互作分析
本研究通过单细胞RNA测序系统解析了经典型霍奇金淋巴瘤的肿瘤微环境,并揭示了早复发患者与晚复发患者之间显著不同的免疫特征。研究最重要的发现是:早复发患者肿瘤微环境中存在明显的naïve B细胞富集现象,同时伴随免疫调控分子LGALS9的高表达。这一结果提示,B细胞分化状态的改变可能是影响cHL复发时间的重要因素,而未成熟B细胞可能通过免疫调节机制促进肿瘤免疫逃逸。
参考文献:
Yin Y, Rai S, Jiang A, Xu A, O'Brien L, Telenius A, Delabie J, Chong L, Hung S, Merchant A, Scott DW, Savage KJ, Aoki T, Steidl C. Tumor microenvironment differences between diagnostic and relapsed classic Hodgkin lymphoma revealed by scRNA-seq. Blood Adv. 2026 Jan 13;10(1):29-38. doi: 10.1182/bloodadvances.2025017107. PMID: 40924921; PMCID: PMC12803924.






