颠覆性发现:阿尔茨海默病不仅是大脑的问题,眼睛里的慢性感染同样致命
肺炎衣原体是一种与阿尔茨海默病(AD)相关的胞内细菌,但其在视网膜病理及疾病进展中的作用尚不明确。本研究在视网膜中鉴定出肺炎衣原体包涵体,其在AD患者视网膜和脑组织中的负荷更高,且随APOEε4基因型、疾病阶段及认知缺陷程度增加而升高。视网膜和皮层蛋白质组学分析揭示了细菌感染及相关的NLRP3炎症小体通路。视网膜NLRP3在轻度认知障碍(MCI)中升高,在AD痴呆中激活,表现为caspase-1、裂解型白细胞介素-1β及裂解型N端gasdermin-D水平增加。肺炎衣原体与β42淀粉样蛋白、炎症、凋亡、焦死及AD状态相关。在神经元培养及APPSWE/PS1ΔE9模型小鼠中,感染诱导β淀粉样蛋白沉积、炎性小体激活、神经炎症及神经毒性,慢性感染加剧认知功能损害。AD视网膜中病原体共定位的小胶质细胞减少,暗示清除功能受损。机器学习发现视网膜肺炎衣原体或NLRP3与β42淀粉样蛋白联合存在时可预测AD诊断及病程阶段。这些发现支持肺炎衣原体在疾病放大中的作用,并提出通过抑制NLRP3或基于抗生素的早期干预策略。该研究于2026年1月发表在《Nature Communications》,IF:15.7。
技术路线

主要研究结果:
1.肺炎衣原体在AD痴呆患者视网膜和脑组织中的负担加重
为探究肺炎衣原体感染及其与AD视网膜神经炎症和神经退行性变的关系,我们分析了104名患者的视网膜和脑组织样本:其中51例为AD痴呆患者(平均年龄±标准差:85.90 ± 10.06岁,女性29例/男性22例),16例AD相关MCI(平均年龄89.43 ± 6.90岁,女性7例/男性9例),以及37例认知正常对照组(平均年龄83.96 ± 10.96岁,女性21例/男性16例)。各组间年龄、性别及死后间隔时间无显著差异。用于视网膜及脑组织病理学与生化分析的捐献者队列的人口统计学、临床及神经病理学特征汇总见图1A、表1及补充表1-5。为探究与肺炎衣原体感染相关的蛋白表达谱,我们重新分析了近期发表的人类视网膜及皮质组织质谱(MS)蛋白组学数据集。视网膜样本同步进行了Western blot和基因组DNA定量PCR检测。免疫组织化学(IHC)分析重点关注上颞部(ST)视网膜和背外侧前额叶皮层(A9),因其与AD病理密切相关。同时,我们考察了肺炎衣原体感染是否会调节人源神经元细胞及AD⁺小鼠(n = 45)中AD相关病理进展。
我们采用逐步策略来确定肺炎衣原体在人类视网膜中的存在与分布。首先,通过IHC使用经肺炎衣原体、沙眼衣原体和鹦鹉衣原体验证的抗衣原体多克隆抗体(pAb)进行广泛筛查,该抗体可与上述物种发生交叉反应。使用该抗体时,通过荧光免疫标记(图1B;n = 6)和过氧化物酶免疫标记(补充图1A、B;n = 6)均可清晰观察到衣原体阳性包涵体。随后采用不与其他衣原体物种发生交叉反应的抗肺炎衣原体单克隆抗体(mAb),通过过氧化物酶法(n = 18)和荧光法(n = 69)检测(图1C、D及补充图1C、D),在视网膜横切面中确认了肺炎衣原体包涵体的特异性存在。本研究中所有关于肺炎衣原体负荷的定量分析(包括阳性细胞计数、免疫反应性区域测量及相关性分析)均基于该肺炎衣原体特异性单克隆抗体。与认知功能正常对照组相比,MCI及AD患者视网膜在视网膜神经节细胞层(GCL)和内核层(INL)呈现显著的肺炎衣原体阳性信号。大多数肺炎衣原体包涵体表现为胞质点状聚集物,而其他包涵体则见于核周区域或细胞核内,并与DAPI染色呈共定位,其形态与抗衣原体多克隆抗体检测到的模式相似。在AD患者对应的A9皮层区域,单克隆抗体同样检测到肺炎衣原体包涵体(补充图1C、E),其形态特征与先前报道的AD脑组织包涵体模式一致,属于典型的细胞内包涵体。
为量化视网膜中肺炎衣原体的负担,我们首先进行了基于细胞计数的分析,结果显示与正常认知组和MCI组相比,AD组视网膜中肺炎衣原体阳性细胞分别增加了2.1倍和1.9倍(图1E;p < 0.001–0.0001)。此外,我们通过分析视网膜及配对脑组织中肺炎衣原体的免疫染色面积,以获取更综合的细菌负荷指标,结果显示AD患者的肺炎衣原体包涵体面积较正常认知对照组显著增加2.9倍和4.1倍(图1F;p < 0.0001;视网膜:n = 69,脑组织:n = 16)。两项分析结果一致(图1E、F):正常认知组与MCI组间肺炎衣原体负荷无显著差异,表明该病原体感染扩散可能发生于AD临床痴呆阶段的疾病晚期。事实上,视网膜和脑组织中肺炎衣原体水平的高斯分布曲线显示,正常认知组与MCI组之间存在显著重叠,而AD组则明显分离(补充图1F、G)。然而,在MCI患者中,视网膜或脑组织中肺炎衣原体水平超过正常认知组均值(红线)的比例为60%–79%,AD痴呆患者中该比例达100%,而正常认知组仅为38%–40%(图1F)。视网膜肺炎衣原体空间分布分析显示,中央(C)、中周(M)及远周(F)视网膜色素上皮亚区存在均匀分布的病原体负荷(补充图2A、B)。在任何诊断组内,男性与女性的视网膜肺炎衣原体水平均无差异(补充图2C),表明视网膜感染负担不存在性别特异性差异。
通过三种互补的组织学和分子学方法进一步验证了肺炎衣原体在人类视网膜中的存在:吉姆萨染色、荧光原位杂交(FISH)以及实时定量PCR检测基因组DNA(图1G–I;补充图3–4)。尽管吉姆萨染色并非特异性识别特定细菌种类,但视网膜横切面中的包涵体呈现深蓝色结构,与肺炎衣原体感染小鼠肺组织中的观察结果一致(图1G及补充图3A、B; n = 8例供体),且与AD视网膜及脑组织中经抗体免疫染色鉴定的肺炎衣原体包涵体特征一致(图1C、D)。采用荧光标记的肺炎衣原体特异性DNA探针进行的FISH分析进一步证实了该细菌基因组物质存在于视网膜组织中(图1H及补充图4;n = 11名供体),而在未添加探针的AD视网膜及正常认知组织中未检出。吉姆萨染色与FISH分析均显示,AD视网膜中的包涵体负荷高于正常认知个体。值得注意的是,定量PCR分析在2例AD病例的视网膜组织中检测到肺炎衣原体特异性精氨酸抑制因子(argR)基因,而1例MCI病例和2例正常认知对照组中均未检出,证实肺炎衣原体存在于人类视网膜中(图1I;n = 5名供体)。此外,视网膜与对应脑区肺炎衣原体负荷间的皮尔逊相关系数(r)显示,中枢神经系统(CNS)组织中细菌负荷存在高度一致性(图1J;rp = 0.62,p = 0.0143);在视网膜亚区域与大脑间进行的扩展相关性分析显示,中周边部区域呈现最强关联性(补充图5A、B;rp = 0.71,p = 0.0046)。
鉴于视网膜与脑部肺炎衣原体负荷存在显著关联,我们进一步探究了该细菌负荷与中枢神经系统组织中AD相关病理及疾病严重程度的关系。研究发现视网膜肺炎衣原体负荷与视网膜β淀粉样蛋白亚型存在高度相关性(图1K及补充表8; Aβ42:rp = 0.63,p < 0.0001;Aβ40:rp = 0.65,p = 0.0014),但与细胞内Aβ寡聚体无相关性(补充表8),表明其特异性关联于细胞外斑块主导型Aβ42及血管主导型Aβ40异构体。视网膜肺炎衣原体负荷与视网膜tau病变标志物亦存在显著相关性,包括成对螺旋丝状体tau(PHF-tau)(rp = 0.54,p = 0.0085,图1L)、高磷酸化S396-tau(rp = 0.38,p = 0.0116)、 T22+寡聚tau蛋白(rp = 0.43, p=0.0040)及瓜氨酸化tau蛋白(CitR209: rp = 0.48, p = 0.0028;补充表8)。视网膜肺炎衣原体负荷量与视网膜AT8阳性磷酸化tau蛋白或MC-1阳性成熟tau蛋白缠结无显著关联(补充表8),亦与磷酸化位点S404、S396、 S199、S231或S214位点测定的p-tau/总tau比值(通过NanoString GeoMx数字空间分析技术在该队列子集中测定;补充图5C-G;n = 22名供体)。总体而言,这些数据表明肺炎衣原体包涵体存在于MCI和AD患者的视网膜中,主要分布于神经节细胞层和内层神经节细胞层,与淀粉样蛋白原性β淀粉样蛋白密切相互作用,并与某些视网膜tau蛋白同工型存在轻度关联,但与其他同工型无关联。
接下来,我们评估了视网膜肺炎衣原体负荷是否与AD相关脑病理、载脂蛋白E(APOE)ɛ4等位基因、疾病分期或认知缺陷程度存在关联(图1M–Q;补充图5H–J及补充表8)。我们发现视网膜肺炎衣原体与脑内神经原纤维缠结(NFTs)的严重程度显著相关(图1M;rs = 0.54,p < 0.0001),且在Braak分期晚期患者中其载量高出2.1-2.4倍(图1N;III-IV期或V-VI期患者中比0-II期患者高出2.1-2.4倍:p < 0.05-0.001,n = 60),表明肺炎衣原体参与了脑tau蛋白病变的进展。此外,视网膜肺炎衣原体负荷量与以下脑部病理显著相关:β淀粉样斑块(rs = 0.40,p = 0.0014)、ABC严重程度评分(rs = 0.54, p<0.0001)、神经纤维缠结(NT;rs = 0.37,p = 0.0033)、脑淀粉样血管病(CAA;rs = 0.35,p = 0.0057)、胶质增生(rs = 0.40,p = 0.0016)及脑萎缩(rs = 0.48,p = 0.0001;补充表8)。值得注意的是,无论是否确诊AD,APOE ɛ4等位基因携带者视网膜和脑部肺炎衣原体负荷均高于非携带者(图1O;p = 0.037,n = 37;及补充图5H;趋势性差异,p = 0.06,n = 13)。
常见细菌感染(如幽门螺杆菌、肺炎衣原体、伯氏疏螺旋体及螺旋体属梅毒螺旋体)此前已被证实与老年人认知功能衰退及痴呆风险增加相关。在本研究队列中,视网膜肺炎衣原体负荷与简易精神状态检查(MMSE)评分呈负相关(图1P,n = 47名捐献者;及补充图5I;rs=−0.53,p < 0.0001),临床痴呆评级量表(CDR)评分(图1Q; rs=−0.43,p=0.0010),以及蒙特利尔认知评估量表(MOCA)评分(补充图5J; rs=−0.56,p=0.0334; 补充表8),进一步证实了视网膜肺炎衣原体负荷与全球性认知障碍之间的关联。尽管队列规模有限(n=15),脑部肺炎衣原体负担仍与AD脑病理学指标显著相关,包括ABC评分、Braak分期、神经原纤维缠结、神经原纤维缠结、胶质增生及萎缩(补充表9;rs=0.60–0.77, p < 0.05–0.001),与脑淀粉样血管病变(CAA)评分呈中等关联但与Aβ斑块负担无关,且显著关联MMSE表现较差(rs = −0.73, p = 0.0043)。综合而言,这些数据将视网膜和脑部肺炎衣原体负担与APOE ε4状态、广泛性AD神经病理改变及整体认知衰退紧密关联。
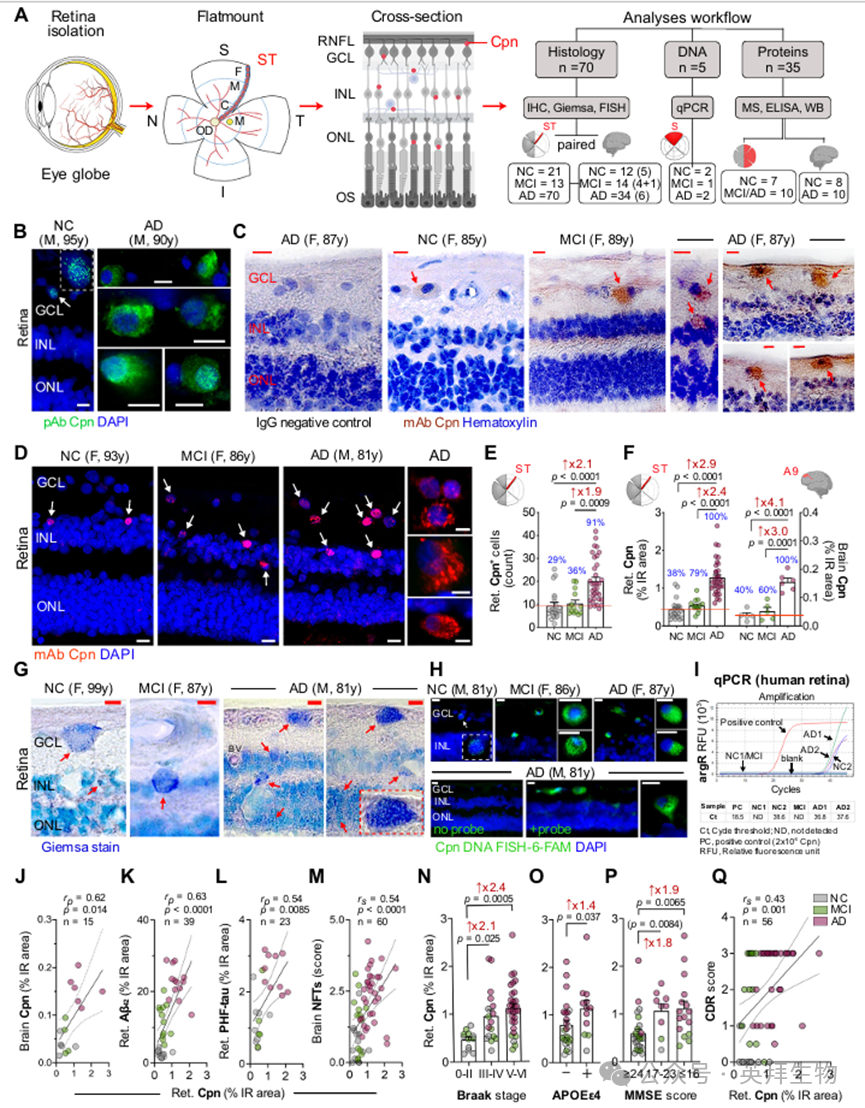
图1.MCI和AD患者视网膜和大脑中肺炎衣原体包裹体的鉴定及其与疾病状态的相关性
2.衣原体相互作用组与AD中的NLRP3激活及细胞死亡相关
在AD患者视网膜和脑组织中检测到革兰氏阴性肺炎衣原体包涵体,促使我们通过基于质谱的二次蛋白质组学分析,在独立的人类视网膜和皮质队列中探究感染驱动的蛋白质失调现象(补充表2-5;视网膜:n = 12,脑:n = 18)。Metascape基因本体论(GO)分析揭示,AD患者脑组织和视网膜中存在多种参与细菌感染应答(包括革兰氏阴性细胞内细菌)的异常调控人类蛋白(图2A、B),表明细菌感染在AD发病机制中具有重要作用。为深入探究衣原体感染机制,我们筛选了AD与正常认知组脑组织及视网膜中差异表达蛋白(DEPs),并将其纳入衣原体相互作用组分析(图2C、D;上调/下调DEPs详见补充数据表10和11)。在衣原体相互作用网络中的787种蛋白质48-52中,有607种在人类大脑中被鉴定出来,其中84种在AD患者与认知正常对照组相比呈差异表达(52种下调,32种上调;占比13.8%)(图2C)。值得注意的是,尽管源自不同队列,AD视网膜中仍发现了相似的细菌感染相关通路(图2A、B)及畸变的衣原体相互作用网络差异表达蛋白(图2D及补充图6A),在710个鉴定差异表达蛋白中包含52个下调蛋白和40个上调蛋白(占差异表达蛋白总数的13.0%)(图2D)。GO网络分析进一步揭示,AD脑组织和视网膜中富集了参与微生物免疫应答和细胞死亡的蛋白质(图2E、F,补充图6B-D及补充图7A-C)。炎症相关蛋白主要关联于细胞因子信号传导、Toll样受体(TLR)通路、干扰素反应、核因子κB(NF-κB)激活、NLRP3炎症小体激活及焦死亡等通路——这些通路通常由革兰氏阴性菌在周围组织中触发。这些数据表明AD脑组织与视网膜存在共同的感染及免疫相关机制。
研究表明,衣原体可触发宿主的先天免疫反应,该过程需要TLR2/MYD88信号通路及NLRP3/ASC/caspase-1炎症小体激活。事实上,在AD视网膜中,MYD88先天免疫信号转导适配体(MYD88)和含PYD及CARD结构域蛋白(PYCARD或ASC)均呈现上调(图2F)。此外,DNA病原体传感器及衣原体相互作用蛋白——富含亮氨酸重复序列结合FLII相互作用蛋白1(LRRFIP1)——通过与FLII肌动蛋白重塑蛋白(FLII)竞争与MYD88的结合来正向调控TLR4,该蛋白在AD脑组织和视网膜中均呈上调(图2F及补充图6A)。值得注意的是,视网膜AD蛋白组富集了与焦死相关的蛋白(图2E及补充图6B、D),这种炎症调控性坏死由细胞内病原体(包括衣原体)触发。值得注意的是,参与焦死/坏死过程的gasdermin(GSDM)家族成员GSDMD、GSDME(或DFNA5)和GSDMA33在AD视网膜中均呈上调(图2F)。参与凋亡、焦死和炎症的蛋白质普遍与质谱测定的脑部和视网膜tau异构体水平相关,并与酶联免疫吸附试验(ELISA)测定的视网膜Aβ1-42水平相关(补充图7D–H和8A–J)。值得注意的是,视网膜中Aβ1-42水平与多种与细胞退化相关的蛋白质呈强至极强的相关性,包括Casp3(相关系数rp = 0.77,p = 0.0099)、Bcl-2相关衰亡因子3(BAG3,rp = 0.76,p = 0.012) GSDMD(相关系数rp = 0.89,p值 = 0.0006),以及炎症调节因子如皮肤素(Dermcidin,DCD,相关系数rp=0.78,p值 = 0.0084)和LRRFIP1(相关系数rp=0.81,p值=0.0046)(补充图8A-E)。相反,细胞保护性与抗炎蛋白(如硫醇甲基转移酶1A(TMT1A,rp =-0.77,p = 0.015)和适配蛋白复合物2α2亚基(AP2A2,rp =-0.88,p = 0.0008))则与视网膜Aβ1-42呈负相关。与视网膜淀粉样变性类似,衣原体相互作用组蛋白也与视网膜(0N4R)tau异构体及脑部(1N3R、2N4R)tau异构体呈现显著关联(补充图8F–J及7G、H)。尤其值得注意的是,视网膜0N4R型tau蛋白与GSDMD(相关系数rp = 0.65,p = 0.022)、BAG3(rp = 0.85,p = 0.0005)、RAD23核苷酸切除修复蛋白B(RAD23B,rp = 0.90,p < 0.0001)、 LRRFIP1(相关系数rp = 0.81,p = 0.0015)、钙蛋白酶抑制剂(CAST,rp = 0.91,p < 0.0001)及TMT1A(rp = -0.92,p < 0.0001;补充图8F–J)。总体而言,这些发现表明AD脑组织和视网膜中富集了参与细胞内革兰氏阴性细菌感染的蛋白质(包括衣原体相关蛋白),同时存在炎性小体激活和退行性病变的特征性标志物。
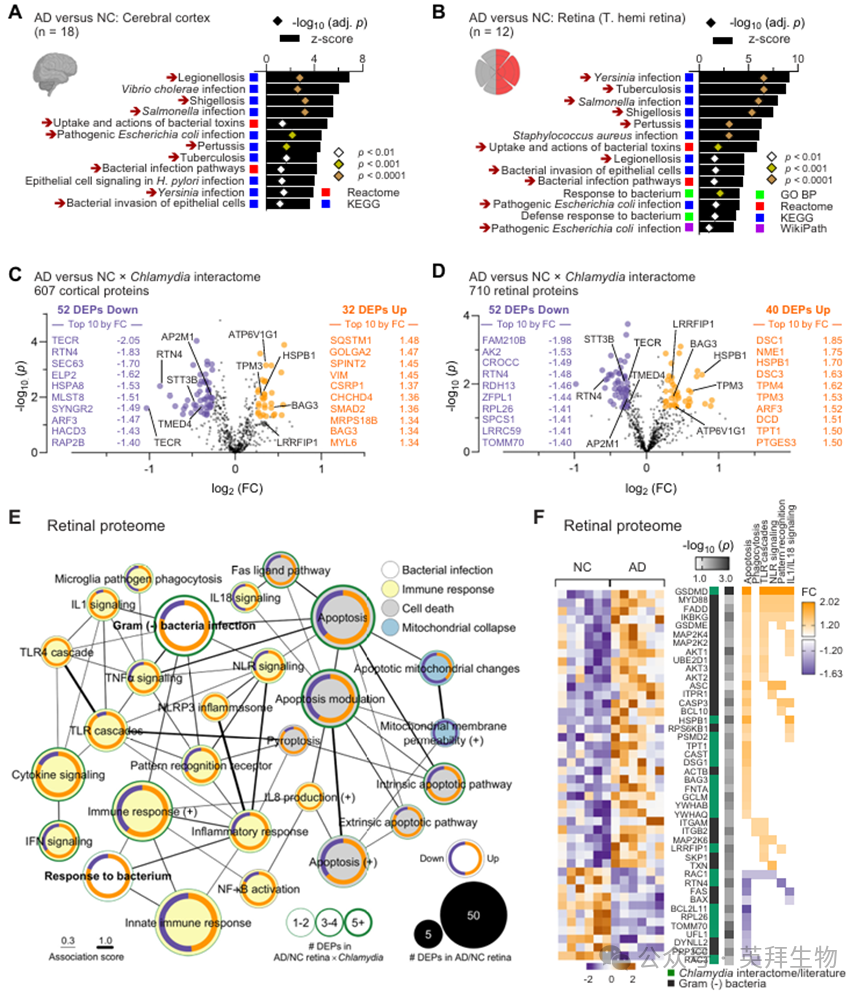
图2.AD视网膜和大脑皮层中细菌感染相关的蛋白质组通路
3.肺炎衣原体驱动AD病理并加剧认知功能衰退
为确定肺炎衣原体在AD中是否扮演驱动者而非旁观者角色,我们进一步验证神经元细胞及AD转基因小鼠感染该病原体是否足以触发炎性小体激活并加剧AD相关病理变化。将SH-SY5Y人神经母细胞瘤细胞感染肺炎衣原体(感染复数[MOI]为5)68小时后,显著诱导了Aβ42、NLRP3和IL1β水平,并通过乳酸脱氢酶(LDH)释放检测到细胞膜损伤(图3A-F)。免疫细胞化学证实肺炎衣原体对SH-SY5Y神经元具有强感染性,且感染细胞相较未感染对照组显示:NLRP3表达量升高2.5倍,IL1β升高3.2倍,H31L21+ Aβ42免疫反应区域扩大3.5倍(均p < 0.0001;图3B、C;补充图9A;每组条件n = 6孔,每组细胞数n = 41-74)。此外,通过检测培养基中乳酸脱氢酶(LDH)释放量发现,感染神经元细胞的LDH渗漏量较未感染对照组显著增加3.9倍(图3D,p < 0.001,每组6孔),表明肺炎衣原体感染可诱发神经毒性。通过Western blot分析进一步验证了上述发现:与对照组相比,感染神经元中NLRP3、裂解型IL1β(1.5倍,p < 0.05)、 12F4+ Aβ42(6.7倍,p < 0.05)及N端裂解型gasdermin D(NGSDMD)水平显著升高(图3E,F;每组n = 3-6孔)。这些发现共同表明,肺炎衣原体感染足以驱动神经元细胞中NLRP3炎症小体激活、焦死性细胞死亡及Aβ42积累——这些正是AD病理特征的细胞表现。未来研究需阐明肺炎衣原体通过何种分子通路放大Aβ生成、维持炎症小体信号传导,并最终促进神经退行性病变。
这些体外观察促使我们研究急性及长期肺炎衣原体感染对APPSWE/PS1ΔE9(AD+)小鼠模型体内AD样病理及认知功能的影响(图3G–S)。在急性肺炎衣原体感染模型中,我们检测了8只磷酸盐缓冲盐水(PBS)处理的AD⁺对照组小鼠和14只感染组AD⁺小鼠(n = 22)。长期感染模型中,研究对象包括6只PBS处理的野生型(WT)小鼠、8只PBS处理的AD⁺小鼠及9只感染组AD⁺小鼠(n = 23)。经鼻腔接种肺炎衣原体(1×10⁶包涵体形成单位,IFU)后,AD⁺小鼠脑组织中细菌包涵体显著增多(图3G,H),该现象通过以下实验得到验证:与未感染小鼠相比,感染小鼠脑组织裂解液处理的HEp2细胞中肺炎衣原体IFU更高,且肺炎衣原体基因组DNA拷贝数增加(图3H)。感染肺炎衣原体7天后(急性期),感染AD⁺小鼠海马区及皮层中:离子化钙结合适配分子1(IBA1)⁺小胶质细胞增生达3.2倍,胶质纤维酸性蛋白(GFAP)⁺星形胶质细胞增生达2.5倍(图3I,J;p < 0.05–0.01;补充图9B–D),表明感染导致神经炎症反应增强。此外,感染AD⁺小鼠的Il6(p < 0.01)、Il1β(p < 0.05)及Nlrp3(p < 0.01)mRNA表达水平显著升高(图3K),进一步支持NLRP3炎症小体信号通路在肺炎衣原体感染中的激活作用。这些发现表明,急性鼻腔感染足以使肺炎衣原体到达大脑,建立感染,并随后触发炎症小体激活和神经炎症。
在AD⁺小鼠8月龄时进行单次鼻腔接种(1×10⁶ IFU肺炎衣原体或PBS)后6个月,评估了肺炎衣原体感染对小鼠行为及病理的长期影响(图3L–S;补充图9E–J)。在14月龄小鼠中进行了为期12天的多领域行为测试,以PBS处理的野生型动物作为健康行为对照组。开放场和X迷宫测试显示,肺炎衣原体感染未影响AD⁺小鼠的运动功能,这体现在站立活动、行走活动及臂架进入总次数上(图3L及补充图9E、H)。然而,在评估视觉认知功能的X型迷宫测试中(该功能在AD+小鼠中本已减弱),肺炎衣原体感染进一步削弱了小鼠在色彩与对比度刺激模式下的表现(图3M、N)。在色彩模式X迷宫中,感染虽未影响特定臂部进入次数,但显著降低感染AD+小鼠在蓝色(B)↔白色(W)臂间的双向转换频率,表明存在色彩视觉功能障碍(图3M及补充图9F,G)。在对比度模式X迷宫实验中,PBS对照组AD+小鼠对白色物体所在臂的进入次数增加,而肺炎衣原体感染的AD+小鼠该指标进一步升高(图3N及补充图9I)。感染的AD+小鼠还表现出黑色(B)↔白色(W)双向转换增加,黑色(B)↔透明(C)双向转换减少,表明感染导致对比敏感度视觉恶化(补充图9J)。在巴恩斯迷宫实验中,PBS对照组AD+小鼠(相较于野生型)在找到逃生箱前、4天习得阶段、长期记忆保持阶段及2天逆转阶段均出现显著更多错误(图3O)。值得注意的是,AD+小鼠感染肺炎衣原体后,在第9天逆转测试中(该测试衡量空间学习与认知灵活性)的错误次数进一步增加(图3O,P)。搜索覆盖率分析显示,肺炎衣原体感染的AD+小鼠在新旧逃生箱位置两侧区域的局部错误率更高(图3P)。这些结果表明,长期肺炎衣原体感染会加剧AD⁺小鼠的视觉认知功能障碍,但不影响运动功能。
随后我们对比了长期感染与未感染AD⁺小鼠皮层及海马区的AD相关病理变化(图3Q–S)。分析显示,与PBS处理的AD⁺小鼠相比,肺炎衣原体感染的AD⁺小鼠皮层中:6E10+淀粉样斑块显著增加(1.6倍,p < 0.001),IBA1+小胶质细胞显著增多(1.3倍,p < 0.01)• GFAP+星形胶质细胞显著增多(1.3倍,p < 0.05)(图3R)。海马区亦呈现类似增长(图3S)。这些发现表明,AD⁺小鼠长期感染肺炎衣原体可加剧神经胶质细胞活化及Aβ病理变化,支持慢性感染会恶化类AD神经病理的假说。
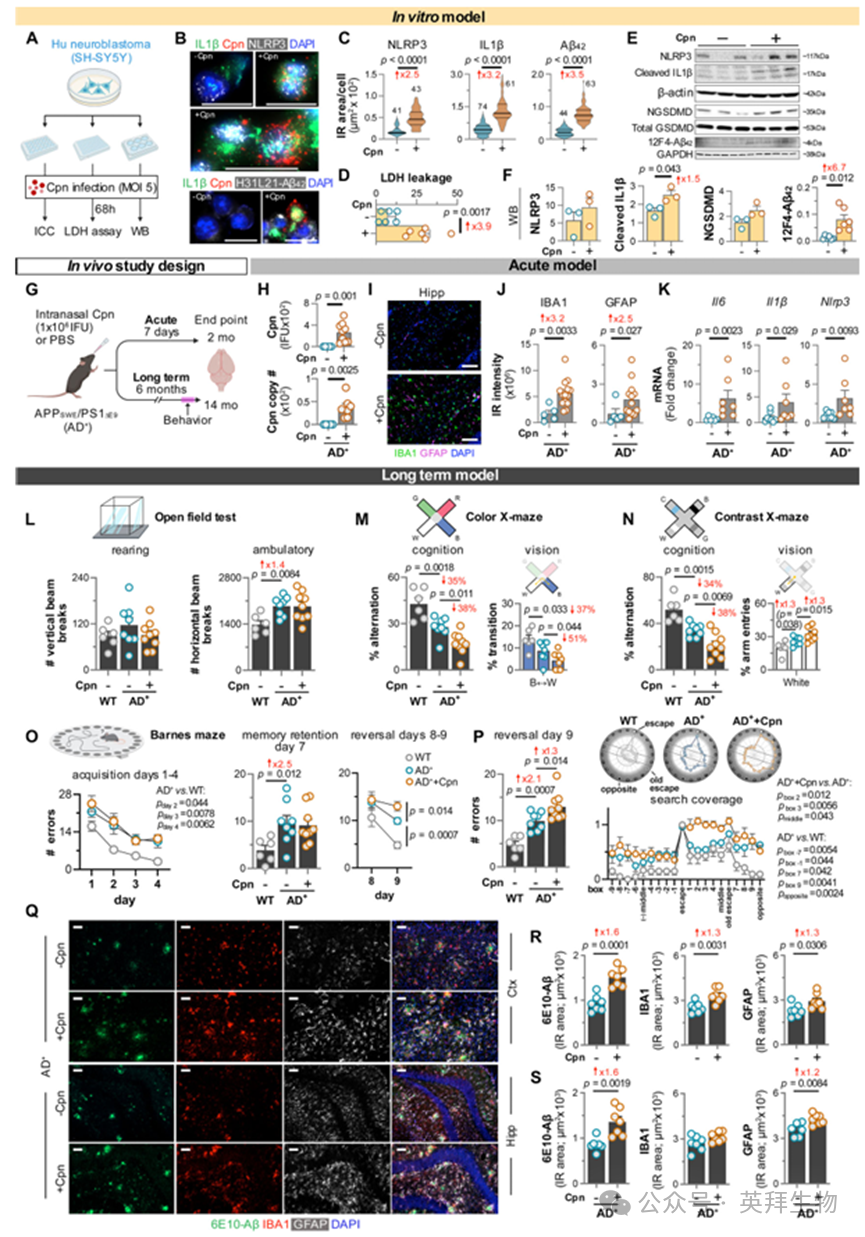
图3.肺炎衣原体感染对SH-SY5Y细胞及AD+小鼠的影响
4.视网膜NLRP3激活将肺炎衣原体与细胞死亡联系起来
基于质谱的蛋白质组学、肺炎衣原体感染细胞培养及AD+小鼠模型提供的多方证据,均表明该病原体可激活脑内NLRP3炎症小体。结合先前小鼠感染研究证实肺炎衣原体可驱动NLRP3激活,我们进而验证类似的炎症小体通路及相关细胞死亡机制是否存在于人类AD视网膜中。为此,我们首先对源自AD相关MCI及AD痴呆患者的视网膜横切面进行定量免疫组化分析,并与认知正常的匹配非AD个体进行比较(图4A-I;补充图10;n = 25-27名捐赠者)。与认知正常对照组相比,MCI患者视网膜NLRP3表达显著升高,AD患者进一步增加(分别升高2.1倍和3.6倍;p < 0.001-0.0001),并与caspase-1呈现强共定位——后者在AD中上调2.5倍,而在MCI中未见变化。这种炎性体激活特征伴随着肺炎衣原体相关的ASC斑点信号在AD中增加3.1倍,但在MCI中未见此现象(图4A-E;补充图10A、B)。NLRP3免疫反应性的早期升高及随后诱导的caspase-1和ASC标志物表达,可能表明NLRP3是由视网膜中错误折叠的Aβ和tau蛋白积累等早期过程激活的。
接下来,我们研究了视网膜中肺炎衣原体介导的NLRP3炎症小体激活对关键凋亡和焦死成分的影响。在AD视网膜中,肺炎衣原体感染细胞常同时表达焦死效应因子NGSDMD和早期凋亡标志物裂解型半胱天冬酶-3(CCasp3)(图4F-I;补充图10C、D)。定量免疫组化分析显示,与认知正常对照组相比,AD视网膜中NGSDMD和CCasp3信号分别显著升高2.2倍和3.0倍(p < 0.001–0.0001),而MCI视网膜仅呈现非显著性升高趋势(图4G,I)。多数肺炎衣原体阳性细胞同时表达焦死或凋亡标志物,表明AD视网膜中的肺炎衣原体感染同时激活两种细胞死亡通路。此外,AD视网膜中NGSDMD的显著增加为NLRP3炎症小体介导的焦死激活提供了功能性证据。
随后评估了视网膜肺炎衣原体负荷、NLRP3炎症小体组分与细胞死亡标志物之间的相互关系(图4J;补充表12)。本队列的多变量相关分析显示,视网膜肺炎衣原体负荷与视网膜NLRP3炎症小体组分呈强至极强的关联性,尤其表现为:caspase-1(r = 0.87,p < 0.0001)、 NLRP3(r = 0.70,p < 0.0001)及ASC(r = 0.60,p = 0.0012)存在显著至极显著的相关性(图4J)。除与视网膜肺炎衣原体负荷相关外(补充表8),视网膜Aβ42及T22+寡聚tau均与NLRP3和caspase-1呈强至极强相关性(r = 0.60–0.81,p < 0.01–0.0001;补充表12),证实其作为视网膜NLRP3炎症小体潜在激活因子的作用。视网膜寡聚tau蛋白与凋亡及焦死标志物均呈显著相关,包括CCasp3(r = 0.80,p < 0.0001)和NGSDMD(r = 0.77,p < 0.0001),视网膜Aβ42同样与CCasp3(r = 0.77,p = 0.0003)和NGSDMD(r = 0.64,p = 0.0247;补充表12)呈显著关联。视网膜NLRP3炎症小体组分间存在显著相关性(r = 0.58–0.83,p = 0.0016–p < 0.0001;图4J),其中NLRP3与caspase-1关联最为紧密。三者均与CCasp3呈强至极强相关(r = 0.76–0.81,p < 0.0001),而NGSDMD凋亡与NLRP3关联最密切(r = 0.74,p < 0.0001),与caspase-1和ASC仅呈中等相关性(r = 0.57-0.58,p < 0.01;图4J及补充表12)。为评估NLRP3炎症小体激活的经典下游效应器,我们通过Western blot技术测定AD患者与正常认知对照组视网膜匀浆中的促炎细胞因子IL-1β水平。与炎性体激活一致,AD视网膜呈现显著的促IL-1β向活性裂解形式的转变:促IL-1β水平显著降低49.8%,成熟IL-1β水平显著升高2.1倍(图4K;p < 0.01-0.001,n = 10供体)。综合上述发现,揭示了肺炎衣原体、Aβ42及寡聚tau蛋白共同激活视网膜NLRP3炎症小体通路,该通路通过促进IL1β成熟及诱导凋亡/焦死机制参与AD病理进程(总结见图4L)。
我们随后探讨了视网膜中肺炎衣原体相关的NLRP3炎症小体激活成分与视网膜萎缩、一系列脑部AD病理指标及临床结局之间的关联(图4M;补充表12和13)。视网膜NLRP3和caspase-1与视网膜萎缩严重程度呈极强正相关,该严重程度通过内界膜至外界膜的变薄指数量化(r = 0.82–0.86, p < 0.001–0.0001),并与全脑萎缩评分呈中度正相关(r = 0.41–0.47,p < 0.05)。视网膜ASC与视网膜萎缩呈强相关(r = 0.62, p = 0.0171),但与脑萎缩无关。视网膜肺炎衣原体负荷与视网膜萎缩呈强相关(r = 0.75,p < 0.0001),并与脑萎缩呈中等相关(r = 0.48,p < 0.001)。视网膜CCasp3与脑萎缩及视网膜萎缩均呈中度至极强相关(图4M;r = 0.45–0.86,p < 0.05–0.001),而NGSDMD仅与视网膜萎缩呈强相关(r = 0.60,p = 0.0247),与脑萎缩无关联。与视网膜肺炎衣原体类似,所有视网膜炎性小体组分及相关细胞死亡标志物均与Braak分期呈中度至高度相关(r = 0.55–0.72,p < 0.01–0.0001),并与MMSE认知表现呈负相关(图4M;r = –0.49至–0.69,p < 0.05–0.001)。这些关联共同表明,视网膜中的肺炎衣原体负担与NLRP3炎症小体活化是局部神经退行性病变及整体AD严重程度的综合指标。它们支持这样一种模型:病原体相关的视网膜炎症小体信号传导与并行发生的脑萎缩和认知衰退同步发展,并可能促成这些病理变化。
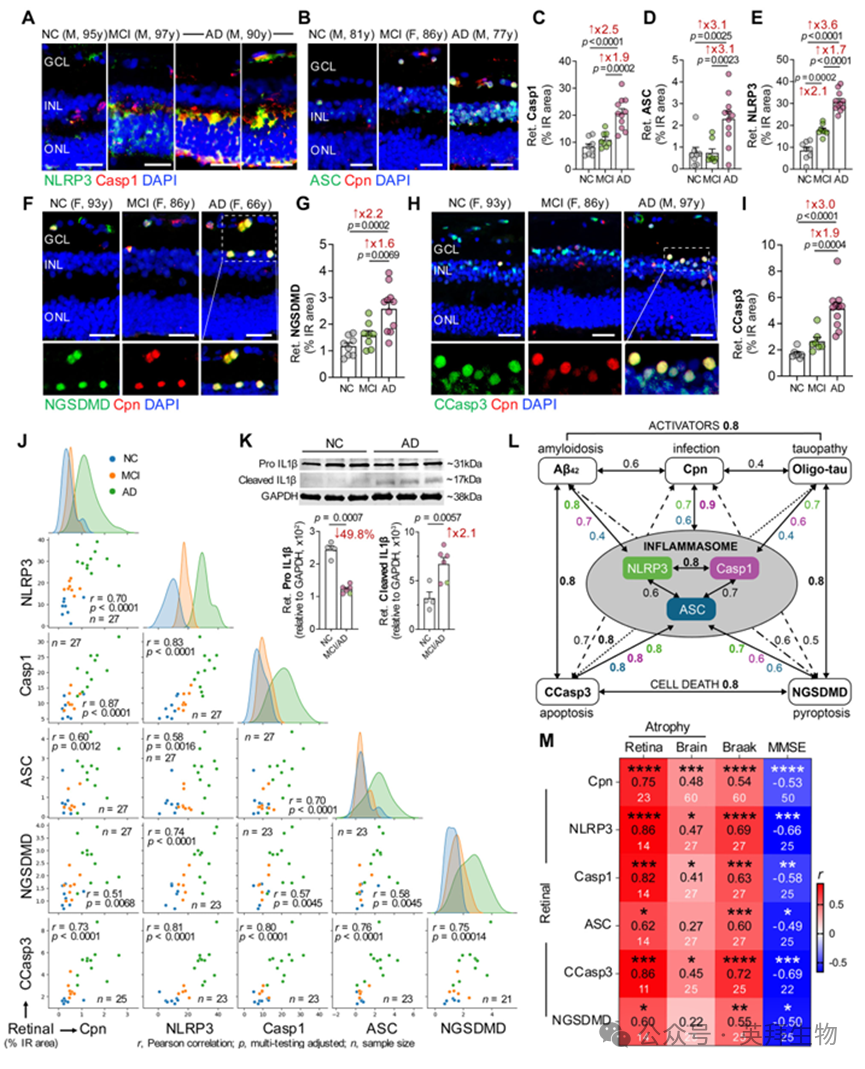
图4.视网膜NLRP3炎症小体、焦死及凋亡标志物与早期及晚期AD中肺炎衣原体感染的相关性
5.胶质细胞增生包围视网膜衣原体,伴随AD中吞噬作用的衰退
肺炎衣原体可感染星形胶质细胞和神经元并在其中大量复制,而小胶质细胞主要参与肺炎衣原体的吞噬作用。尽管包括我们自身在内的先前研究已证实MCI和AD患者视网膜存在显著的胶质增生,但这些患者视网膜中胶质细胞与肺炎衣原体之间的潜在相互作用仍未被探索。本研究观察到,在MCI和AD患者视网膜中,肺炎衣原体包涵体与视网膜小胶质细胞、星形胶质细胞及穆勒胶质细胞存在显著的空间相互作用,胶质细胞常围绕或吞噬含阳性细菌的包涵体(图5A-J;补充图11A、B;n = 21-32名供体)。定量免疫组化分析显示,AD视网膜中GFAP⁺星形胶质细胞和IBA1⁺小胶质细胞数量显著增加(1.5倍,p < 0.05–0.001),而MCI视网膜未见此现象(图5B、H)。值得注意的是,通过分析GFAP⁺和vimentin⁺巨胶质细胞以及IBA1⁺小胶质细胞的免疫染色面积(该指标兼顾细胞形态与突起肥大程度),发现所有胶质增生标志物在MCI视网膜中均显著扩张(1.5–1.9倍,p < 0.05–0.01),而AD视网膜相较于正常认知对照组呈现更显著扩张(2.3–2.8倍,P < 0.0001)(图5C、E、I;补充图11C–E)。这些发现表明,视网膜AD连续体早期即出现胶质细胞活化与突起肥大,随后在e期出现明显的胶质细胞增殖。
我们随后考察了视网膜细菌负荷是否与胶质增生负担呈正相关。视网膜肺炎衣原体负荷与GFAP⁺星形胶质细胞增生和IBA1⁺小胶质细胞增生呈显著相关(图5D、J;r = 0.65–0.70,p < 0.0001),并与波形蛋白⁺巨胶质细胞反应性呈中等相关(图5F;r = 0.55,p = 0.0090)。与上述视网膜相互作用一致,脑部肺炎衣原体负荷与脑胶质增生存在显著相关性(r = 0.77,p = 0.0008)。肺炎衣原体负荷与胶质增生间的强关联提示细菌感染可能引发慢性炎症级联反应。值得注意的是,视网膜星形胶质细胞似乎被肺炎衣原体直接感染,而视网膜小胶质细胞则呈现吞噬细菌包涵体或受感染细胞的特征(图5A、K)。具体而言,视网膜小胶质细胞对肺炎衣原体感染细胞呈现不同阶段的反应:多数细胞与衣原体阳性细胞紧密邻接并部分接触(识别阶段);另有小胶质细胞直接参与吞噬或摄取感染细胞(图5K)。与认知功能正常对照组相比,AD视网膜中肺炎衣原体相关小胶质细胞(CAM)计数比例增加50%,而MCI视网膜未见此变化(图5L;1.5倍,p < 0.01,n = 44供体)。然而,与认知功能正常的对照组相比,AD视网膜中视网膜CAM细胞计数与细菌载量的比值降低了61%(图5M; p < 0.0001, n = 44;补充图12A-C),表明AD视网膜中存在肺炎衣原体吞噬功能缺陷。为进一步验证肺炎衣原体相关IBA1⁺细胞确属驻留小胶质细胞而非血管周围或浸润性巨噬细胞,我们采用跨膜蛋白119(TMEM119)进行视网膜切片共标记——该标志物在人类大脑和视网膜的驻留小胶质细胞中富集(图5N,n = 12;补充图12D)。所有参与识别、吞噬或摄取肺炎衣原体包涵体的IBA1⁺细胞均共表达TMEM119,证实其小胶质细胞身份。我们将此类细胞命名为CAM细胞。视网膜CAM细胞占比与细菌负荷呈显著负相关(图5O;r = –0.72,p < 0.0001),且在认知正常个体中相关性更强(补充图12E;r = –0.79,p = 0.0004)。在认知功能正常组中,三名女性个体表现出与视网膜细菌负荷不成比例的低CAM百分比,其模式与AD中观察到的相似(图5M和补充图12E)。值得注意的是,这些个体还表现出最高的视网膜肺炎衣原体载量(图1F),且视网膜与大脑的AD相关病理水平相当,这表明即使在某些临床正常的个体中,小胶质细胞与细菌感染细胞的结合能力也存在选择性受损。综合这些数据表明,尽管AD视网膜中常驻小胶质细胞的募集增加,但其吞噬活性相对于细菌负荷明显降低,这与AD视网膜中微胶质细胞清除肺炎衣原体功能受损的现象相一致。
视网膜胶质增生与视网膜及脑部多种AD生物标志物之间的多重交互热图(图5P;补充表12和13)显示:视网膜GFAP+或vimentin+巨胶质细胞增生与NLRP3负荷存在极强关联(r = 0.84–0.91, p值 < 0.01–0.0001),以及视网膜GFAP+星形胶质细胞增生与CCasp3+凋亡(r = 0.85,p < 0.0001)之间存在显著关联。在淀粉样变性与tau病变方面,视网膜Aβ42及寡聚tau负荷与视网膜IBA1+小胶质细胞增生水平呈最密切相关(图5P;r = 0.69–0.85,p < 0.0001)。此外,视网膜GFAP+与Braak评分呈显著相关(r = 0.78,p < 0.0001)。这些发现表明视网膜胶质细胞与肺炎衣原体感染细胞之间存在密切相互作用,与NLRP3炎症小体成分及凋亡/焦死细胞死亡标志物高度相关,且阿尔茨海默病视网膜中微胶质细胞吞噬并清除肺炎衣原体感染的能力可能受损。
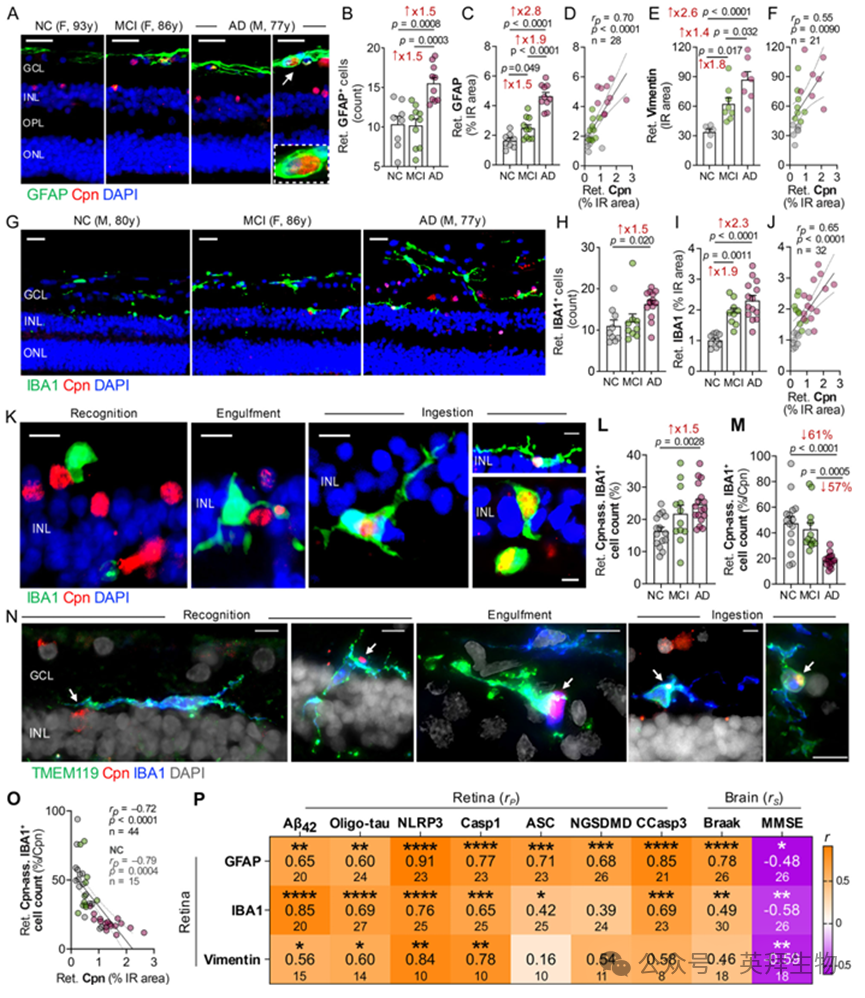
图5.MCI和AD视网膜中肺炎衣原体相关胶质细胞激活和吞噬
6.视网膜肺炎衣原体与NLRP3可预测AD诊断及病程阶段
我们随后验证了视网膜肺炎衣原体负荷及其相关标志物能否作为AD诊断、脑病理严重程度、疾病阶段及认知功能障碍的预测指标(图6;补充图13-15)。除视网膜肺炎衣原体外,我们纳入了与感染及AD病理显著相关的关键视网膜标志物,具体包括NLRP3、CCasp3-凋亡及Aβ42。这些标志物可单独分析,也可与视网膜胶质增生(IBA1+GFAP+vimentin)、萎缩和Aβ42组合分析;后者可在活体患者中成像。我们评估了 80 种生物标记物衍生的回归和分类估计器,采用诊断分层法将 56 名捐赠者(80%)用于模型训练,14 名捐赠者(20%)用于测试。采用随机森林机器学习模型的多变量分析表明,仅视网膜肺炎衣原体即可弱预测AD相关脑病理(包括ABC评分和Braak分期)(图6A、B),以及认知功能(MMSE,图6C;MOCA,补充图13B)。通过5×2交叉验证比较多种模型,以获得模型性能分布。当视网膜肺炎衣原体与视网膜Aβ42或胶质增生联合分析时,其预测能力普遍增强(图6A-C及补充图13A-E)。我们发现,仅视网膜Aβ42即可有效预测脑内神经原纤维缠结(NFTs)、ABC评分、Braak分期及简易精神状态检查(MMSE)评分(图6A-C及补充图13A)。值得注意的是,视网膜肺炎衣原体与胶质增生联合指数是预测ABC评分(图6A,r² = 0.34)和脑部胶质增生(补充图13E,r² = 0.26)的最佳指标。预测Braak分期最优的组合为视网膜Aβ42与CCasp3(r² = 0.41),其次为与NLRP3(r² = 0.38)及肺炎衣原体(r² = 0.28)的组合(图6B)。此外,视网膜NLRP3与Aβ42联合指数是预测MMSE评分的最佳指标(图6C,r² = 0.25),而视网膜Aβ42联合肺炎衣原体或CCasp3亦可预测MMSE(图6C,r² = 0.22–0.23),而单一标志物均无法预测脑萎缩(补充图13D)。
我们进一步通过受试者工作特征曲线下面积(AUC)评估了这些变量在疾病诊断中的性能(图6D–F及补充图14A–D;各诊断组的单独分析见补充图15A–D)。当与视网膜淀粉样病变(Aβ42)联合使用时,视网膜肺炎衣原体的AUC值从0.80升至0.94(图6D、E),尤其在区分MCI与正常认知诊断方面表现突出(图6D)。这些发现表明,视网膜肺炎衣原体与Aβ42的组合可能构成区分疾病状态的高效标志物对(图6F)。单独的视网膜Aβ42(AUC=0.87)在分类正常认知受试者时表现最佳(AUC = 0.92;补充图15D)。与随机森林模型结果一致,视网膜NLRP3、CCasp3及萎缩在疾病诊断中均表现出强劲的AUC值,与Aβ42联合使用时显著提升(分别为0.92、0.87和0.89;图6E及补充图14B-D),包括在各诊断组内(补充图15A-C)。基于图6E、F结果,我们选取肺炎衣原体与视网膜Aβ42联合模型对测试集进行评估(测试集包含认知正常/MCIAD诊断的3/4/7名患者);结果见表2。该模型对MCI(MCI)受试者的识别效果不佳,但在识别正常认知和AD方面表现尚可。我们注意到,在测试集中,正常认知组和MCI组的样本量不足。
我们进一步通过比较预测概率与临床疾病严重程度(评分0-3)来评估所选模型的性能,该严重程度基于生前CDR量表和MMSE认知表现评定。利用测试集,我们获得了每种诊断的预测概率,并将这些概率与疾病严重程度进行对比(补充图15E)。正常认知(r = -0.78)与AD(r = 0.79)的预测概率均与疾病严重程度呈高度相关。如预期所示,MCI预测与疾病严重程度无相关性。观察各诊断类别的预测概率可知,正常认知、MCI和AD的标准差分别为0.41、0.22和0.34。高确定性预测将导致更高标准差;MCI患者的预测确定性较低,表明通过增加训练样本或可提升该类别的可检测性。
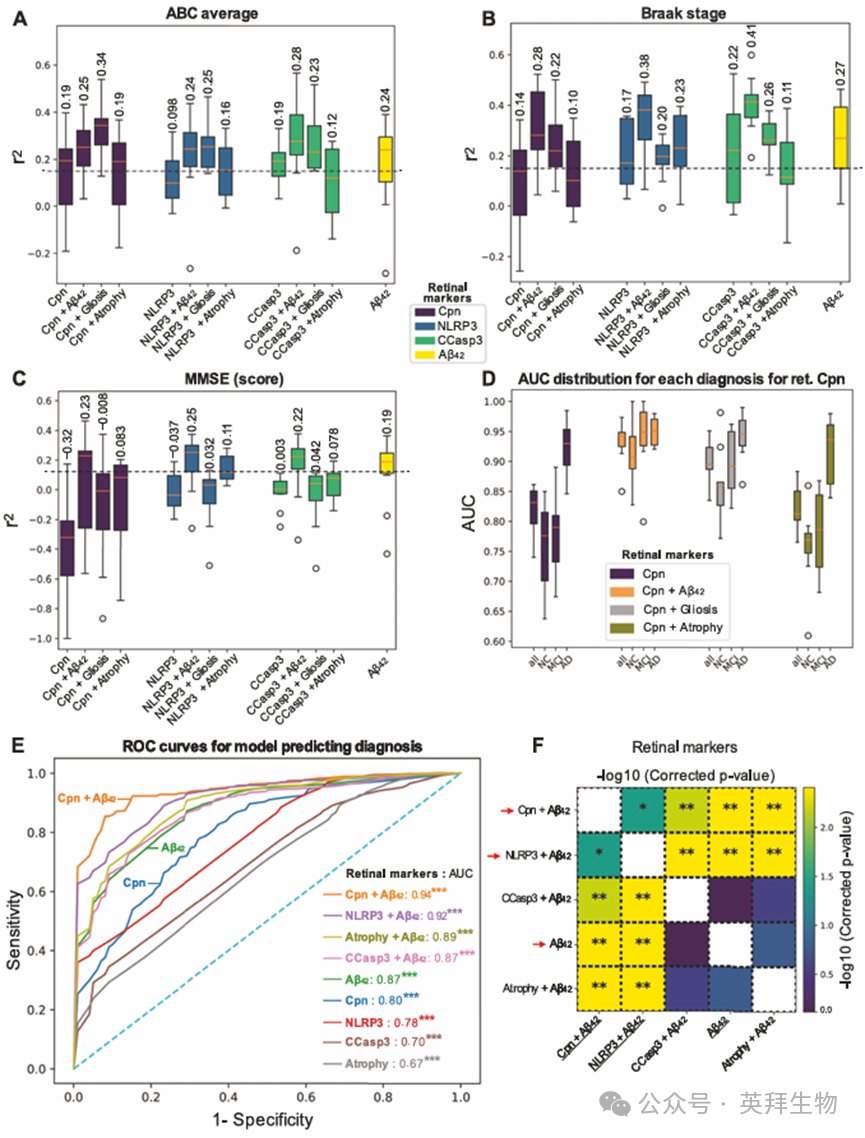
图6.
结论
综上所述,本研究在MCI和AD患者视网膜中鉴定并空间定位了肺炎衣原体,并揭示了细菌负荷与视网膜NLRP3炎症小体激活、胶质细胞损伤、神经退行性变以及相应脑病理改变和临床状态之间的关联。结合人类神经元培养及AD⁺小鼠模型的多方证据,本研究确立了肺炎衣原体作为AD病理与功能障碍的放大器地位,并强调针对病原体和NLRP3的干预策略——包括及时抗生素治疗及炎症小体调节干预——是可验证的疾病进展调控途径,同时加速开发可及性视网膜成像生物标志物以评估感染相关AD负担。
参考文献
Gaire BP, Koronyo Y, Vit JP, Hutton A, Subedi L, Fuchs DT, Swerdlow N, Rentsendorj A, Shahin S, Martinon D, Robinson E, Ljubimov AV, Schneider JA, Schneider LS, Hawes D, Graham SL, Gupta VK, Mirzaei M, Black KL, Meyer JG, Arditi M, Crother TR, Koronyo-Hamaoui M. Identification of Chlamydia pneumoniae and NLRP3 inflammasome activation in Alzheimer's disease retina. Nat Commun. 2026 Jan 22;17(1):771. doi: 10.1038/s41467-026-68580-4. PMID: 41571675; PMCID: PMC12827417.






