一种新的候选肿瘤抑制因子tRF-Ser通过调节CNBP/HSPA8轴抑制胃癌进展
胃癌(GC)是一种高度侵袭性的恶性肿瘤,预后较差。tsRNA与肿瘤发生有关,但其在GC进展中的确切机制仍不完全清楚。我们发现了一种新的tsRNA,tRF-Ser,在GC组织和细胞系中显著下调,其表达与有利的生存相关。在功能上,tRF-Ser通过抑制上皮-间质转化(EMT)、诱导铁死亡和增强对5-氟尿嘧啶化疗的敏感性来发挥肿瘤抑制作用。机制上,tRF-Ser直接与CNBP结合,促进其在细胞质中积累,阻止其与HSPA8启动子结合下调HSPA8。然后,tRF-Ser/CNBP/HSPA8轴通过抑制β-catenin核易位抑制EMT,并通过促进STUB1介导的GPX4泛素化降解促进铁死亡。我们的研究揭示了tRF-Ser/CNBP/HSPA8轴可能通过调节能量代谢来抑制GC的进展,这突出了靶向该轴治疗GC的治疗潜力。本文于2026年3月发表于 Cell Death and Disease(IF=9.6)上。
技术路线:

结果:
1)tRF-Ser 在胃癌中表达下调,并与良好的生存率相关
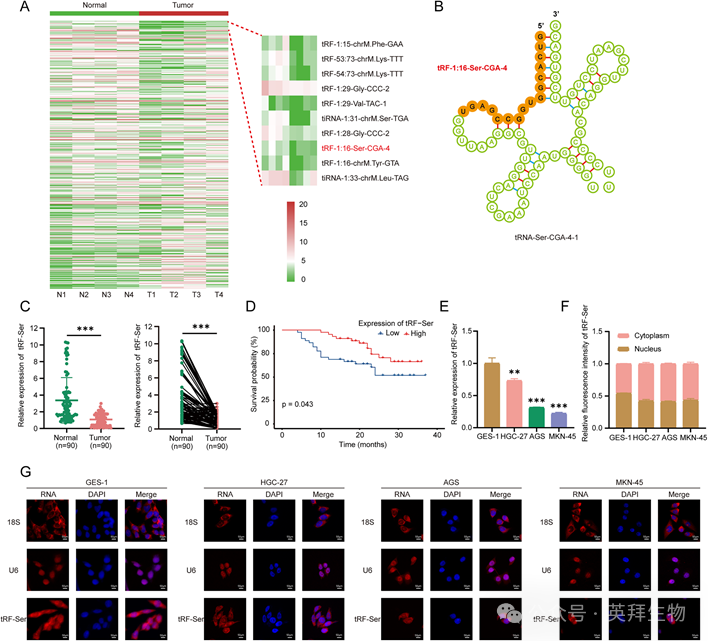
对四个配对的GC/相邻组织中的tRF /tiRNAs进行高通量测序,鉴定出一种新的5 '衍生的tsRNA,tRF-1:16-Ser- CGA-4(命名为tRF-Ser;图1A,B)。通过测序,GC组织中tRF-Ser显著下调(图1A),在我们中心的90例GC患者的独立队列中也观察到类似的结果(图1C)。在临床上,低tRF-Ser表达预示较差的总生存期(图1D)。与临床结果一致,与正常胃上皮细胞(GES-1)相比,多个胃上皮细胞(HGC-27、AGS和MKN-45)中的tRF-Ser减少(图1E)。亚细胞定位显示,GES-1细胞的核和细胞质分布占主导地位,但GC细胞的核信号明显减少(图1F,G)。综上所述,这些结果确定了tRF-Ser是GC中具有预后和治疗潜力的新型下调tsRNA。
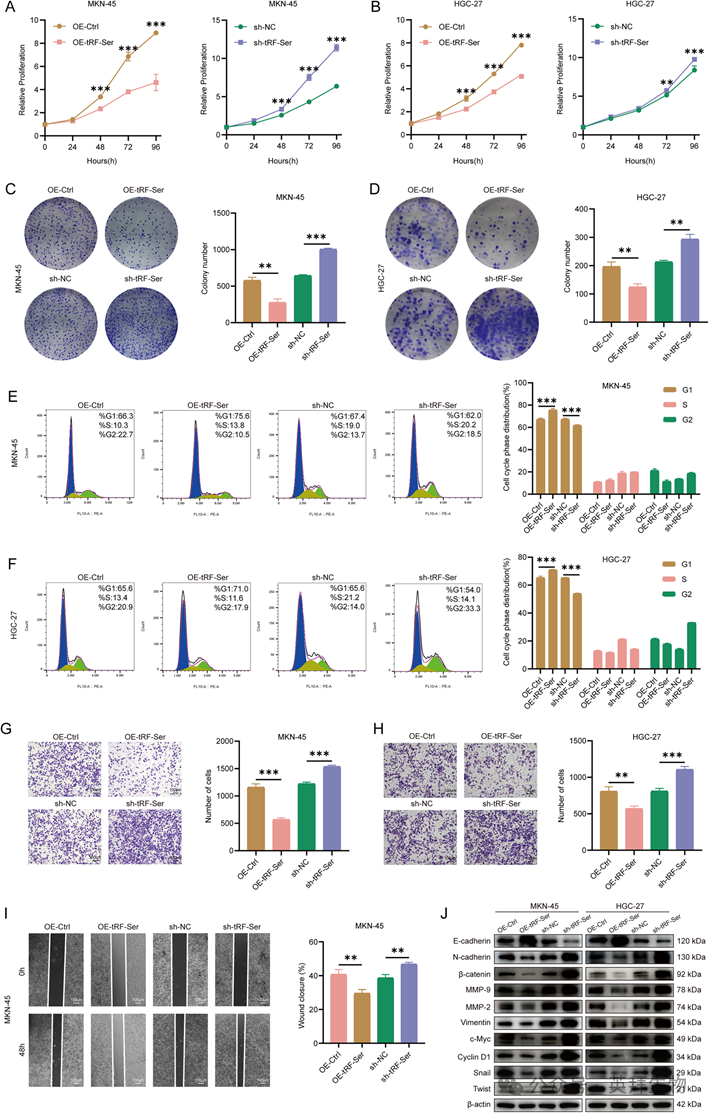
2)tRF-Ser在体外抑制GC进展
为了阐明tRF-Ser在GC进展中的生物学功能,我们使用MKN-45 (tRF-Ser的最低内源性表达)和HGC-27 (tRF-Ser的最高内源性表达)细胞系转染tRF-Ser模拟物或抑制剂和稳定的慢病毒过表达或敲低。tRF-Ser异位表达显著抑制细胞增殖(图2A-D),诱导G1期细胞周期阻滞(图2E,F),减少细胞侵袭和迁移(图2G-I),抑制EMT (图2J)。相反,tRF-Ser敲低促进了这些恶性活动。这些结果提示,在GC中,tRF-Ser可能是一个关键的肿瘤抑制因子。
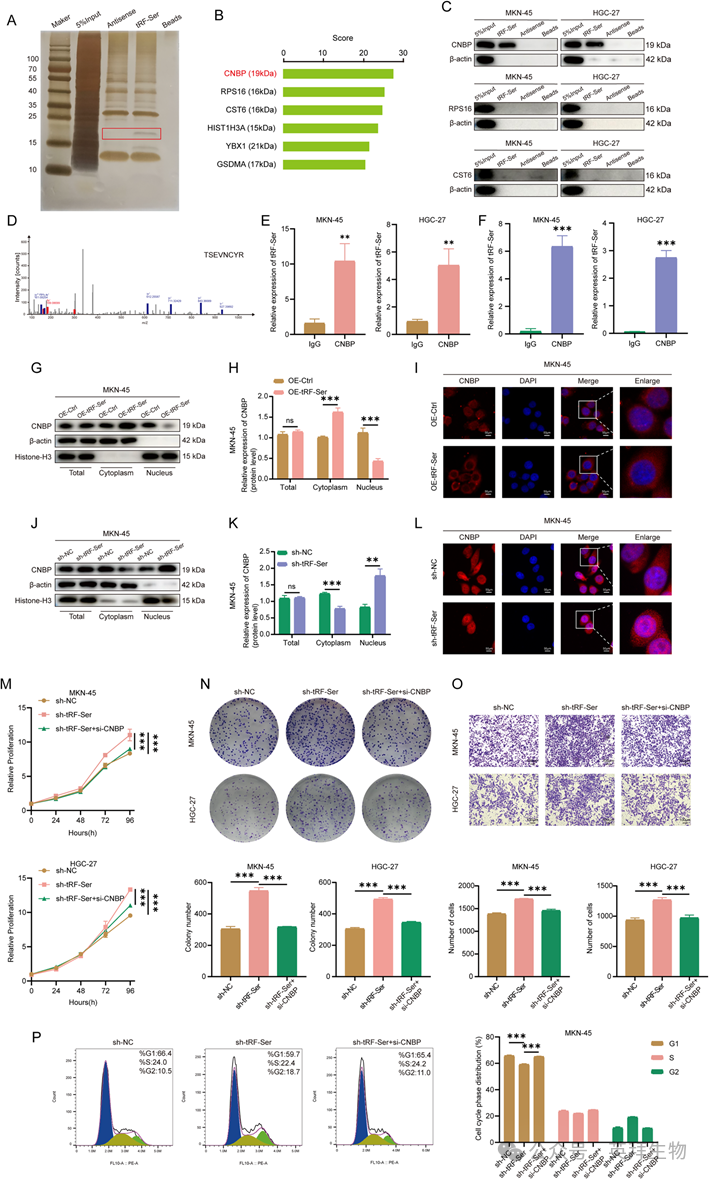
3)tRF-Ser与CNBP蛋白结合并调节其亚细胞定位
为了揭示tRF-Ser介导的GC抑制的潜在机制,我们采用RNA下拉结合银染色和质谱法来鉴定潜在的结合伙伴。在差异银染带对应的蛋白中,CNBP (19 kDa)的匹配评分最高(图3A-D)。然后,为了筛选可能与tRF-Ser相互作用的蛋白,我们根据候选蛋白评分的排名选择了CNBP、RPS16和CST6进行独立的RNA下拉实验。值得注意的是,只有CNBP被tRF-Ser拉,而非其反义RNA(图3C)。此外,tRF-Ser和CNBP之间的特异性相互作用通过RIP(图3E)和CLIP测定(图3F)核细胞质分离(图3G,H,J,K)和IF(图3I,L)检测显示,tRF-Ser表达与CNBP核积累负相关。tRF-Ser的过表达促进了CNBP在细胞质中的积累,而tRF-Ser的下调则增加了其在细胞核中的富集。为了功能性地询问GC中的tRF-Ser/CNBP轴,我们建立了CNBP过表达模型,并选择si-CNBP-2(表现出最高的敲除效率)进行拯救实验。CNBP敲低可有效逆转tRF-Ser敲低诱导的促癌作用,包括减少增殖/侵袭和加重G1阻滞(图3M-P)。结果提示tRF-Ser可能通过抑制CNBP的核定位来发挥其肿瘤抑制作用。
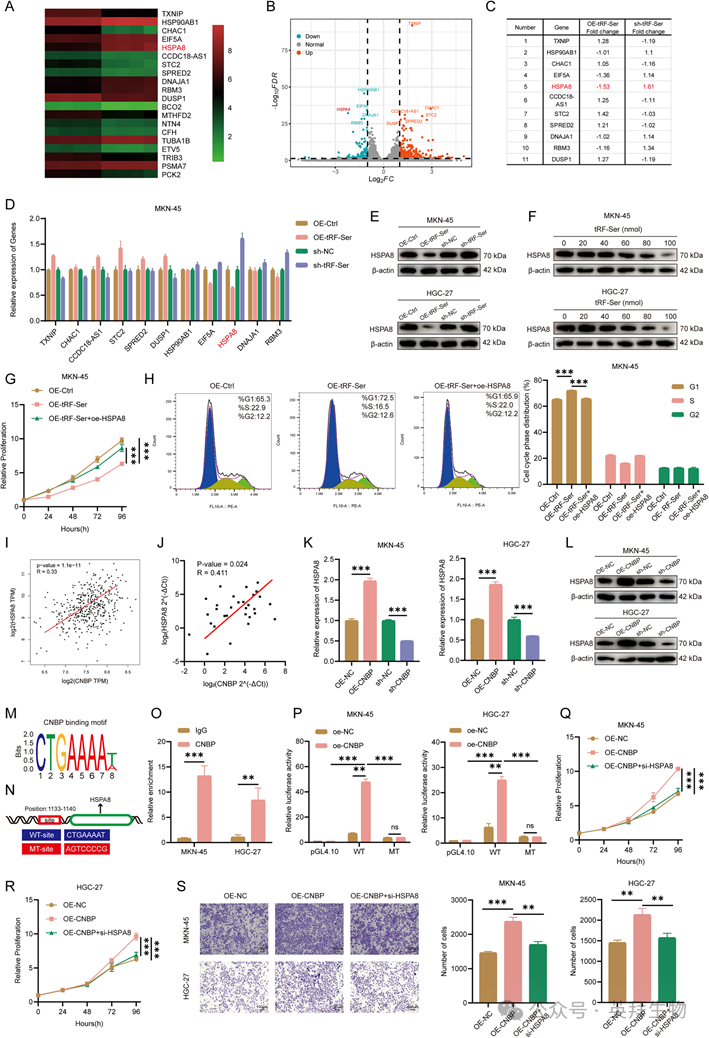
4)tRF-Ser/CNBP轴转录抑制HSPA8以抑制GC进展
为了进一步探索tRF-Ser的分子机制,我们对tRF-Ser过表达和对照处理的MKN-45细胞进行了RNA测序。热图(图4A)、火山图(图4B)和qRT-PCR分析(图4C、D)显示,在前11个候选基因中,HSPA8是调控最显著的靶基因,WB分析(图4E、F)也显示,tRF-Ser负调控HSPA8的表达。过表达HSPA8可有效逆转tRF-Ser过表达的肿瘤抑制作用,恢复细胞增殖、侵袭和细胞周期进程的能力(图4G,H)。这些发现表明,tRF-Ser可能通过靶向HSPA8抑制GC进展。鉴于我们的RNA-seq数据表明,tRF-Ser转录抑制HSPA8,我们假设这种作用是通过抑制CNBP核定位介导的。有几条证据支持这种机制上的联系。首先,生物信息学分析(GEPIA;图4I)和我们的数据(图4J)显示CNBP和HSPA8表达之间存在显著的正相关。其次,调节CNBP表达(通过过表达或敲低)相应地改变HSPA8 mRNA和蛋白水平(图4K,L)。第三,NCBI数据库分析显示HSPA8启动子区具有与CNBP识别基序高度匹配的序列(图4M,N)。这种相互作用在功能上得到了验证:ChIP-qPCR发现CNBP在HSPA8启动子中富集(图4O),双荧光素酶报告基因检测显示,CNBP过表达增强了WT荧光素酶活性,在MT中激活减弱(图4N,P)。最后,拯救实验证明了HSPA8在CNBP通路中的功能必要性。敲低HSPA8可有效逆转CNBP过表达的致瘤作用,抑制增殖和侵袭,诱导细胞周期阻滞(图4Q-S)。总的来说,tRF-Ser/CNBP轴转录抑制HSPA8以抑制GC进展。
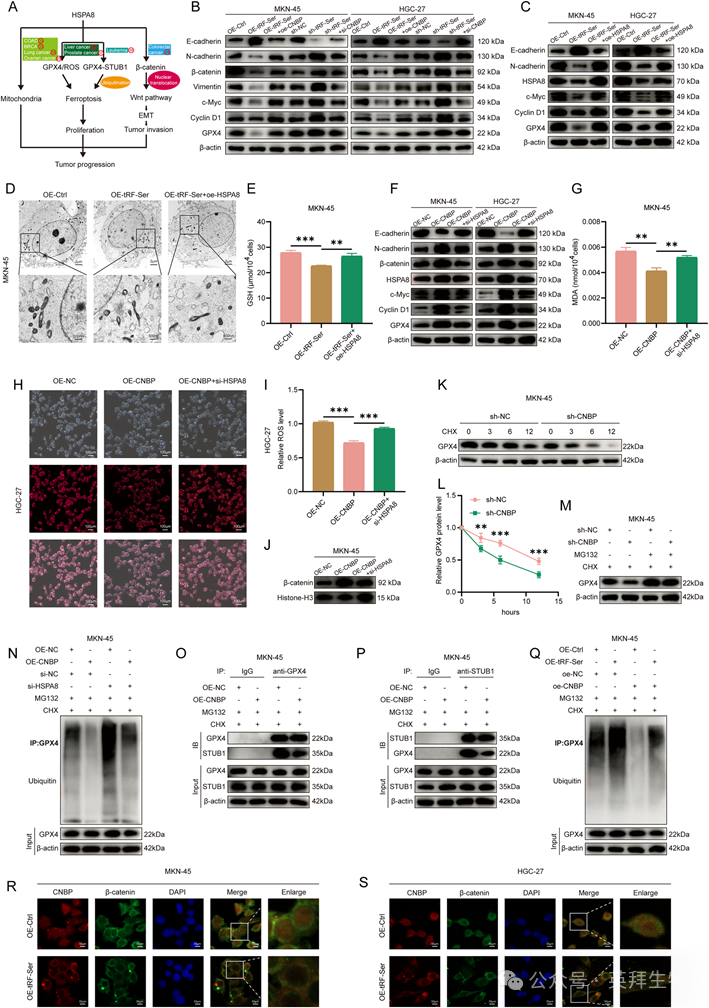
5)tRF-Ser/CNBP/HSPA8轴抑制GC进展
HSPA8作为调控肿瘤进展的关键基因,已被证明通过多种机制驱动恶性肿瘤(图5A)。在拯救实验中,CNBP敲低逆转了tRF-Ser敲低的作用,抑制EMT并促进铁死亡(图5B)。此外,HSPA8过表达逆转了tRF-Ser过表达引起的肿瘤抑制作用(图5C-E)。然后,HSPA8敲低阻断CNBP过表达的促肿瘤作用,抑制β-catenin核易位和EMT,同时促进铁死亡(图5F-J)。机制上,我们的结果表明,CNBP敲低缩短了GPX4蛋白的半衰期,蛋白酶体抑制剂MG132逆转了这一作用(图5K-M)。CNBP过表达抑制GPX4泛素化,HSPA8敲低可逆转这一作用(图5N)。此外,双向Co-IP分析显示,CNBP过表达破坏了STUB1和GPX4之间的结合(图5O,P)。最后,我们验证了整个tRF-Ser/CNBP/HSPA8调控轴。泛素化实验显示,CNBP过表达可逆转tRF-Ser诱导的GPX4泛素化(图5Q)。IF实验发现,tRF-Ser过表达抑制了细胞核中CNBP和β-catenin的积累(图5R,S)。
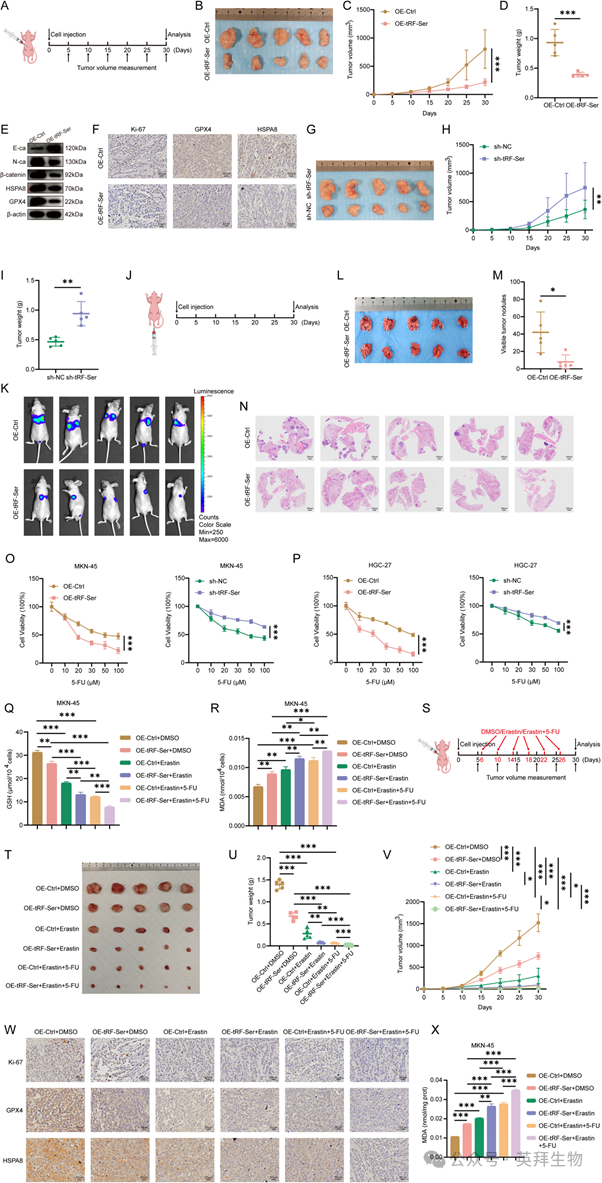
6)tRF-Ser在体内抑制肿瘤生长和转移,增强5-FU在GC中的敏感性
两种不同模型的体内功能研究表明,tRF-Ser发挥了其肿瘤抑制作用。首先,在皮下异种移植物中,tRF-Ser过表达显著损害肿瘤生长,减少肿瘤体积和重量(图6A-D),而其下调则增强肿瘤发生(图6G-I)。WB和IHC对这些异种移植物的分子分析显示,tRF-Ser过表达组的EMT标记物、GPX4和HSPA8下调(图6E,F)。其次,在肺转移模型中,tRF-Ser过表达可显著降低肺转移负荷,表现为转移结节数量和大小的减少(图6J-N)。总之,这些发现表明,tRF-Ser可能在体内抑制GC的进展和转移。鉴于已知tRF-Ser通过抑制EMT和促进铁死亡来抑制GC,我们研究了它是否也通过扰乱能量代谢来增强对5-FU的敏感性。功能实验表明,tRF-Ser使GC细胞对5-FU增敏。在5-FU处理下,tRF-Ser过表达细胞的细胞活力显著降低,而tRF-Ser低表达细胞的细胞活力显著提高(图6O,P)。然后我们评估了一种新的组合策略:tRF-Ser过表达与Erastin和5-FU联合。在体外,与任何单一或双重处理相比,这种三联用药协同增加MDA水平和消耗GSH更有效(图6Q,R)。在体内,与所有其他组相比,它产生了最明显的抗肿瘤作用,显著减少了皮下肿瘤的体积和重量(图6S-V)。组织学和生化分析显示,在三联治疗组中,Ki-67、GPX4和HSPA8的表达显著降低,MDA水平升高(图6W,X)。总之,我们的研究结果表明,tRF-Ser可能通过多种功能抑制GC进展:抑制EMT,诱导铁死亡,并使肿瘤对5-FU化疗敏感。
结论:
我们发现了一种特定的 tsRNA,即tRF-Ser,其在GC中显著下调。我们发现 tRF-Ser 能够抑制EMT,激活铁死亡,并使胃癌细胞对5-FU化疗更敏感。机制上,tRF-Ser 与CNBP 结合,调节其核定位以及随后 HSPA8 基因的激活。tRF-Ser/CNBP/HSPA8轴抑制β-连环蛋白介导的EMT,并促进了 STUB1 依赖性的GPX4 泛素化降解以驱动铁死亡。我们的研究结果表明,tRF-Ser/CNBP/HSPA8 轴可能在GC中发挥关键的调控网络作用,并且是一个有前景的治疗干预靶点。
参考文献:
Jiao J, Wang G, Liu J, Xiao K, Gao Z, Dong D, Shan K, Cui H, Shang L, Li L, Zhang C. A new candidate tumor suppressor tRF-Ser inhibits gastric cancer progression by regulating the CNBP/HSPA8 axis. Cell Death Dis. 2026 Mar 25;17(1):379. doi: 10.1038/s41419-026-08608-1.






