M1巨噬细胞来源的迁移体通过自噬改善颞下颌关节骨性关节炎
滑膜细胞和软骨细胞之间的相互作用在骨关节炎的进展中起着关键作用。然而,最近发现的囊泡细胞器介导细胞间通讯的迁移体的作用在这种情况下仍然没有得到充分的探讨。在这里,我们首先证实了颞下颌关节骨性关节炎(TMJ-OA)患者的滑膜组织和滑膜液样本中存在迁移体。综合分析,结合单细胞转录组学和体外验证,确定浸润M1巨噬细胞是滑膜迁移体的主要来源之一。值得注意的是,M1巨噬细胞来源的迁移体减轻了TNF-α-诱导的软骨细胞凋亡,减少了蛋白聚糖的消耗,抑制了分解代谢酶的表达。进一步的分析显示,这些迁移体富含自噬相关蛋白,暗示迁移体与自噬之间存在联系。通过滑膜-软骨类器官共培养模型(“Mini-TMJ”),我们观察到,在谷氨酸钠碘乙酸诱导的炎症条件下,阻断迁移体从滑膜向软骨类器官的转移导致软骨类器官自噬激活减少。相反,外源性添加M1巨噬细胞来源的迁移体到软骨类器官中可以恢复自噬活性。在大鼠TMJ-OA模型中,关节内注射M1巨噬源性迁移体可有效减轻软骨降解并促进自噬激活。总的来说,我们的研究结果表明,M1巨噬细胞来源的迁移体通过增强自噬来改善TMJ-OA的进展。本文于2026年3月发表于J Nanobiotechnology(IF=12.6)上。
技术路线:
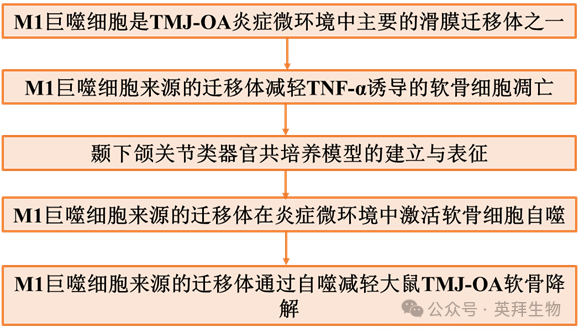
结果:
1)M1巨噬细胞是TMJ-OA炎症微环境中主要的滑膜迁移体之一
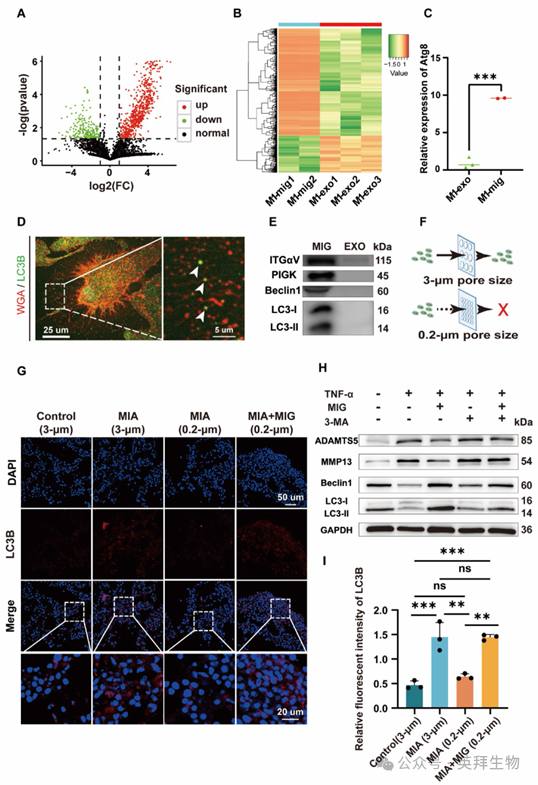
为了证实在TMJ-OA的炎症微环境中存在迁移体,我们使用透射电镜(TEM)分析了临床诊断患者的滑膜组织样本。我们的分析在这些样品中发现了典型的石榴状结构,直径范围从0.5到3 μm(图1A)。这些结构还包含多个腔内小泡,与先前报道中描述的迁移体形态一致。为了全面筛选复杂滑膜微环境中迁移体的细胞来源,我们分析了来自健康对照小鼠和CFA诱导的关节炎小鼠TMJ组织的单细胞RNA测序(scRNA-seq)数据集(GSE267942)。我们标注了主要的细胞群,包括成纤维细胞、内皮细胞和巨噬细胞(图1B)。随后,我们基于关键生物发生基因(Tspan4、Cpq、Ndst1、Pigk、Eogt、Itgb1、Itga5)的汇总表达量,计算了每个细胞簇的迁移体评分。我们的分析揭示了健康与疾病组之间存在细胞组成的差异。驻留细胞群(如成纤维细胞和内皮细胞)在两组中保持了相对一致的迁移体评分,而巨噬细胞簇则表现出一种独特的、依赖于浸润的模式(图1C)。具体而言,这种Cd86高表达的促炎巨噬细胞簇在对照组中几乎不存在,但在CFA诱导组中则显著浸润至颞下颌关节(TMJ)组织中,同时伴随着极高的迁移体评分。这表明,在炎症条件下,M1型巨噬细胞构成了迁移体的主要来源之一。为了进一步在原位验证这些生物信息学发现,我们采用多重免疫组织化学(mIHC)研究了人类TMJ-OA滑膜组织中迁移体和特定细胞类型之间的空间关系。我们观察到迁移体的标记物TSPAN4和PIGK与CD80 (M1巨噬细胞的特异性标记物)共定位。相反,TSPAN4/PIGK和vimentin(成纤维细胞标记物)或CD31(内皮细胞标记物)之间的共定位很少(图1D)。为了在体外证实M1型巨噬细胞产生迁移体的能力,我们将THP-1单核细胞诱导分化为M1型巨噬细胞。小麦胚凝集素(WGA)染色分析显示,这些极化的M1型巨噬细胞表现出旺盛的迁移体形成能力(图1E)。同时,我们从TMJ-OA患者中分离原代FLS(滑膜成纤维细胞),并利用THP-1单核细胞诱导生成M0型巨噬细胞以进行对比。对WGA染色的定量分析表明,M1型巨噬细胞产生迁移体的数量显著高于FLS,而M0型巨噬细胞则几乎没有形成迁移体(图1E-F)。为了验证这些迁移体能否被释放到滑液中,我们收集了TMJ-OA患者的滑液,并采用密度梯度离心法分离囊泡。对这些囊泡的TEM分析显示,其形态与滑膜组织中的迁移体相一致(图1G)。总的来说,M1巨噬细胞是炎症条件下滑膜迁移体的主要来源之一。
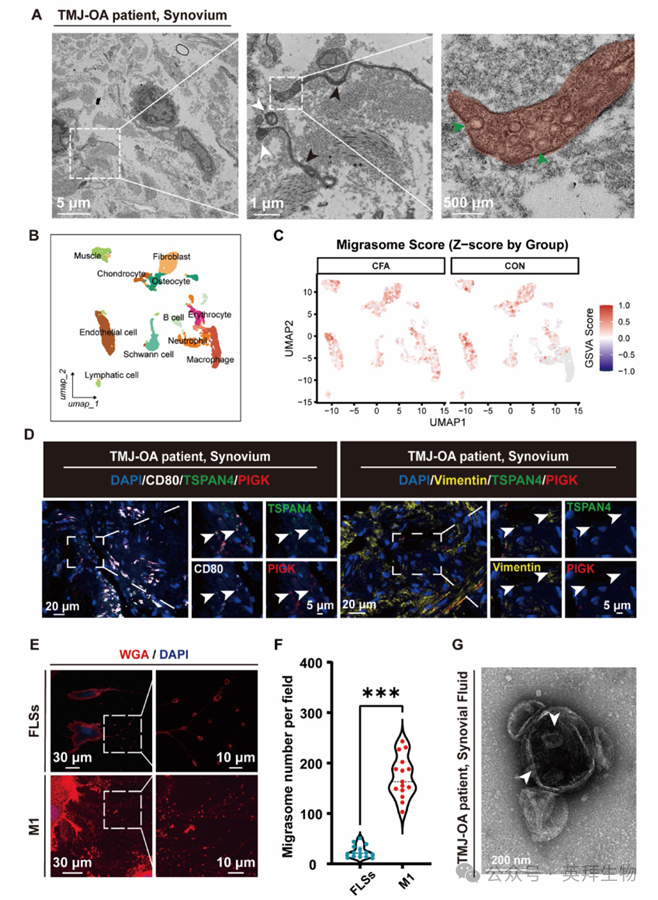
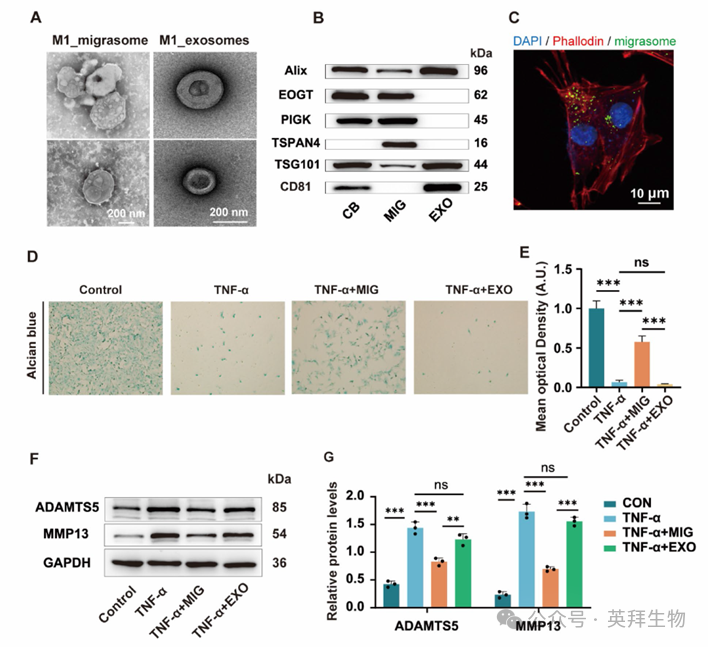
2)M1巨噬细胞来源的迁移体减轻TNF-α诱导的软骨细胞凋亡
鉴于M1型巨噬细胞具有强大的迁移体产生能力,且滑液中存在这些囊泡,我们假设在TMJ-OA的炎症环境中,迁移体促进了巨噬细胞与软骨细胞之间的细胞间通讯。为了验证这一假设,我们首先利用密度梯度离心法纯化了M1巨噬细胞来源的迁移体。纯化后的囊泡呈现出典型的石榴状形态(图2A)。Western blot分析表明,纯化的迁移体中显著富集了关键的迁移体相关标志物,包括TSPAN4、EOGT和PIGK(图2B)。接下来,我们将WGA标记的迁移体加入原代大鼠软骨细胞中。共聚焦显微镜观察显示,迁移体被软骨细胞内化,并分散在整个细胞质中(图2C),表明软骨细胞能够有效摄取迁移体。为了在体外模拟TMJ-OA的炎症条件,我们使用TNF-α处理软骨细胞。结果显示,100 ng/mL TNF-α处理24小时后,细胞活力显著降低,蛋白聚糖耗竭。值得注意的是,随后再加入10 μg/mL迁移体继续培养24小时,可显著减轻TNF-α诱导的细胞凋亡和蛋白聚糖丢失(图2D、E)。此外,Western blot分析显示,TNF-α处理上调了ADAMTS5和MMP13的蛋白水平。然而,外源性添加迁移体使ADAMTS5和MMP13的表达均发生下调,而外泌体则几乎没有作用(图2F、G)。综上所述,我们的研究结果表明,M1巨噬细胞来源的迁移体减轻了TNF-α-诱导的软骨细胞凋亡,抑制了分解代谢酶的表达。
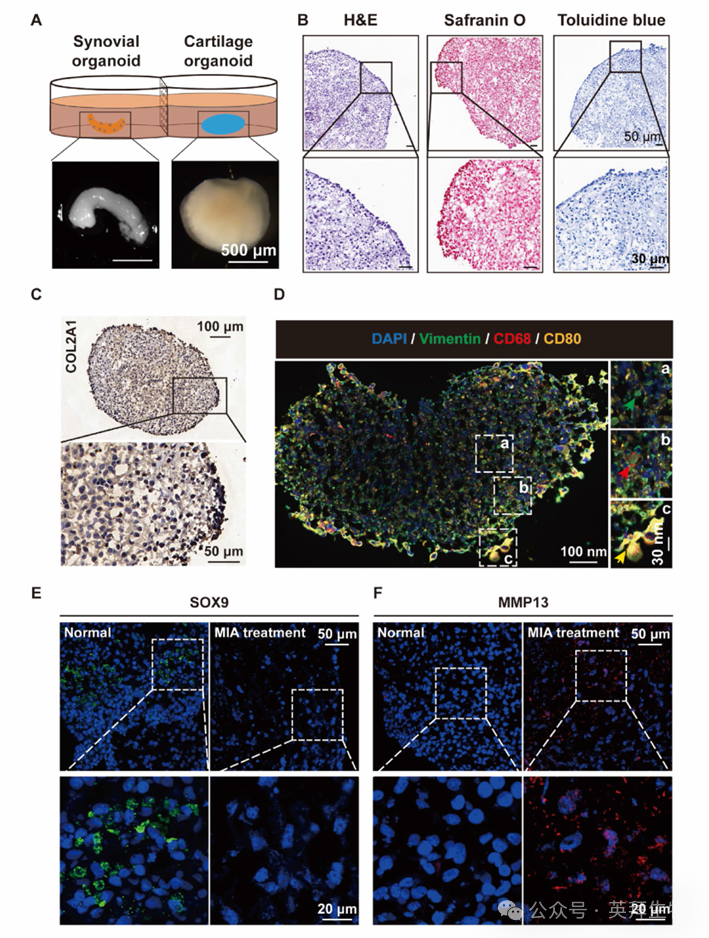
3)颞下颌关节类器官共培养模型的建立与表征
传统的二维培养在重现复杂的三维细胞结构、准确模拟细胞间相互作用以及反映细胞与细胞外基质之间的关系方面存在固有的局限性。为了克服这些挑战,我们构建了一种“Mini-TMJ”(微型颞下颌关节)模型,这是一种滑膜-软骨类器官共培养模型,能够模拟天然TMJ的分层结构和功能微环境(图3A)。H&E染色显示,软骨类器官具有分层结构,包含明显的表层和增殖层,与天然髁突软骨的组织结构高度相似。番红O/甲苯胺蓝染色显示软骨类物体内有丰富的聚集蛋白聚糖)沉积(图3B),而免疫组化染色证实了II型胶原蛋白(COL2A1)呈阳性表达(图3C)。滑膜类器官则是通过在三维微环境中将原代人FLS与THP-1细胞共培养而构建的。mIHC分析显示,CD68+的M0型巨噬细胞和CD68+/CD80+的M1型巨噬细胞主要定位于表层,而Vimentin+的FLS则位于较深的衬里下层,重现了炎症条件下天然滑膜的组织结构(图3D)。进一步的免疫荧光分析显示,MIA处理48小时后,类器官出现了显著的病理变化,与对照组相比,表现为MMP13蛋白水平升高以及SOX9表达降低(图3E和F)。
4)M1巨噬细胞来源的迁移体在炎症微环境中激活软骨细胞自噬
为了探究迁移体缓解软骨细胞凋亡的机制,我们对M1巨噬细胞来源的外泌体和迁移体进行了质谱分析。蛋白质组学分析揭示了两者在蛋白质货物上存在显著差异(图4A、B)。值得注意的是,与外泌体相比,迁移体中显著富集了ATG8家族蛋白(图4C)。鉴于LC3是哺乳动物中研究最为广泛的ATG8同源物,在自噬体形成和底物选择中发挥着关键作用,我们采用高分辨率共聚焦显微镜来研究迁移体与自噬相关蛋白之间的空间关系。免疫荧光分析显示,LC3B阳性斑点与迁移体存在空间重叠(图4D)。Western blot分析进一步证实,与M1巨噬细胞来源的外泌体相比,典型的自噬标志物Beclin1和LC3B在M1巨噬细胞来源的迁移体中显著富集(图4E)。这些发现暗示M1巨噬细胞来源的迁移体可能通过调节自噬发挥软骨保护作用。为了验证这一假设,我们在TMJ-OA类器官模型中引入了尺寸选择性滤膜(孔径分别为3 μm和0.2 μm),以调控迁移体介导的细胞间串扰(图4F)。3 μm滤膜允许迁移体自由穿梭,而0.2 μm滤膜则完全阻断了迁移体在滑膜类器官与软骨类器官之间的运输。免疫荧光分析显示,使用0.2 μm滤膜阻断迁移体运输后,软骨类器官中LC3B和Beclin1的蛋白水平降低,同时促进了p62蛋白的积累。值得注意的是,外源性添加M1巨噬细胞来源的迁移体可恢复自噬活性,这与允许迁移体自由穿梭的3 μm滤膜组中观察到的结果相一致(图4G、I)。我们进一步在TNF-α刺激的软骨细胞中验证了这些发现。Western blot分析显示,与M1巨噬细胞来源的迁移体共培养的软骨细胞表现出增强的自噬活性,这体现在LC3-II/LC3-I比值升高以及Beclin1蛋白水平上调。值得注意的是,与单独使用TNF-α处理相比,MMP13和ADAMTS5的蛋白水平也随之受到抑制(图4H)。为了明确这种保护作用是否依赖于自噬,我们使用了抑制剂3-甲基腺嘌呤(3-MA)。结果显示,3-MA显著消除了这些效应。这些结果表明,M1巨噬细胞来源的迁移体能够激活软骨细胞自噬,并抑制炎症微环境中的软骨降解。
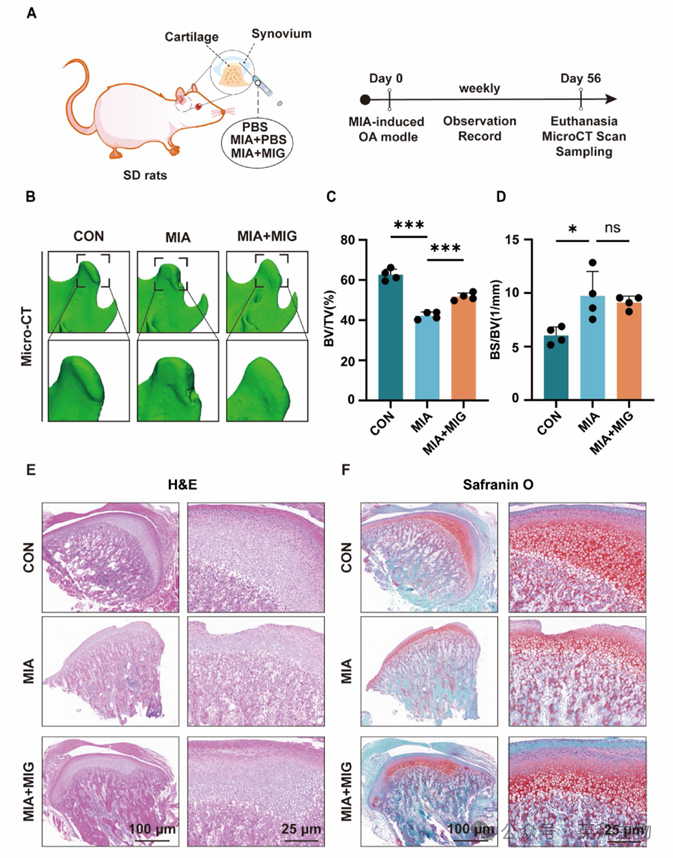
5)M1巨噬细胞来源的迁移体通过自噬减轻大鼠TMJ-OA软骨降解
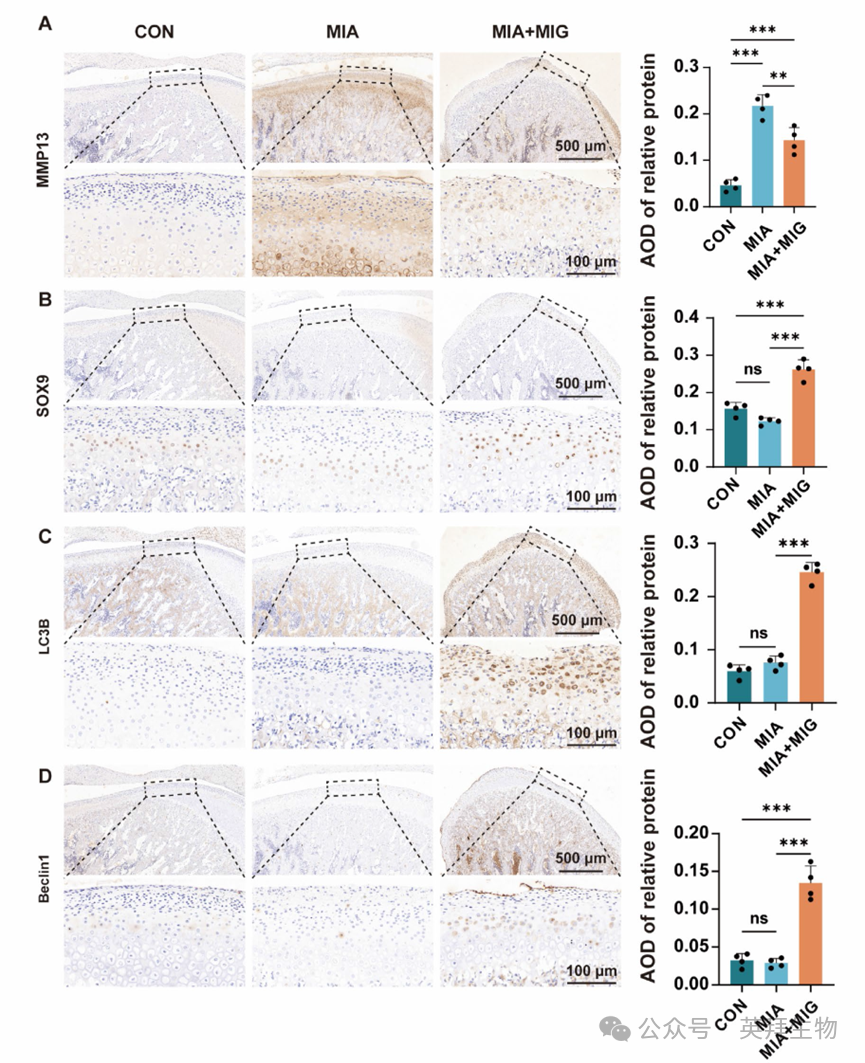
我们进一步探讨了这些迁移体在骨关节炎模型中是否能发挥软骨保护作用。为此,我们构建了大鼠TMJ-OA模型,其中对照组接受关节腔内PBS注射,MIA组接受关节腔内MIA注射,MIA+MIG组接受关节腔内MIA注射联合M1巨噬细胞来源的迁移体治疗(图5A)。注射8周后,进行micro-CT分析和三维重建以评估髁突的形态。结果显示,与对照组相比,MIA组髁突前斜面出现了明显的骨小梁吸收,同时骨体积分数(BV/TV)显著降低,骨表面积与骨体积比(BS/BV)升高。相比之下,MIA+MIG组的迁移体治疗有效维持了骨小梁微结构的完整性(图5B–D)。H&E染色证实对照组的软骨结构保持完好。相比之下,MIA组表现出典型的退行性改变。这些骨关节炎病变在MIA+MIG组中得到了显著减轻(图5E)。番红O/固绿染色的组织学评估显示,与MIA组相比,MIA+MIG组的糖胺聚糖含量出现了明显的恢复(图5F)。与对照组相比,MIA组的免疫组化分析显示MMP13水平显著升高,且SOX9表达明显降低。MIA+MIG组有效减轻了MIA诱导的MMP13升高和SOX9降低,展现出对骨关节炎进展的强大保护作用(图6A,B)。此外,MIA+MIG组与对照组和MIA组相比,LC3B和Beclin1的蛋白水平均有所增加(图6C,D)。这些结果表明,注射M1巨噬细胞来源的迁移体可显著促进自噬,从而抑制大鼠TMJ软骨的软骨降解。
结论:
我们在TMJ-OA中发现了迁移体的存在,并在Mini-TMJ共培养模型和大鼠TMJ-OA模型中证明了M1巨噬源性迁移体通过自噬改善TMJ-OA。我们的研究结果表明,M1巨噬细胞衍生的迁移体可能作为TMJ-OA的一种新的治疗策略。
参考文献:
Sa G, Zou Z, Zhou H, Sa G, Zhou J, Tu H, Shi Y, He Y, Guo Y, Liu Z, Yang X. M1 macrophage-derived migrasomes ameliorate temporomandibular joint osteoarthritis via autophagy. J Nanobiotechnology. 2026 Mar 10;24(1):370. doi: 10.1186/s12951-026-04248-x.






