miRNA-711在细胞外结合并激活TRPA1以引起急性和慢性瘙痒
越来越多的证据表明,细胞外miRNAs可能作为疾病的生物标志物,但细胞外miRNA的生理相关性尚不清楚。8月8号杜克大学医学中心研究人员在《Neuron》上发表论文,该论文发现面颊皮内注射miR-711在首次接受试验的小鼠中可诱导TRPA1依赖性瘙痒(刮擦)而没有疼痛(擦拭)。细胞外灌注miR-711可通过核心序列GGGACCC在TRPA1表达的异源细胞和固有感觉神经元中诱导TRPA1。计算机模拟显示,核心序列结合TRPA1胞外S5-S6环上的几个残基,这些残基对miR-711激活TRPA1至关重要,而不是异硫氰酸烯丙酯。在免疫缺陷小鼠中,皮内接种人类Myla细胞会诱发淋巴瘤和慢性瘙痒,这与癌细胞分泌的血清miR-711水平升高有关。miR-711抑制剂和阻断肽可破坏miR-711/TRPA1相互作用,从而可抑制淋巴瘤诱导的慢性瘙痒。研究结果证明了细胞外miRNA作为瘙痒介质和离子通道调节因子的非常规生理作用。
研究路线:
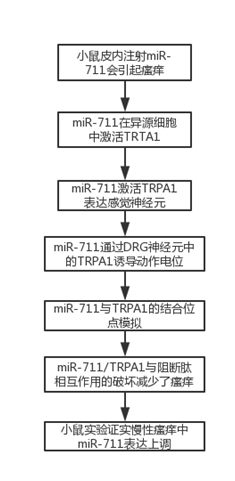
研究结果:
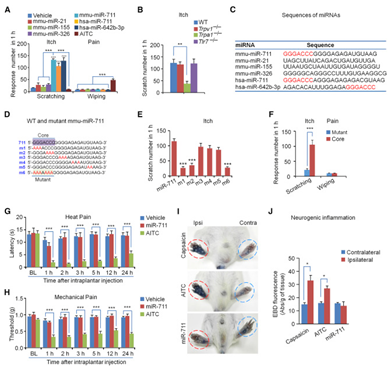
图1 皮内miR-711通过GGGACCC核心序列和TRPA1诱导瘙痒但不疼痛
(A)皮内注射含有miRNA的GGGACCC(B)mmu-miR-711诱导的划痕在Trpa1 - / -而不是Trpv1 - / -和Tlr7 - / -小鼠中降低。(C)在该研究中测试的miRNA的序列。(D)mmu-miR-711的序列和mmu-miR-711的6个突变体。(E)通过皮内注射mmu-miR-711及其突变体(1mM,5μL)诱导的划痕。(F)核心序列GGGACCC而不是突变序列AAAAAAA足以在幼稚小鼠中引起刮擦而不是擦拭。(G)热痛觉过敏。(H)机械异常性疼痛(I)伊文思蓝染色的后爪的图像。(J)同侧和对侧后爪中伊文思蓝染色的定量。
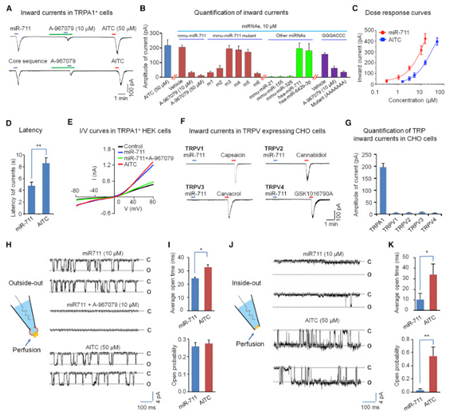
图2 miR-711 在异源细胞中激活TRPA1
(A)由mmu-miR-711和核心序列诱导的内向电流痕迹。(B)由AITC(50μM),miRNA(10μM),核心序列,突变RNA 寡核苷酸和A967079的作用诱导的内向电流的定量(振幅)。(C)剂量 - 反应曲线,比较由mmu-miR-711和AITC诱导的内向电流的幅度。(D)由AITC和mmu-miR-711引起的内向电流的潜伏期。(E)由mmu-miR-711,AITC和mmu-miR-711 + A967079引发的I / V曲线。(F)诱导的内向电流的痕迹激动剂的TRPV1 ,TRPV2 ,TRPV3,和 TRPV4。(G)(F)中描述的内向电流的量化。(H)单渠道活动的痕迹。(I)单通道开放时间和开放概率的量化。(J)单渠道活动的痕迹。(K)单通道开放时间和开放概率的量化。
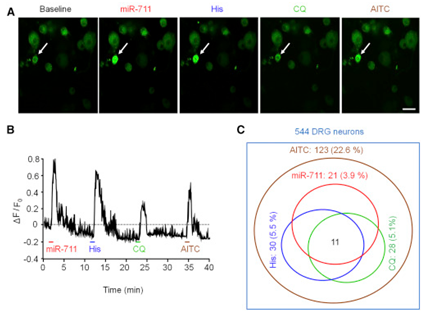
图3 DRG培养物中的钙成像显示Pirt-GCaMP3小鼠中miR-711 激活TRPA1表达感觉神经元亚群
(A)mmu-miR-711,组胺 ,氯喹 和AITC的代表性图像。 (B)mmu-miR-711,组胺,CQ和AITC的神经元钙响应。(C)维恩图显示miR-711-响应神经元和组胺- ,CQ-和AITC-响应神经元之间的重叠以及培养的DRG神经元中每个群体的百分比。
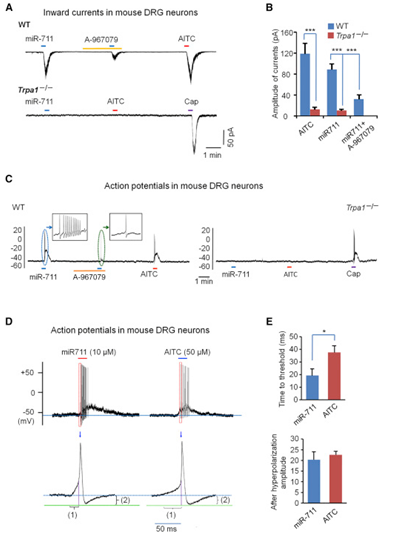
图4 miR-711 通过小鼠DRG神经元中的TRPA1 诱导内向电流和动作电位
(A)内向电流的痕迹。(B)内向电流的幅度。(C)miR-711和AITC在WT和Trpa1 - / -小鼠中的小直径小鼠DRG神经元中诱导的动作电位。(D和E)miR-711和AITC在WT小鼠中的小直径DRG神经元中诱导的不同动作电位。(D)动作电位的痕迹。(E)动作电位的上升时间或阈值时间的定量,在(D)中和在超极化振幅之后表示为(1),如(D)中的(2)所示。
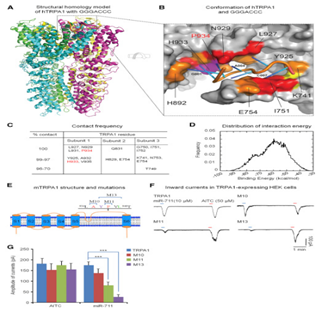
图5 miR-711核心序列与hTRPA1细胞外环结合的计算机模拟及结合位点的鉴定
(A)与hTRPA1细胞外表面结合的核心序列GGGACCC的结构。 (B)与TRPA1细胞外表面结合的GGGACCC的缩放视图。(C)hTRPA1残基与GGGACCC之间的接触频率。(D)GGGACCC的分布估计通过200万步RexDMD模拟收集的hTRPA1的结合能。从结合能等于-75kcal / mol开始,分布的左肩表征高亲和力GGGACCC / TRPA1复合物的构象整体。(E)具有亚基1的详细残基的hTRPA1的示意图。(F)由mmu-miR-711诱导的表达mmu-TRPA1或其突变体的CHO细胞的内向电流痕迹。(G)ATIC和mmu-miR-711诱导电流的定量。
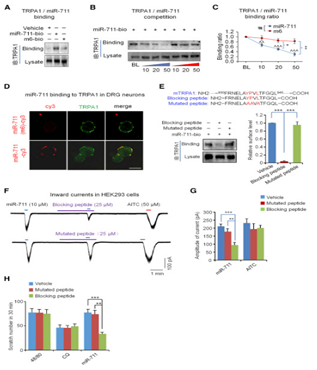
图6 miR-711 / TRPA1与阻断肽相互作用的破坏减少了瘙痒
(A)RNA pull-down测定显示hTRPA1与生物素缀合的mmu-miR-711结合。(B)RNA pull-down显示野生型mmu-miR-711与bio-mmu-miR-711竞争结合hTRPA1。(C)(B)中所示的mmu-miR-711 / hTRPA1结合活性的定量。(D)活细胞标记显示Cy3标记的mmu-miR-711与培养的DRG神经元表面上的mTRPA1的结合。(E)RNA pull-down测定显示阻断肽破坏mmu-miR-711 / hTRPA1相互作用,但不破坏突变肽。(F)表达hTRPA1的HEK293细胞中阻断肽对mmu-miR-711诱导的内向电流的抑制。(G)(F)中内向电流的量化。(H)阻断肽抑制皮内注射mmu-miR-711诱导的小鼠瘙痒。
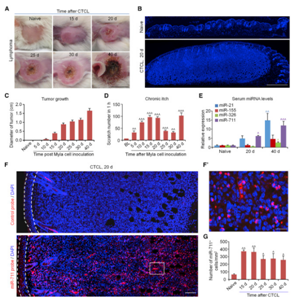
图7 CTCL的小鼠模型显示慢性瘙痒和miR-711上调
(A)通过皮内注射CD4 + Myla细胞接种后15,20,25,30和40天背皮上的淋巴瘤图像(B)CTCL后正常和荷瘤皮肤的DAPI染色图像。(C)接种CD4 + Myla细胞后肿瘤直径显示肿瘤生长的时间过程。(D)CTCL诱发的慢性瘙痒的时间过程。(E)CTCL小鼠的hsa-miR-21,hsa-miR-155,hsa-miR-326和hsa-miR-711的血清水平。(F)原位杂交(红色)显示CTCL诱导后20天在背部皮肤上的淋巴瘤细胞中的hsa-miR-711表达。(F')(F)中的扩大框显示单染色和双染色。(G)在CTCL的不同时间每平方毫米背部皮肤定量hsa-miR-711阳性细胞。
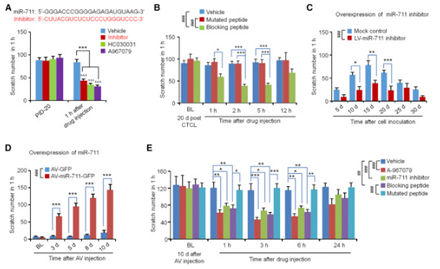
图8 miR-711抑制剂,TRPA1 拮抗剂和miR-711 / TRPA1相互作用阻断肽在CTCL小鼠模型中对慢性瘙痒的抑制作用
(A)通过皮内注射hsa-miR-711抑制剂和TRPA1拮抗剂,抑制CTCL诱发的慢性瘙痒。(B)在Myla细胞接种后20天给予阻断肽对CTCL诱发的慢性瘙痒的抑制。(C)在接种前通过慢病毒在Myla细胞中过表达hsa-miR-711抑制剂减弱CTCL后的慢性瘙痒。(D)通过腺病毒过表达hsa-miR-711诱导皮肤AV注射在背部皮肤上后持续瘙痒。(E)皮内注射A-967079,hsa-miR-711抑制剂和阻断肽。






