Prodrug suicide gene therapy for cancer targeted intracellular by mesenchymal stem cell exosomes
间充质干细胞(MSCs)及其外泌体由于其靶向肿瘤中的天然行为被认为是一种有前景的治疗方法。近日,来自斯洛伐克科学院的Altaner和他的团队在INTERNATIONAL JOURNAL OF CANCER(IF=7.36)在线发表了题目“Prodrug suicide gene therapy for cancer targeted intracellular by mesenchymal stemcell exosomes”的文章,他们设计自杀基因yCD::UPRT在各种人体组织制备的MSCs表达。该自杀基因转导细胞的CM包含外泌体,载着自杀基因的mRNA。该外泌体很容易被肿瘤细胞内化,在前体药物5-氟胞嘧啶(5-FC)的存在下,携带自杀基因的外泌体可以使肿瘤细胞以剂量依赖性的方式死亡。根据他们的检测,由MSC和自杀基因转导的MSC产生的外来体中微小RNA的存在没有显着差异,与治疗效果无关。 携带自杀基因MSC外泌体代表了一类新的肿瘤细胞靶向药物在细胞内起作用并具有治愈潜力。
技术路线
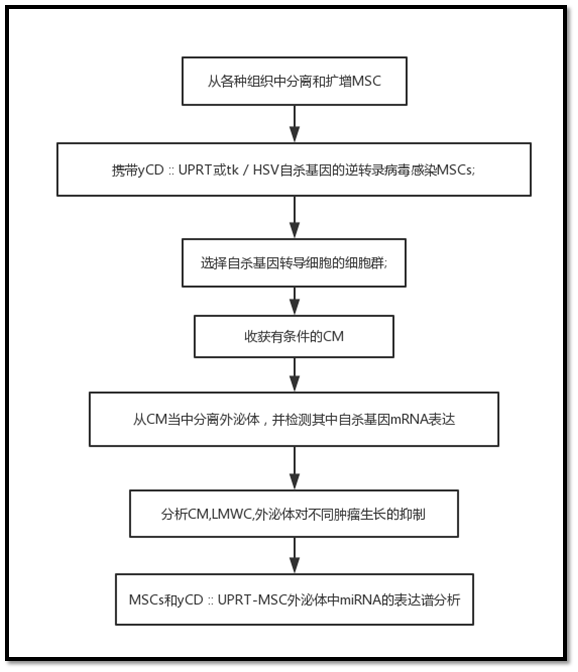
主要结果
1 从各种人组织获得的MSC可以用CD :: UPRT自杀基因转导。
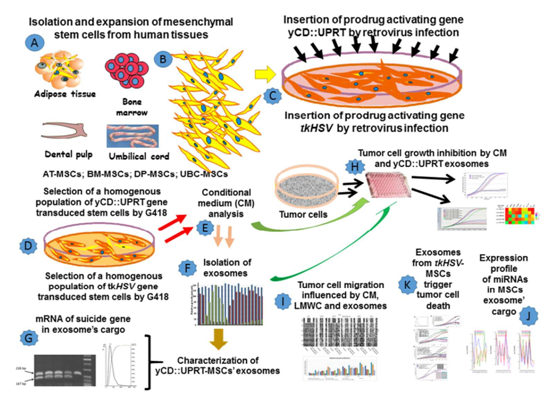
图1 贯穿整个工作的实验步骤。
(A,B)从各种组织中分离和扩增MSC;(C)携带yCD :: UPRT或tk / HSV自杀基因的逆转录病毒感染MSCs; (D)选择自杀基因转导细胞的细胞群;(E)收获有条件的媒介;(F)从CM中分离外泌体;(G)检测外泌体货物中自杀基因的mRNA;(H)用CM和yCD :: UPRT-外泌体抑制肿瘤细胞生长;(I)CM,外泌体和LMWC对肿瘤细胞迁移的影响; (J)MSCs和yCD :: UPRT-MSC外泌体中miRNA的表达谱。
2 与相应MSCs相比,不同来源yCD::UPRT-MSCs对条件培养基肿瘤细胞生长抑制效应更加显著。
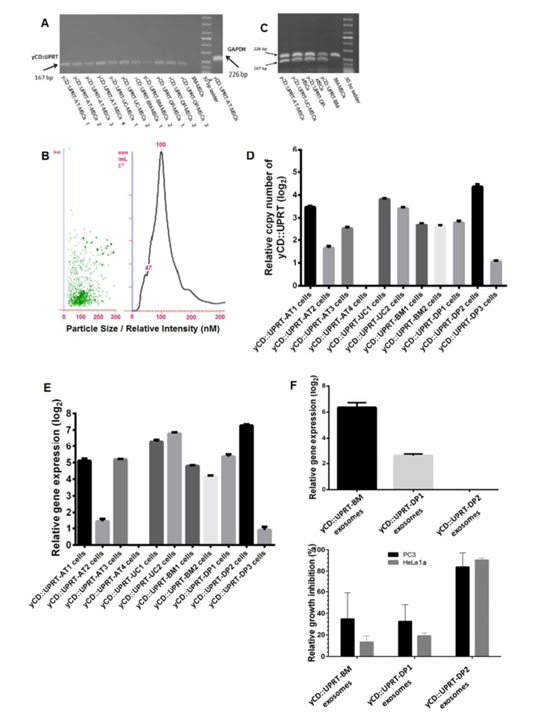
图2 yCD :: UPRT基因在同源培养的yCD :: UPRT- MSCs中的表达
(A)PCR扩增来自yCD :: UPRT基因转导的MSC的分离的细胞DNA。 凝胶分辨率证实了特定序列的存在(B)通过Nanosight检测从yCD :: UPRT基因转导的MSC释放的外泌体;(C)来自yCD :: UPRT基因转导的MSC的分离的经DNase处理的总RNA被逆转录并进行PCR扩增。 通过琼脂糖凝胶电泳显现特定转录物的存在。(D)qRT-PCR估计各种yCD :: UPRT基因转导的MSC的细胞DNA中整合的DNA yCD :: UPRT基因的相对拷贝数。(E)qRT-PCR估计来自yCD :: UPRT转导的MSC的外来体中mRNA的相对表达;(F)外来体货物中yCD :: UPRT基因的mRNA与肿瘤细胞生长抑制活性的比较。
3 来自yCD::UPRT基因转导不同组织来源的MSCs的CM, LMWC, 外泌体的不同肿瘤细胞生长抑制疗效不同。
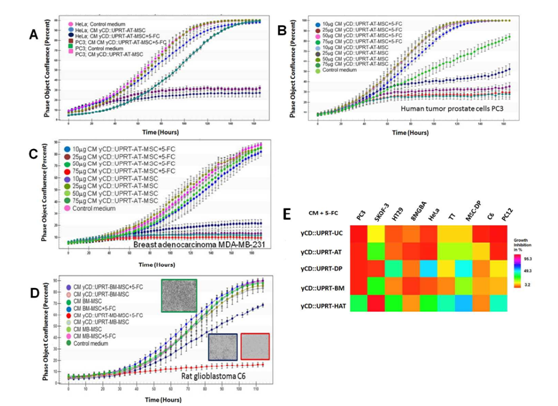
图3 不同MSCs外泌体表达yCD::UPRT基因的对肿瘤细胞生长抑制活性的评估。
(A)刺激了在不存在前药b5-FC的情况下用来自yCD :: UPRT-AT-MSC的CM处理的PC3细胞的生长,但未检测到HeLa1a细胞的生长刺激。(B)在5-FC存在下,用来自yCD :: UPRT-AT-MSC的CM处理的人前列腺肿瘤细胞PC3的生长被剂量依赖性地抑制; (C)人乳腺癌细胞MDA-MB-231的生长在5-FC存在下以剂量依赖性地被抑制,但是在没有5-FC的情况下没有影响他们的成长; (D)大鼠胶质母细胞瘤细胞C6被来自yCD :: UPRT-MB-MSC的CM有效杀死,并被yCD :: UPRT-BM-MSC部分杀死。(E)在5-FC存在下,yCD :: UPRT-MSC的CM中外泌体的肿瘤细胞死亡功效的比较(与具有相同蛋白质含量值(50μg)的CM样品)。
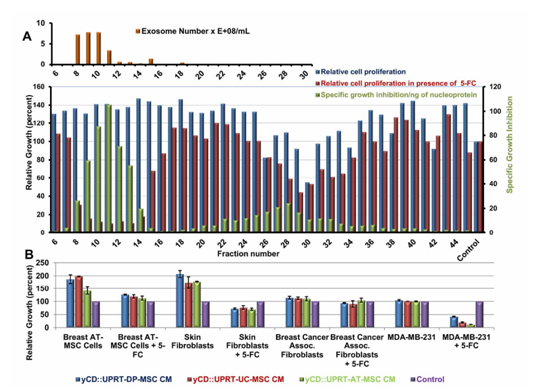
图4 yCD中CM的筛析::UPRT-AT-MSCs和外泌体的肿瘤细胞特异性。
(A) CM与yCD::UPRT-AT-MSCs分离;(B)不同yCD::UPRT转导的MSCs中CM的特异性。
4 MSCs及相应的yCD::不同组织来源的UPRT-MSCs的microrna的表达没有显著不同。
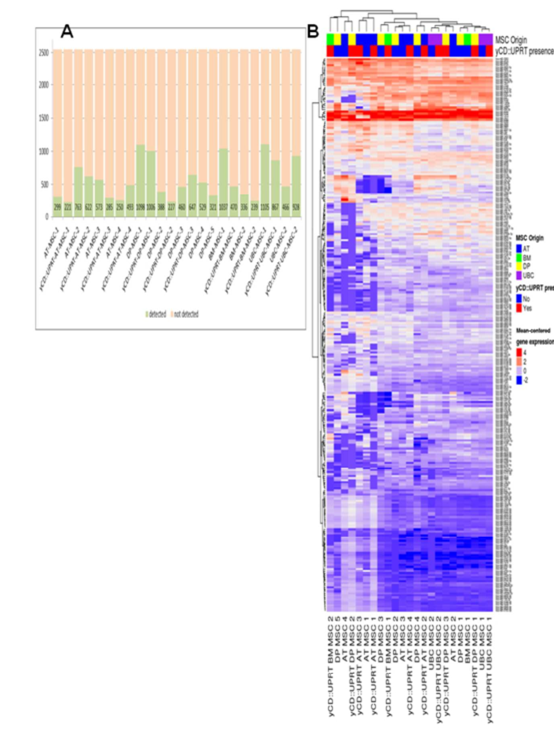
图5 未转导的MSC外泌体和yCD:: uprt -基因转导的细胞中外泌体差异表达的mirna表达谱。
(A)根据组织类型和是否存在yCD::UPRT基因,对2549个微阵列中检测到的microRNAs(绿柱)数量进行比较。(B)基于子集(276 miRNA,至少在75%的样品中表达;)液的检测小分子核糖核酸释放不同的组织起源MSC和相应的yCD::UPRT gene-transduced MSC之间的表达差异(BH调整p值> 0.05)。






