肝纤维化VS 自噬/外泌体
肝纤维化是肝脏受到各种理化因素损伤,肝细胞发生炎症、坏死,并且在坏死区内细胞外基质过度沉积的一种疾病,可发展为肝功能失常的肝硬化,甚至肝癌,有效干预肝纤维化的发生,能预防肝硬化和肝癌的发生,因此,肝纤维化是目前肝病领域的研究热点。肝星状细胞(HSC)的活化被认为是肝纤维化形成的重要环节,其合成和分泌的细胞外基质在肝过度沉积可引起肝纤维化。今天小编就和大家分享一篇关于自噬和外泌体介导的HSC活化进而影响肝纤维化进程的文献。

技术路线
1. TRIB3表达升高有助于肝纤维化的进展
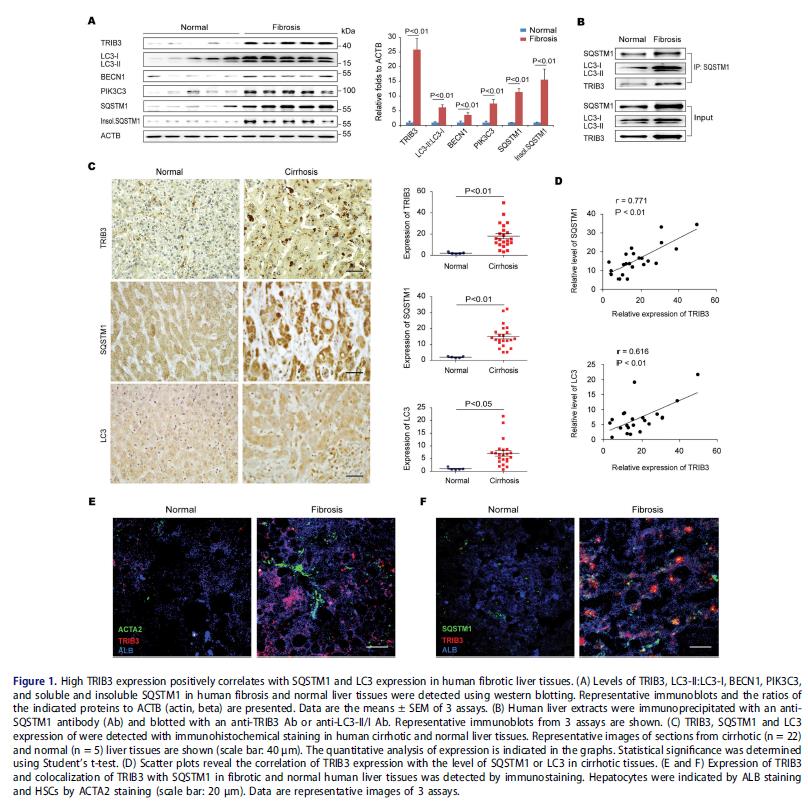
纤维化肝中TRIB3,LC3-II:LC3-I, BECN1, PIK3C3,可溶性和不可溶性SQSTM1是升高的,看到TRIB3-SQSTM1和 SQSTM1-LC3相互作用,TRIB3的表达和SQSTM1或者LC3的表达是正相关,肝细胞和HSC细胞增加,TRIB3与SQSTM1共定位增加。
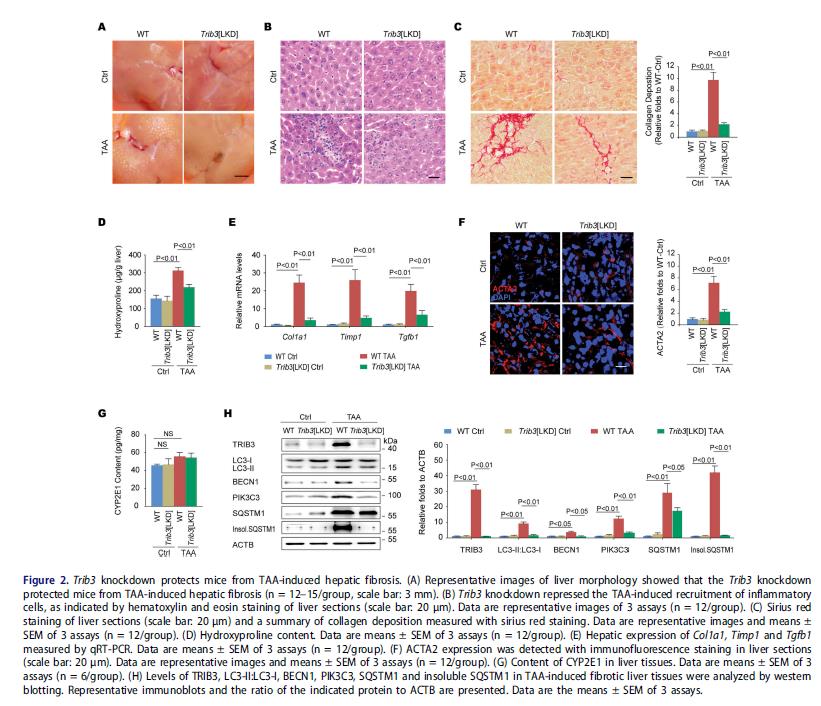
2.TRIB3敲除保护小鼠免受TAA诱导的肝纤维化
TAA处理12周后,Trib3敲低小鼠显示较少的结节、黄疸和肝脏浸润性炎症细胞减少,肝脏的间质非血管区胶原积聚减少,羟脯氨酸含量降低,Col1a1,Timp1和Tgfb1的mRNA水平降低。TAA处理的Trib3 [LKD]小鼠中ACTA2表达减弱。为检测沉默TRIB3是否可以通过自噬影响肝纤维化,检查自噬信号蛋白在纤维化肝组织中的表达。沉默Trib3抑制LC3-II:LC3-I,BECN1和PIK3C3表达,也减少不溶性SQSTM1在TAA处理肝脏中的聚集,不影响可溶性SQSTM1的水平。这些数据表明TRIB3通过抑制自噬来介导肝纤维化。
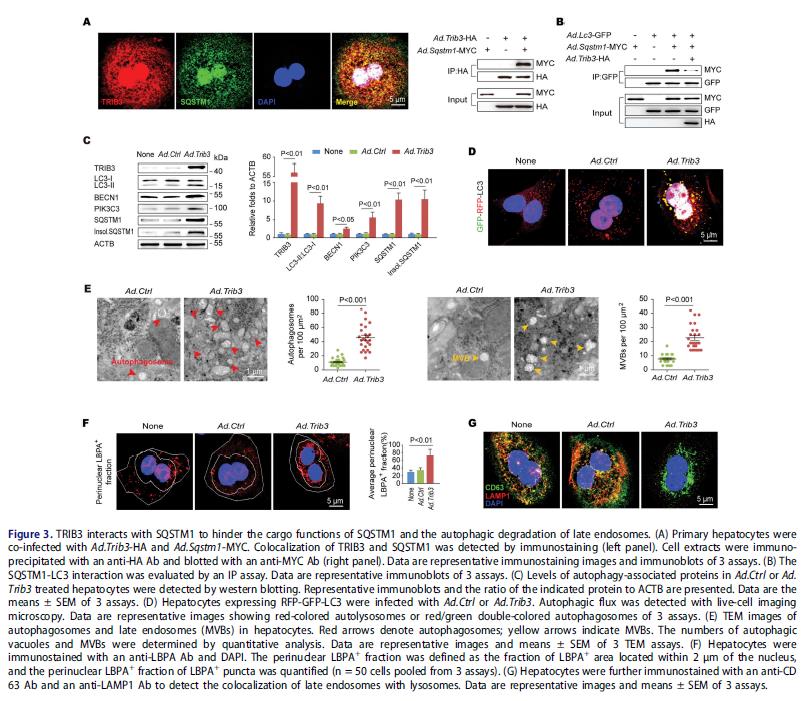
3.TRIB3与SQSTM1相互作用以阻止肝细胞中晚期内体的自噬降解
饥饿的原代小鼠肝细胞TRIB3和SQSTM1有关系,在肝细胞中共表达SQSTM1和 LC3,不管有没有TRIB3,SQSTM1都能与LC3共沉淀,这个相互作用能被TRIB3的过表达减弱。原代肝细胞过表达TRIB3增强LC3-II:LC3-I,BECN1,PIK3C3和SQSTM1的表达和不溶性SQSTM1的聚集。
为确认TRIB3在抑制自噬流中的作用,LC3的腺病毒感染肝细胞测定自噬流,基于溶酶体GFP猝灭的概念。饥饿细胞后检测到RFP-GFP-LC3为红色斑点,而TRIB3过表达增加黄色斑点的存在和动态移动,TRIB3表达升高增加自噬体、MVB的数量。量化多泡体MVB分布,测量核周溶血磷脂酸(LBPA),LBPA +区域被定义为位于核心2μm范围内。与对照肝细胞相比,CQ处理细胞和TRIB3过表达细胞均表现出核周LBPA +片段增加和LBPA +斑点尺寸扩大。使用CD63和溶酶体标记LAMP1(溶酶体相关膜蛋白1)免疫染色精确界定CQ处理或TRIB3过表达的肝细胞细胞器的改变,CD63和LAMP1的共定位在肝细胞中增强,而CQ治疗或TRIB3过表达显着减少这种共定位。
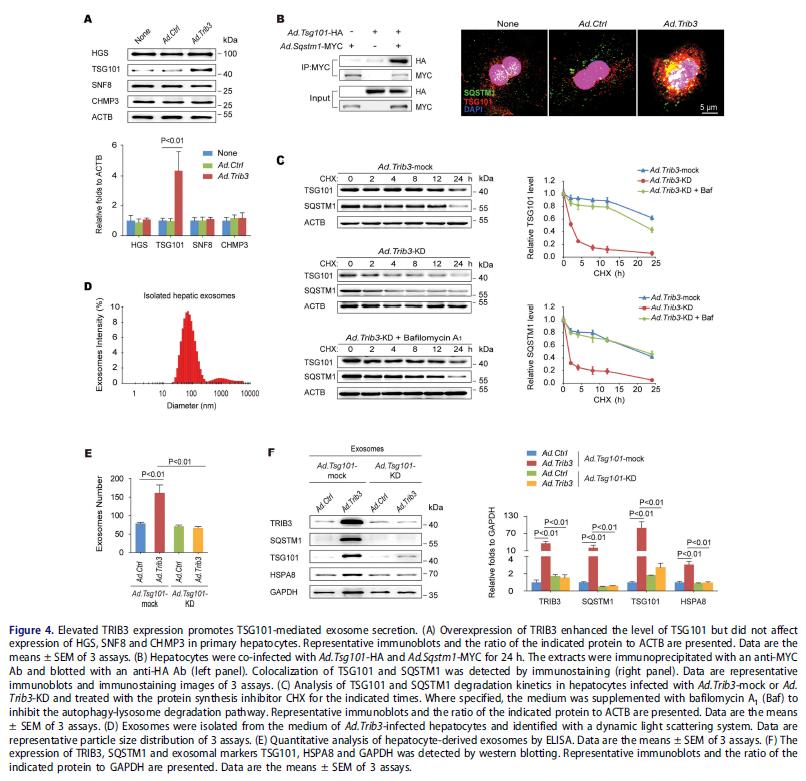
4.TRIB3促进肝细胞的外泌体分泌
鉴于自噬功能障碍是一个外泌体释放的关键因素,推断TRIB3介导的抑制自噬流的变化可导致肝细胞外泌体分泌增强。ESCRT(内体运输所需的分选复合物) 对MVB的形成和MVB来源外泌体的分泌至关重要,TRIB3过表达肝细胞表现出TSG101(肿瘤易感性101 [ESCRT-I的亚基])水平显着增加。共感染Tsg101和Sqstm1的肝细胞,在TRIB3过表达的肝细胞中TSG101与SQSTM1共定位增加。沉默Trib3促进CHX处理的肝细胞中TSG101和SQSTM1的降解,自溶酶体抑制剂巴弗洛霉素A1也有可以降解这两个分子。为确认TRIB3参与的外泌体释放,从Trib3感染肝细胞的培养基中分离外泌体,并用动态光散射系统鉴定,检测TRIB3过表达肝细胞上清液中外泌体的数量增加。TRIB3-过表达肝细胞外泌体标志物如TSG101,HSPA8 / HSC70,和GAPDH以及TRIB3和SQSTM1的表达增加,能被Tsg101缺失逆转。
4.TRIB3通过肝细胞衍生的外泌体激活HSC(肝星状细胞)
用过表达TRIB3肝细胞的外泌体(HepaTRIB3-外泌体)处理HSCs,可看到HSC显着激活,增殖和迁移。200个细胞因子抗体在HepaTRIB3-外泌体中鉴定潜在的HSC激活剂,发现有175种蛋白质没有表达变化或低表达,16种蛋白质下调,9种蛋白质上调。从肝细胞中分离的外泌体处理HSC,大部分外泌体被HSC吞噬(图5E)。INHBA是HepaTRIB3外泌体中最丰富的细胞因子,Inhba敲低肝细胞分泌的外泌体降低HSC中ACTA2和COL1A1的表达。

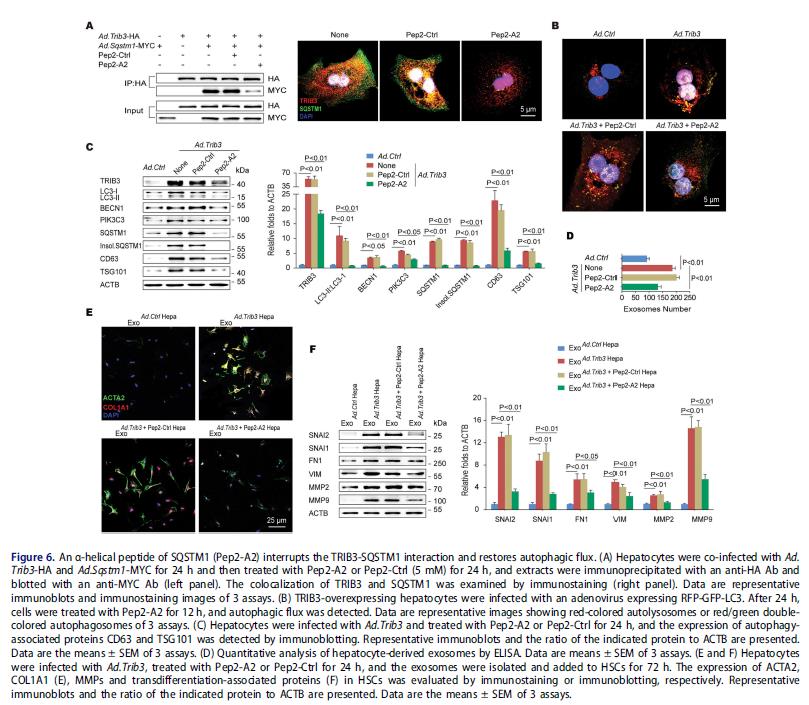
5. 融合肽Pep2-A2能打乱TRIB3和SQSTM1的相互作用并且回复自噬
融合肽Pep2-A2处理抑制过表达TRIB3和SQSTM1的肝细胞中的相互作用和共定位和SQSTM1,用Pep2-A2预处理肝细胞恢复TRIB3抑制的自噬通量,减少培养基中外泌体的数量,消除HepaTRIB3-外泌体的HSC激活作用,HSC中的分化转移信号蛋白MMP2和MMP9也减少。
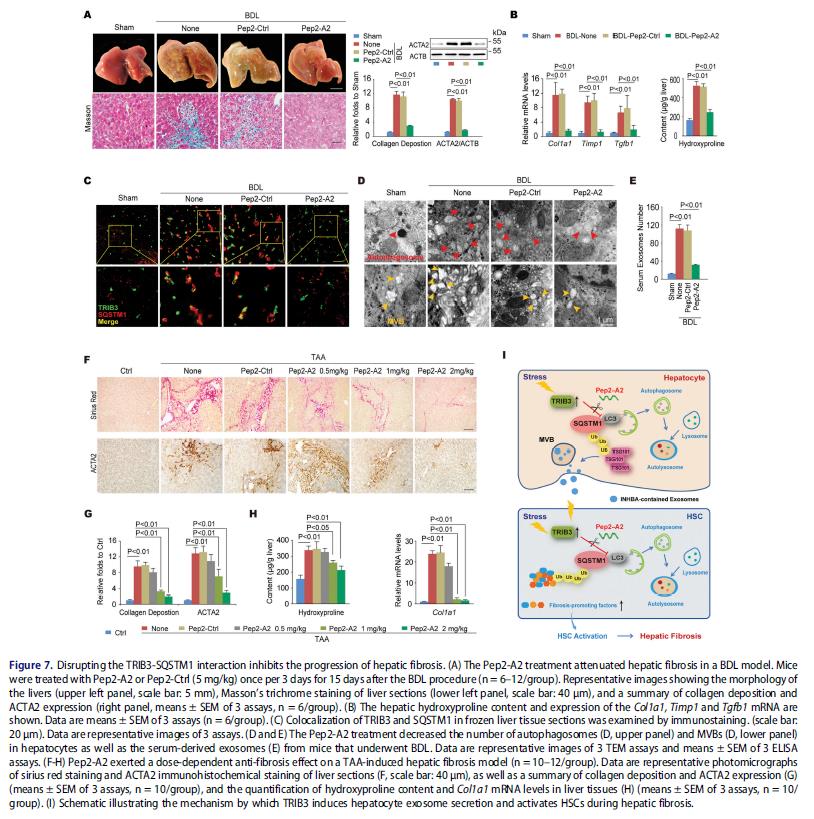
6. 破坏TRIB3-SQSTM1相互作用会减少肝脏纤维化
评估Pep2-A2在BDL-或TAA诱导小鼠肝纤维化模型中的作用。Pep2-A2治疗小鼠显着降低BDL诱导肝纤维化(肝脏形态和胶原沉积改善),肝脏促纤维化基因的表达和羟脯氨酸含量也降低,纤维化肝组织中TRIB3与SQSTM1共定位减少。Pep2-A2处理小鼠中自噬体和MVBs减少,胶原沉积和ACTA2表达减少,羟脯氨酸和Col1a1 mRNA表达减少。这些数据证实了破坏TRIB3-SQSTM1相互作用,通过恢复受阻的自噬通量,来发挥有效的肝纤维化治疗效果。
总结:1. TRIB3表达与肝纤维化密切相关
2. TRIB3与SQSTM1相互作用减弱自噬
3. TRIB3促进肝细胞的外泌体分泌增多,进而可以激活HSC细胞
4.破坏TRIB3-SQSTM1相互作用会减少肝脏纤维化
肝纤维化的进程是一个非常复杂而渐进的过程,受到多种分子及细胞内多种信号转导通路网络的调控。尽管目前对肝纤维化的研究已取得初步的进展,其确切的机制及寻找其治疗靶点仍需深入探讨。






