lncRNA通过ceRNA机制靶向Mir26a调节自噬促进心肌损伤
lncRNA通过ceRNA机制靶向Mir26a调节自噬促进心肌损伤
lncRNA在多种生物学过程中充当调控因子的作用,但是他在急性心肌梗塞(AMI)中的作用尚不清楚。今年九月刚发表在影响因子11.059的Autophagy杂志上的一篇文章探索了这一过程,并发现了lncRNA 2810403D21Rik/Mirf通过靶向Mir26a的ceRNA机制作为抗自噬分子发挥作用。
实验结果如下:
在心肌梗塞(MI)的小鼠模型中Mir26a表达下调(图1A);类似的,使用双氧水处理后的小鼠Mir26a表达也下调(图1B);沉默表达Mir26a降低了自噬体和自噬溶酶体的数量(图1C);并且LC3-II的表达下降,而SQSTM1/p62的表达升高(图1 D)。作者构建了Mir26a的海绵转基因小鼠模型,显著降低小鼠内源性Mir26a的表达(图1E),并降低了射血分数和分数缩短 (Figure 1F),这表明Mir26a敲除损伤了小鼠的左心室功能。此外,Mir26a敲除阻碍了自噬体形成导致心脏中自噬反应下降(图1G)。
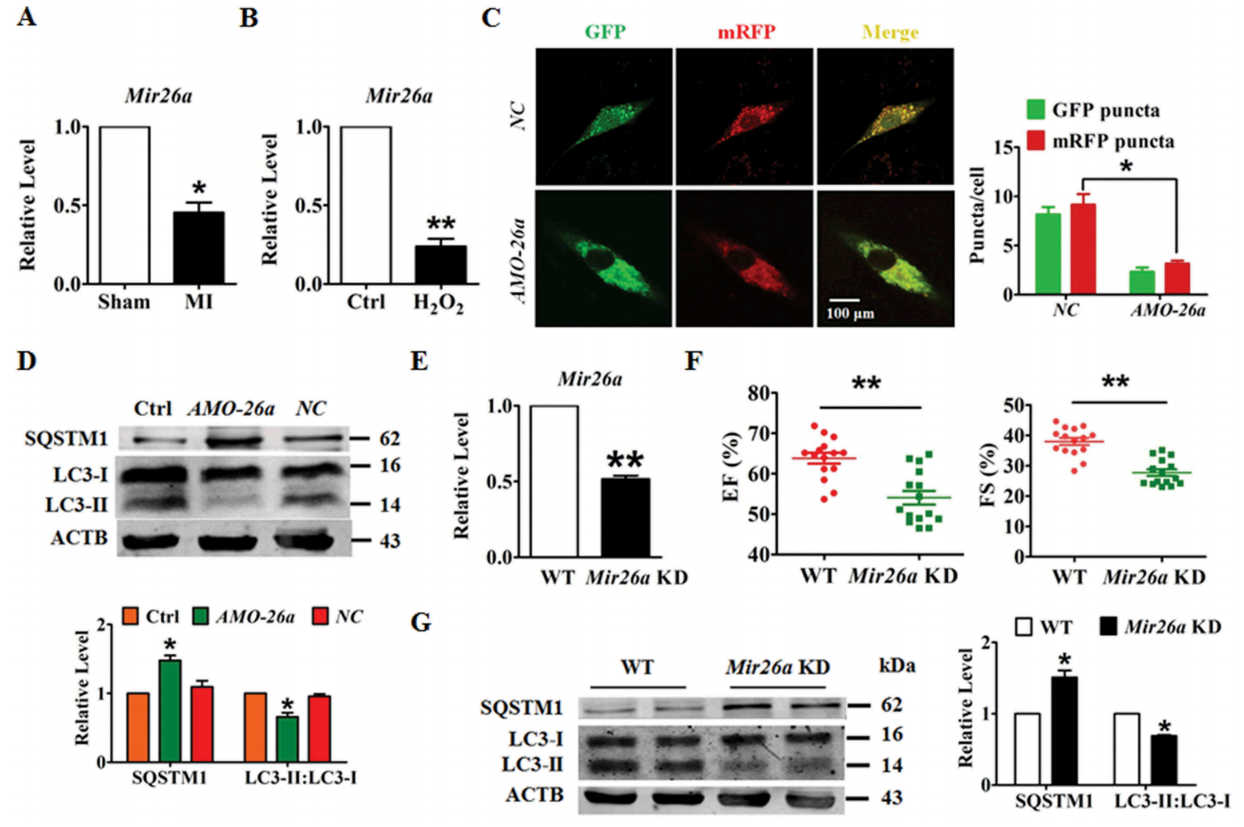
图1敲低Mir26a会减少自噬而损害心脏功能
另一方面,Mir26a的过表达减轻了双氧水对新生小鼠心肌细胞(NMCMs)的细胞活力的抑制作用,这种抑制作用被自噬拮抗剂3-MA所消除(图2 A);过表达Mir26a促进了自噬体的形成以及自噬体-溶酶体的融合,但3-MA可抑制这个作业(图2B);过表达Mir26a可改善心肌梗死模型小鼠的心脏功能,缩小梗死面积(图2C和D);透射电镜观察到Mir26a对心肌梗死小鼠自噬的促进作用(图2 E)。WB显示,过表达Mir26a可以促进MI小鼠自噬相关蛋白的表达(图2F)。
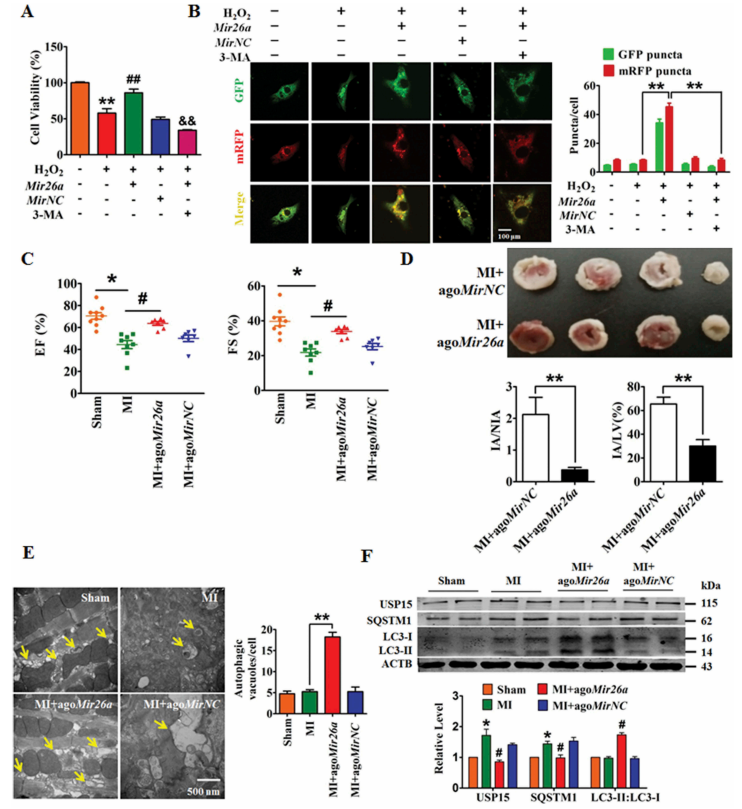
图2 Mir26a的强制表达通过激活自噬保护心肌细胞免受损伤
Targetscan预测分析发现编码Usp15的基因包含了Mir26a的种子序列,该基因在人类、小鼠和大鼠中具有广泛的保守性(图3A);有报道称Usp15拮抗患者成纤维细胞的线粒体吞噬作用,但作者发现在MI心脏的边缘区域和暴露于双眼水的心肌细胞中Usp15上调表达(图3B和C)。共转染Mir26a后,只有携带WT Usp15结合位点的荧光素酶载体或结合位点1突变的荧光素酶载体(mut-1)表现出荧光素酶活性抑制 (图3D)。Mir26a降低了USP15蛋白的水平,但AMO-26a却提高了USP15蛋白的水平,尽管它们均未影响Usp15的转录(图3E和F)。Mir26a KD小鼠中USP15的表达增加(图3G)。在NMCM中过表达Mir26a抑制了SQSTM1 / p62的表达,并促进了LC3-II,ATG7,ECN1 / Beclin1和ATG5的表达(图3H)。
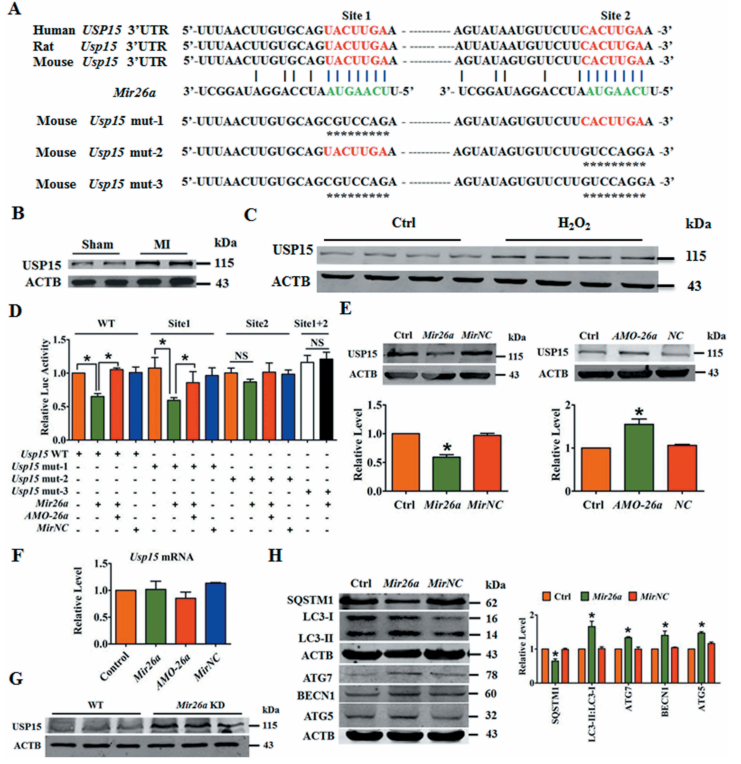
图3 Usp15是Mir26a的直接靶标
4、LncRNA 2810403D21Rik/Mirf能够结合并调控Mir26a的活性
使用miRanda数据库预测到候选的lncRNA AK007586,qRT-PCR显示它在MI模型小鼠中显著上调,将其命名为2810403D21Rik/Mirf,定位于细胞质(图4A和C);在双氧水刺进的NMCM中2810403D21Rik/Mirf的表达显著上调(图4B);过表达2810403D21Rik/Mirf抑制Mir26a的表达,沉默则相反(图4D和E);荧光素酶实验得出类似的结论(图4F-I);亲和分离实验表明,2810403D21Rik/Mirf与AGO2相互作用(图4J)。心肌细胞用生物素化的Mir26a转染,然后以生物素为基础做亲和力分离试验,其中通过qRT-PCR(图4L)和琼脂糖凝胶电泳(图4M)表明Mir26a可以拉下2810403D21Rik / Mirf,并且Mir26a对2810403D21Rik / Mirf的识别是序列特异性的。这些结果表明2810403D21Rik / Mirf与Mir26a和AGO2直接相互作用形成RISC并调节Mir26a的表达和活性。
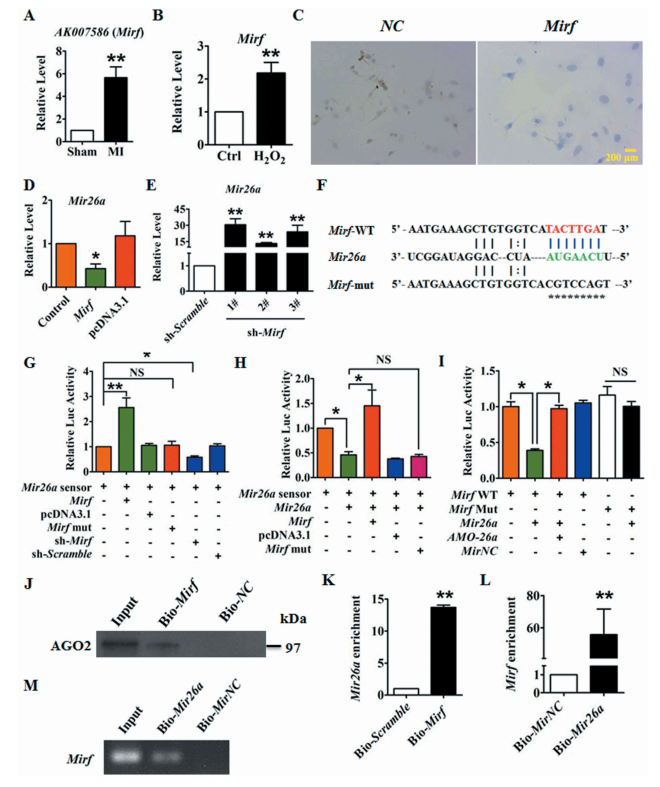
图4 LncRNA 2810403D21Rik/Mirf调控Mir26a的表达和活性
5、LncRNA 2810403D21Rik/Mirf通过Mir26a-Usp15轴调节自噬
2810403D21Rik/Mirf限制了Mir26a/Usp15轴的功能,从而抑制自噬,通过减轻内在的心脏保护活性而导致心肌损伤

图5 2810403D21Rik/Mirf通过调节Mir26a和Usp15调节自噬,促进NMCMs的心脏损伤
如图6所示, 2810403D21Rik/Mirf沉默通过激活Mir26a和自噬保护双氧水诱导的心肌损伤。
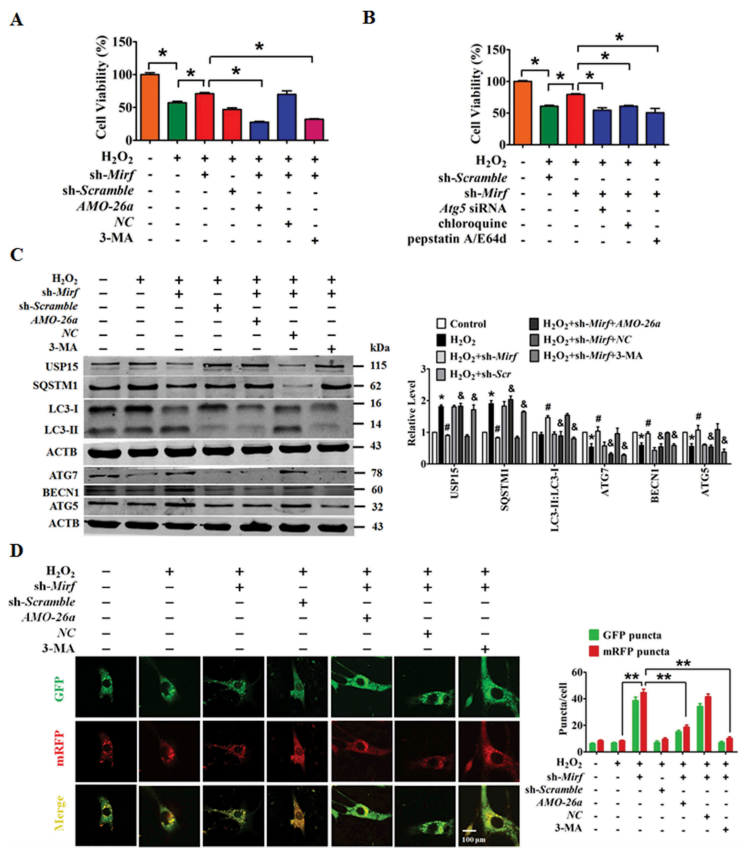
图6抑制2810403D21Rik / Mirf可以通过增加Mir26a的自噬调节来拮抗NMCM中双氧水诱导的损伤。
如图7所示,f-2810403D21Rik/Mirf可以模拟2810403D21Rik/Mirf对自噬和细胞损伤的作用,说明Mir26a结合位点是2810403D21Rik/Mirf的功能域。

图7 f-2810403D21Rik/Mirf的过表达通过抑制内源性Mir26a在体外培养的心肌细胞中引起心肌损伤
6、沉默2810403D21Rik/Mirf可以减轻心肌损伤,保护心肌梗死小鼠的心脏功能
如图8所示,2810403D21Rik/Mirf的沉默可调节自噬,对缺血性心功能损害具有保护作用。

图8 在MI小鼠模型中沉默2810403D21Rik / Mirf可减轻心肌损伤并保护心脏功能
简而言之,本文鉴定了一种新型的抗自噬lncRNA 2810403D21Rik / Mirf,它通过ceRNA机制来调节Mir26a的水平,从而加剧了缺血性心脏损伤。因此,调节2810403D21Rik / Mirf的表达可能是预防和治疗AMI的新方法。






