Circ Res:IL-10缺乏/炎症通过ILK富集抑制内皮祖细胞外泌体的心肌修复作用
近日,美国天普大学Raj Kishore教授研究组在Circulation Research杂志(影响因子15.862)上发表文章“Interleukin-10 Deficiency Alters Endothelial Progenitor Cell -Derived Exosome Reparative Effect on Myocardial Repair via Integrin-Linked Kinase Enrichment”,报道了ILK通过激活NF-κB途径在EPC-外泌体介导的炎症反应中的重要作用。敲低“发炎”外泌体中的ILK会减弱ILK富集的外泌体介导的炎症反应,抑制NF-κB途径的活化并增强缺血性心脏中EPC衍生的外泌体的修复活性。

该研究的新意:
1.IL-10基因敲除小鼠(全身性炎症)的外泌体失去了修复活性。
2.炎症会改变EPC外泌体的蛋白质组成,包括整合素连接激酶(ILK)的富集。
3.富含ILK的外泌体激活受体细胞中的NF-κB信号传导并诱导炎症基因表达。
4.小干扰RNA(siRNA)介导的IL-10 KO EPC中ILK的敲除可恢复其心脏修复能力
思维导图:
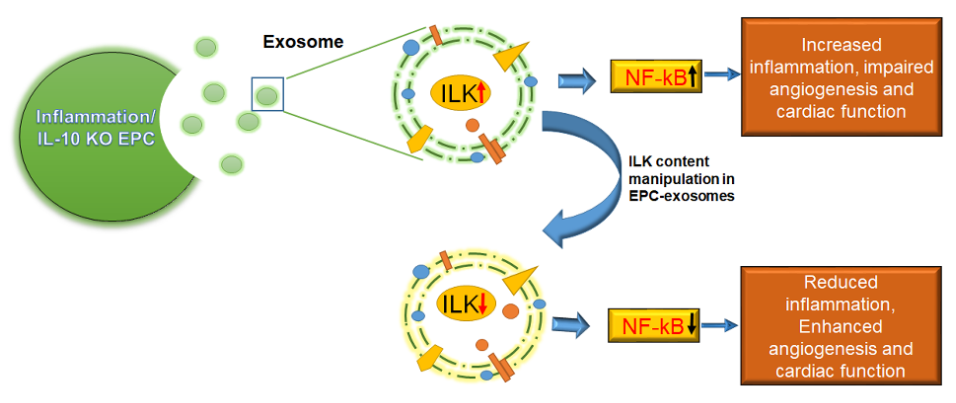
结果:
一、IL10KO EPC的外泌体在功能上是惰性的
为了评估在IL-10缺乏下EPC衍生的外泌体功能障碍,在AMI小鼠模型中进行了心肌内注射WT-EPC-Exo,IL-10KO EPC-Exo或PBS。与表现出修复活性的WT-EPC外泌体相比,IL-10缺陷型EPC的外泌体失去了心肌修复,血管生成和细胞存活的活性。
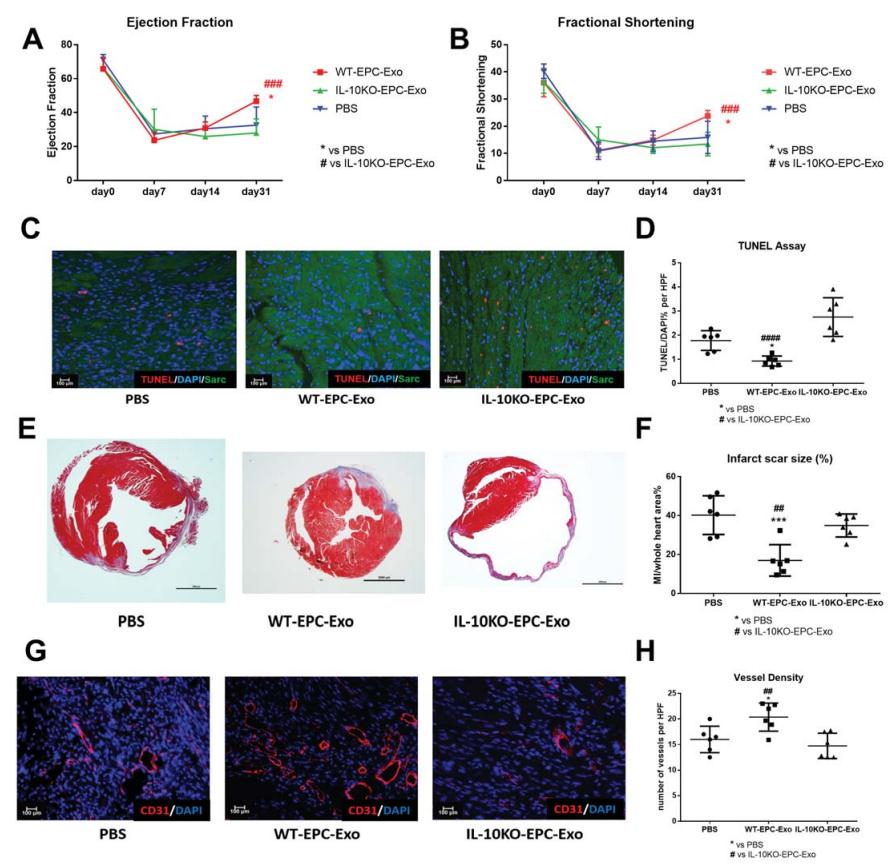
图1. IL-10KO-EPC-Exo不能改善MI后心脏修复
二、IL-10缺乏随着ILK的富集而改变了EPC外泌体蛋白质含量
为了了解外泌体之间的差异蛋白货物是否可能参与了明显相反的生物活性,进行了质谱分析以评估WT EPC-Exo和IL-10KO-EPC-Exo的蛋白质含量。结果发现,炎症刺激改变了细胞来源的外泌体蛋白含量,并且ILK通常富含发炎的外泌体,表明其在介导炎症反应中的潜在作用。
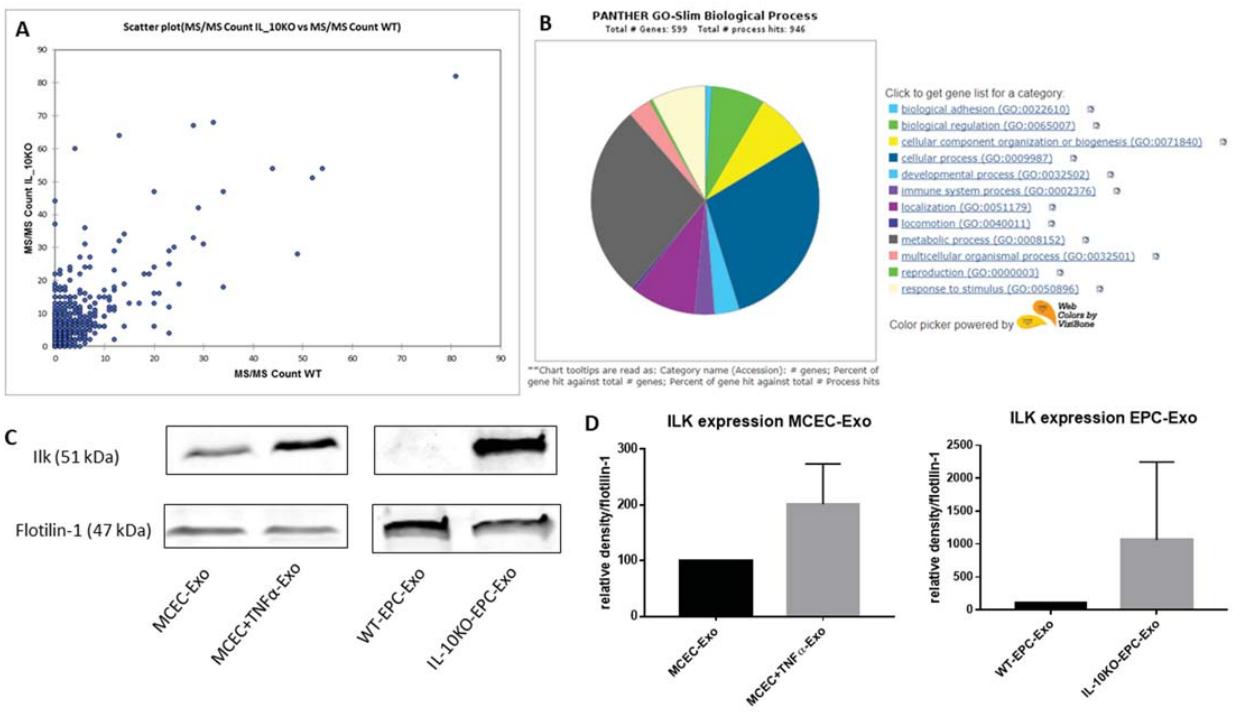
图2. IL-10KO-EPC-Exo和MCEC +TNFα-Exo中的ILK富集
三、富含ILK的外泌体激活受体细胞中的NF-κB途径
为了阐明富含ILK的外泌体在介导炎症反应中的作用,将MCEC用MCEC-Exo,MCEC +TNFα-Exo,PBS或TNFα处理。结果表明富含ILK的外泌体激活受体细胞中的NFκB途径,并通过增强炎症基因表达而增强了炎症反应。
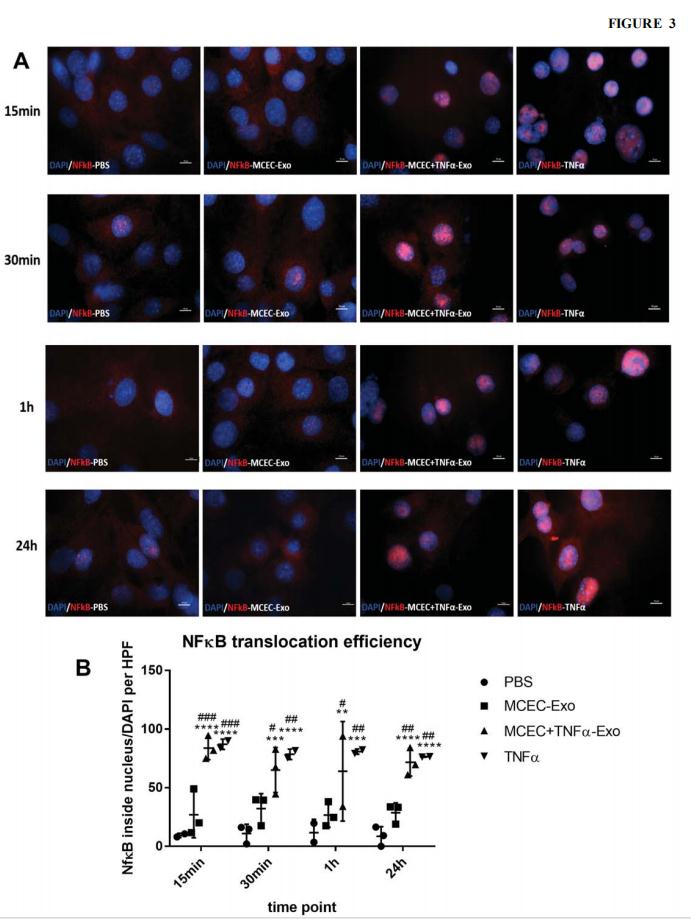
图3. MCEC +TNFα-Exo激活的NF-ĸB核易位
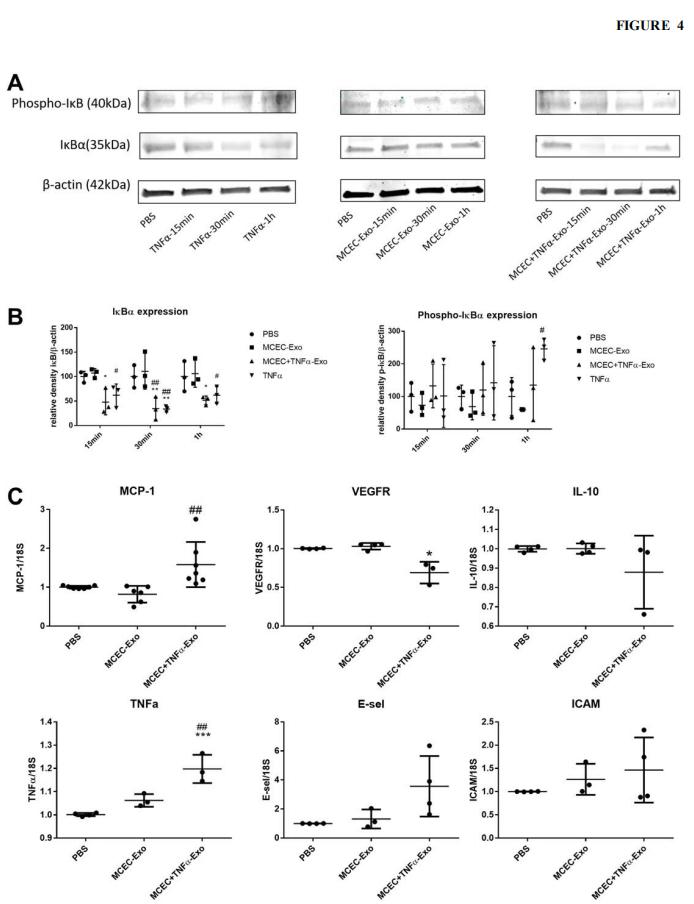
图4. MCEC +TNFα-Exo激活的NFκB信号通路
四、LK敲低外泌体显示减弱的NFκB激活作用
为了证实富含ILK的外泌体在激活受体细胞中炎症反应中的作用,在分离外泌体之前,将siRNA策略用于细胞中ILK的抑制。结果表明富含ILK的外泌体通过NFκB激活激活受体细胞的炎症反应。在外泌体中阻断ILK可成功抑制受体细胞中的NFκB活化和炎症反应。
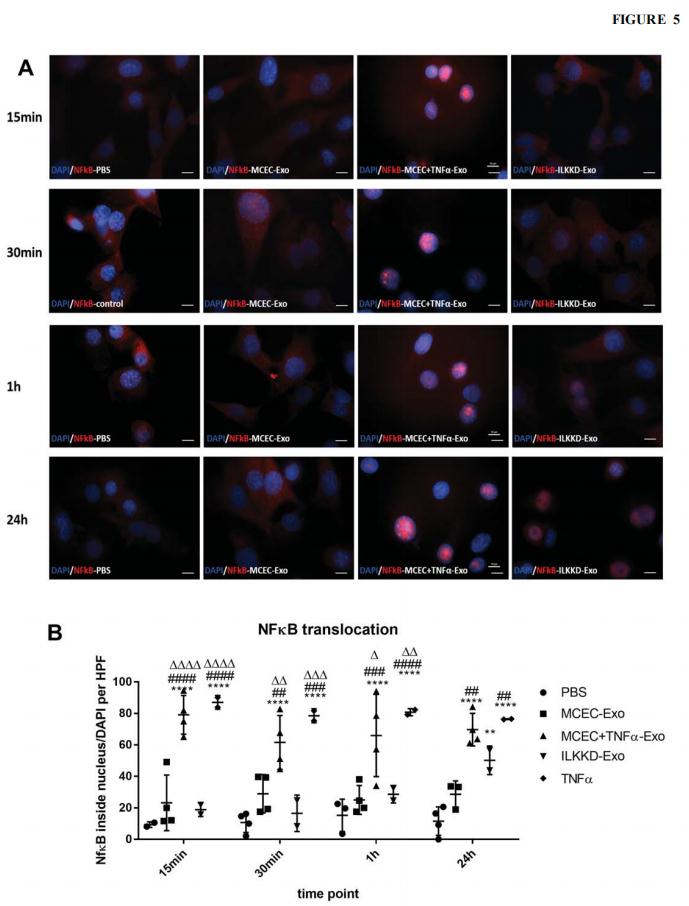
图5. ILK敲低外泌体抑制NF-ĸB核易位
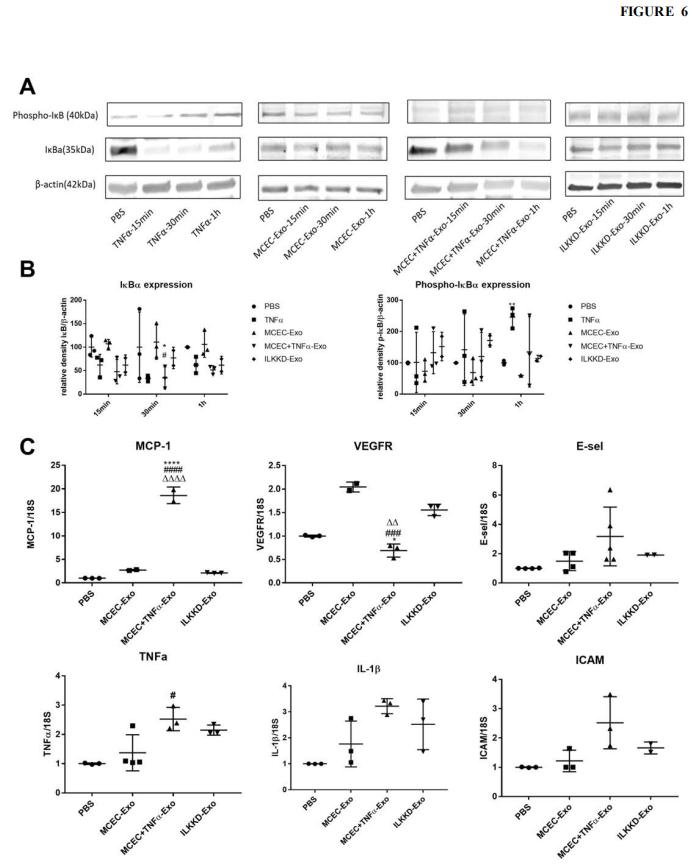
图6. ILK敲低的外泌体减弱了NFκB信号通路的激活
五、在体外,MCEC +TNFα-Exo中的ILK抑制挽救了它们的血管生成活性
先前实验已经证明IL-10KO-EPC-Exo在体外可抑制内皮细胞的管形成能力。用MCEC +TNFα-Exo处理观察到对EC小管发生的类似抑制作用。相反,ILKKD-Exo处理显着增强了内皮细胞的管形成和血管生成能力(图7A和7B)。因此,通过ILK敲低减弱了炎症性外泌体诱导的对血管生成的抑制作用。
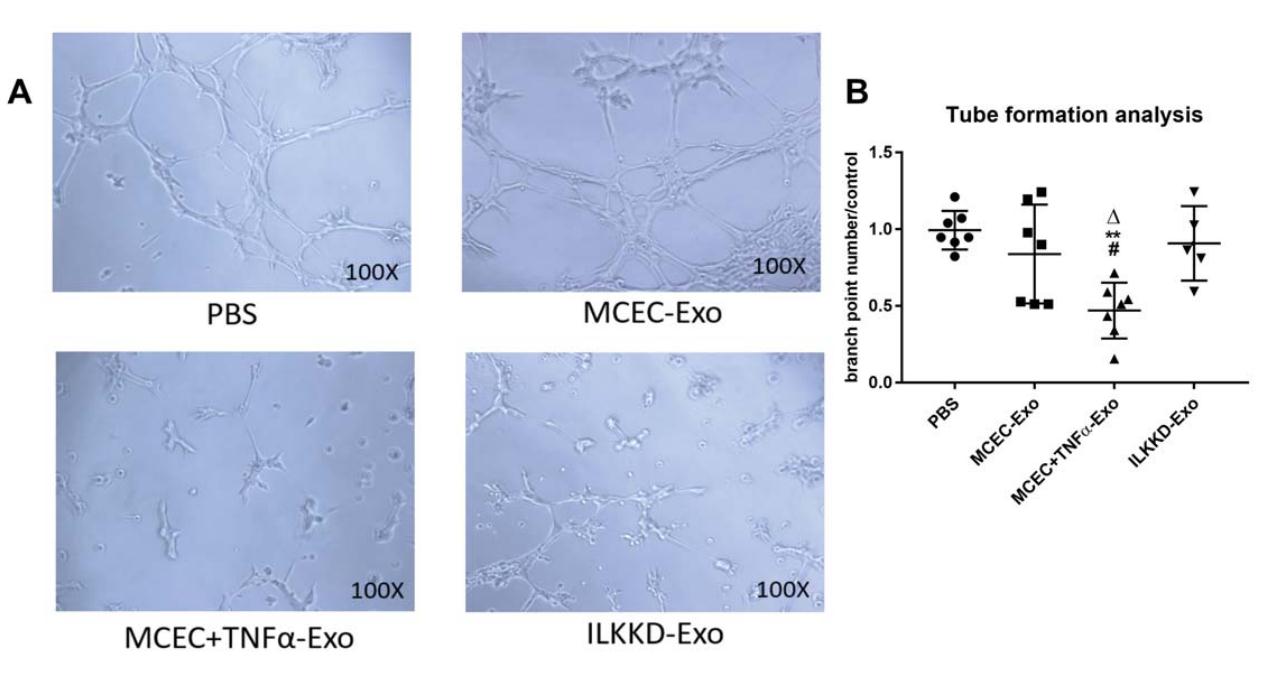
图7. MCEC +TNFα-Exo中的ILK抑制可挽救血管生成功能障碍
六、L-10KO-EPC-Exo中的ILK敲除在体内挽救了它们的修复活性
为了进一步研究ILK敲除外泌体在缺血性心脏修复中的功能,对IL-10KO-EPC进行了相同的siRNA策略,并收集了ILK-KD-EPC-Exo用于小鼠AMI模型的体内治疗,并直接比较了IL-10KO EPC的ILK-KD exo与IL10-KO-EPC-exo的特性。数据表明,ILK敲除成功地挽救了IL-10缺乏/炎症引起的EPC外泌体功能障碍。
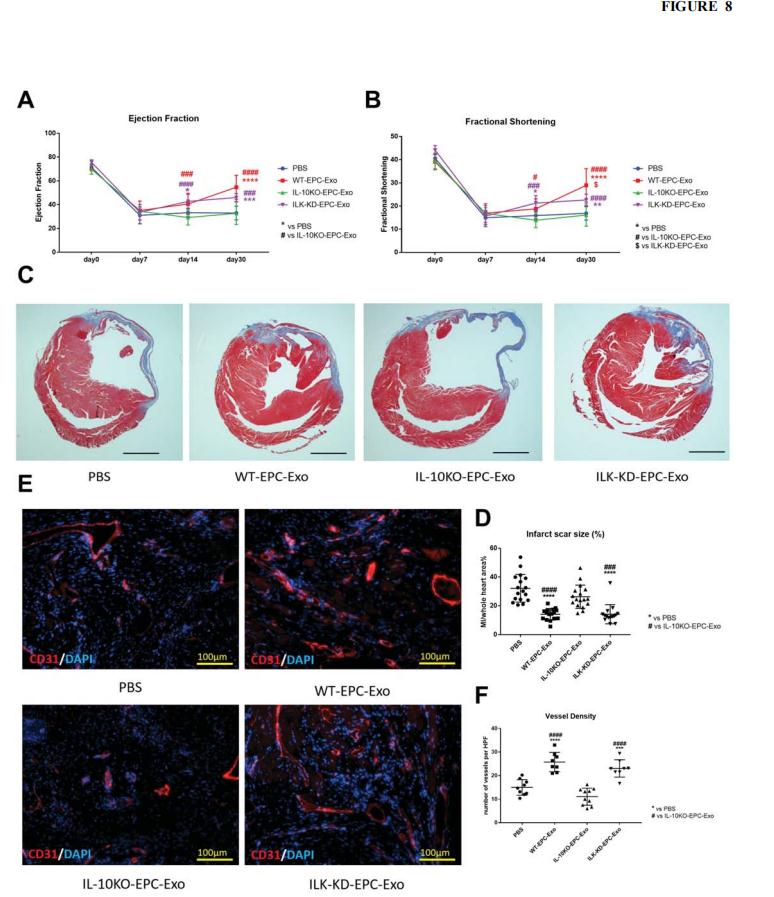
图8. IL-10KO-EPC-Exo挽救的心脏修复和再生功能障碍中的ILK降低
结论:
IL-10缺乏/发炎通过上调外泌体中ILK的富集和受体细胞中ILK介导的NF-ĸB途径的激活而改变了EPC衍生的外泌体功能,含量和对心肌修复的治疗作用,而外泌体中的ILK敲低减弱了NF-ĸB的激活并降低了炎症反应。该研究为炎症如何改变干细胞外泌体介导的心脏修复提供了新的认识,并将ILK鉴定为可改善基于祖细胞外泌体的心脏疗法的靶激酶。
参考文献:
Yue Y, Wang C, Benedict CL, Huang G, Truongcao MM, Roy R, Cimini M, Garikipati VNS, Cheng Z, Koch WJ, Kishore R. Interleukin-10 Deficiency Alters Endothelial Progenitor Cell -Derived Exosome Reparative Effect on Myocardial Repair via Integrin-Linked Kinase Enrichment. Circulation Research. 2019 Dec 9. doi: 10.1161/CIRCRESAHA.119.315829. [Epub ahead of print] IF=15.862






