外泌体-----外伤性ONFH细胞疗法的一种新选择
导语:
外泌体能够携带反映疾病状况的多种遗传分子,在细胞通讯过程中扮演着一个“快递员”的重要角色,由于其较低的免疫原性,致瘤性和更易于管理,因此外泌体已成为疾病细胞疗法的一种有前途的新选择。外伤性股骨头坏死(ONFH)是导致股骨头塌陷的一种情况,其主要治疗方法为全髋关节置换术,预后较差。但是外泌体却能为外伤性ONFH的治疗提供了一种可能的策略。
技术路线:
1.通过微阵列分析,筛选外伤性ONFH相关表达数据集获得差异表达基因(DEGs)和差异表达miRs,
2.收集外伤性和非外伤性外伤性脑脊液瘤患者,并进行随访。
3.纯化和鉴定了BM-MSCs来源的外泌体,然后与外泌体共培养HUVECs。
4.验证miR-224-3p在外伤性ONFH中的功能作用是通过异位表达、耗竭和再通过报告基因实验确定。
5.评估内皮细胞增殖、迁移、侵袭能力和血管生成
6.通过芯片分析验证在ONFH中miR-224-3p表达以及证实FIP200是miR-224-3p的靶基因。
7.验证外泌体mir -224- 3p对内皮细胞增殖、迁移、侵袭能力、血管生成和FIP200表达。
8.最后证明FIP200过表达促进了血管生成
研究结果:
1、BM-MSCs发现有间质表型
在光学显微镜下,观察到,BMMSCs通道4是同质漩涡的形状。流式细胞仪检测,积极的CD90率是97.4%,CD34是0.091%,表明BM-MSCs特定的间质表型,但没有造血表型。
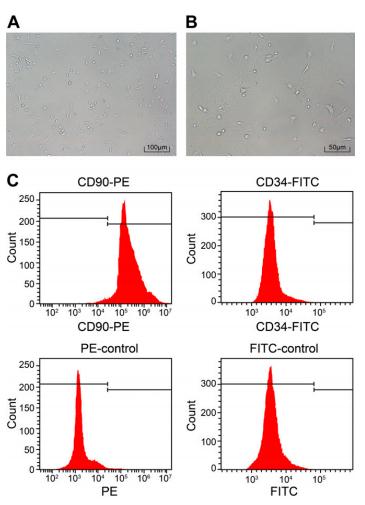
2、外泌体被血管内皮细胞内化
Nanosight分析表明,纯化的外泌体直径范围在30到100 nm之间。通过透射电镜发现,纯化后的外泌体呈圆形,直径约50 nm,说明囊泡的主要成分可能是外泌体。检测到外泌体特异性标志物CD9、CD63和CD81。孵育后,标记为绿色荧光的外泌体被内在化,主要定位于内皮细胞的胞质中,表明外泌体被血管内皮细胞内在化。
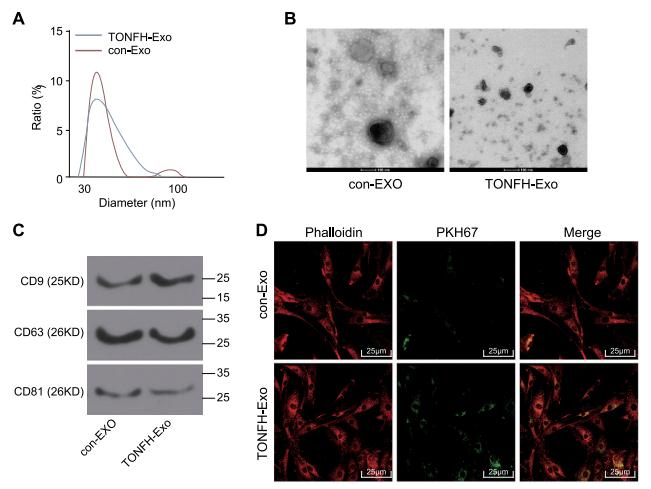
3、外伤性ONFH-Exo促进内皮细胞增殖和血管生成
将HUVECs分别与创伤性ONFH-Exo和con-Exo孵育,以确定外泌体对血管内皮细胞的影响。进行了EdU和mtt分析。外伤性ONFH-Exo较conExo明显促进内皮细胞增殖。此外,我们使用基质凝胶法评估血管生成能力。结果表明,与con-Exo相比,创伤ONFH-Exo增加分支点的数量和总管的长度。划痕试验表明,与con-Exo相比,创伤ONFH-Exo表现出显著增加区域的细胞迁移。与此同时,Transwell化验的结果表现出更多的入侵细胞创伤ONFH-Exo比con-Exo。最后,上述结果提示创伤性ONFH-Exo具有促进血管生成的作用。
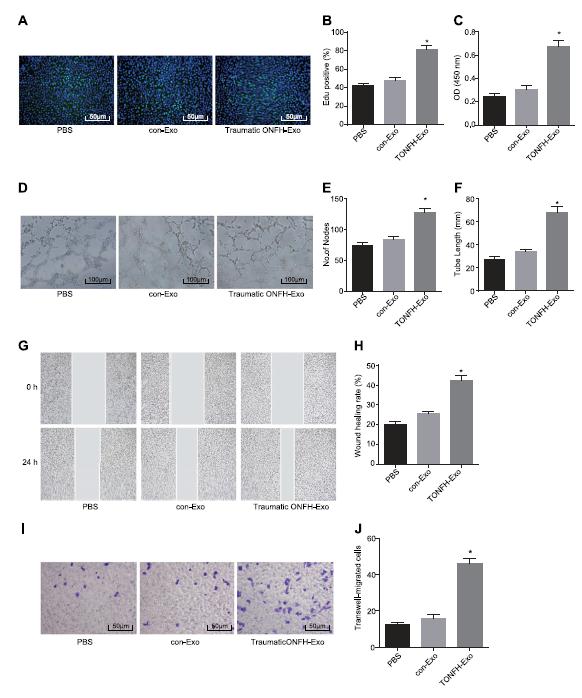
4、MiR-224-3p通过调节FIP200影响外伤性ONFH
从GSE89587表达数据集中筛选出差异表达的miRs(补充表S1),选取前10个下调的miRs绘制表达热点图。利用microRNA数据整合门户(mirDIP)、microRNA靶相互作用数据库(miRTarBase)和DIANA数据库预测miR224-3p的靶基因,分别得到267、113和1031个靶基因。此外,从外伤性ONFH的表达数据集GSE74089中筛选出631个DEGs。然后,将DEGs与miR-224-3p的靶基因进行比较,绘制Venn图。确认存在一个交集基因,即RB1诱导卷曲线圈1 (RB1CC1)。RBCC1在外伤性ONFH中的差异表达可被miR-224-3p调控。GSE74089表达数据的前30个DEGs的表达热图示外伤性ONFH患者RB1CC1表达高于对照组。定量RT-PCR (qRT-PCR)结果证实,外伤性ONFH前5个miRs (miR-4711-3p、-122-5p、-122-3p、-3191- 5p、-224-3p)表达下调,其中miR-224-3p表达最多,约为80%。RB1CC1也被称为FIP200。这些结果表明,miR-224-3p在创伤性ONFH中调节FIP200。
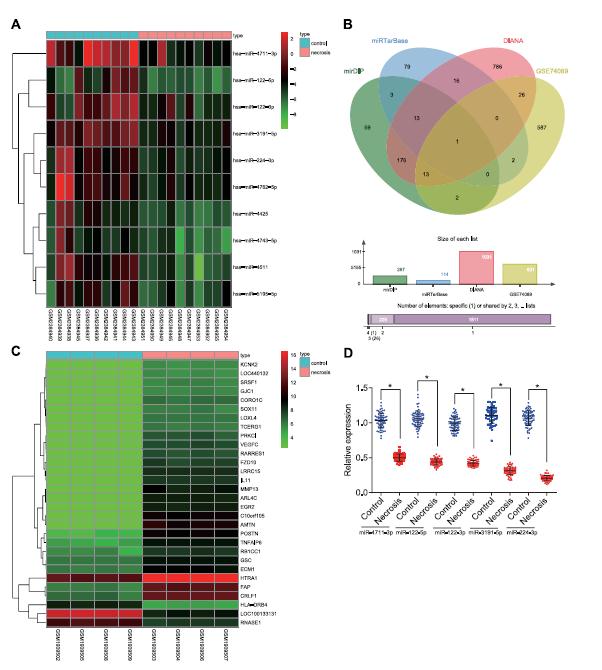
5、 miR-224-3p的下调促进创伤性ONFH血管生成
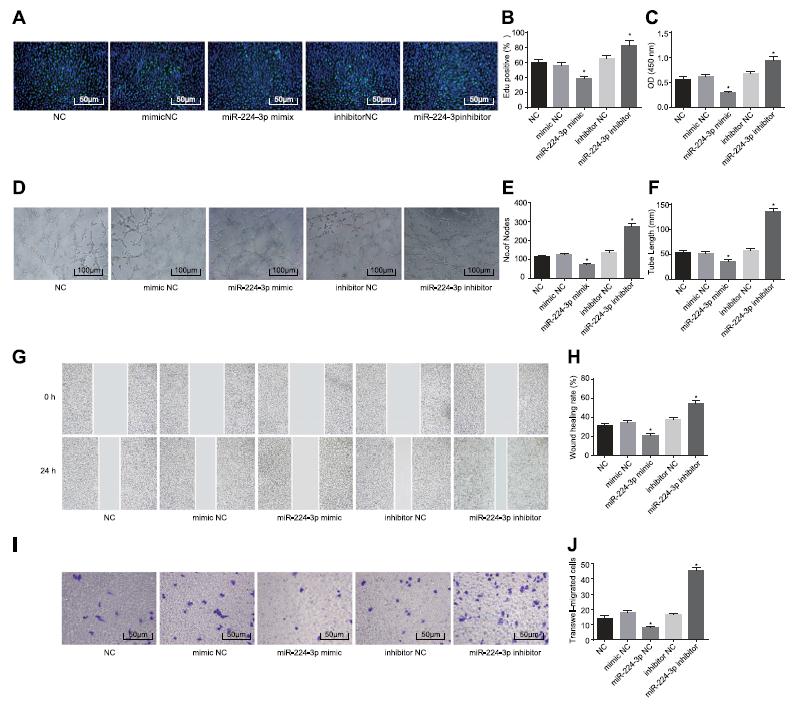
mir -224-3pmimic或抑制剂被送入HUVECs进行功能分析。模拟NC组、抑制剂NC组与对照组在edui阳性细胞、OD值、分支点数量、总管长度、细胞迁移面积、侵袭细胞数量等方面差异无统计学意义(P>0.05)。与对照组相比,EdU-positive细胞和内皮细胞减少的OD值mir - 224 - 3 - P模拟组,而他们显著增加mir - 224 - 3 - P抑制剂组(P< 0.05)。然而,管形成能力减少themir - 224 - 3 - pmimic集团,而这显然增加了mir - 224 - 3 - P抑制剂组(P<0.05)。相对于模拟数控,抑制剂数控,和对照组,miR-224-3p模拟组细胞迁移面积和侵袭细胞数量减少,而miR-224-3p抑制剂组则相反(P<0.05)。这些数据表明,miR-224-3p的下调可能促进创伤性ONFH血管生成。
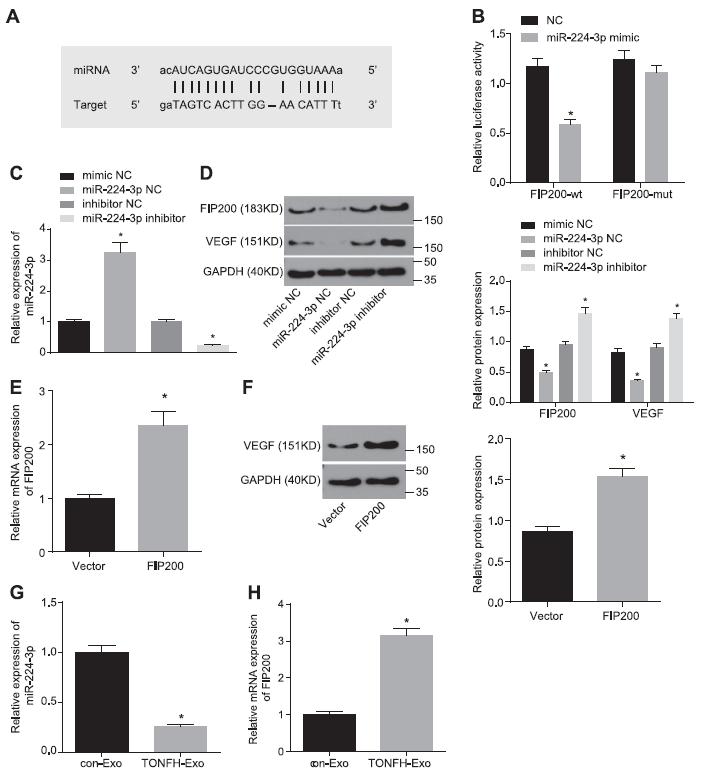
6、 MiR-224-3p下调通过靶向FIP200促进血管生成
在线预测网站揭示了MiR-224-3p和FIP200之间存在一个结合位点。双荧光素酶报告基因检测结果表明转染miR-224-3p和FIP200野生型后,荧光素酶活性显著下降。qRT-PCR结果显示,与mimicNC组相比,miR-224-3p mimic组miR-224-3p水平显著升高;然而,与抑制剂NC组相比,miR-224-3p抑制剂组对miR-224-3p表达有显著的抑制作用(P<0.05)。Western blot分析发现,与mimicNC相比,miR-224-3p模拟组中FIP200和VEGF表达被抑制,而miR-224-3p抑制剂组中FIP200和VEGF表达被促进(P<0.05)。构建FIP200过表达载体。qRT-PCR和Western blot结果显示,与载体组相比,FIP200过表达组FIP200和VEGF的表达明显增加(P<0.05)。与con- Exo组相比,外伤性ONFH-Exo组mir -224- 3p表达明显降低(P<0.05), FIP100表达升高(P<0.05)。这些结果表明miR-224-3p通过负调控FIP200抑制血管生成。
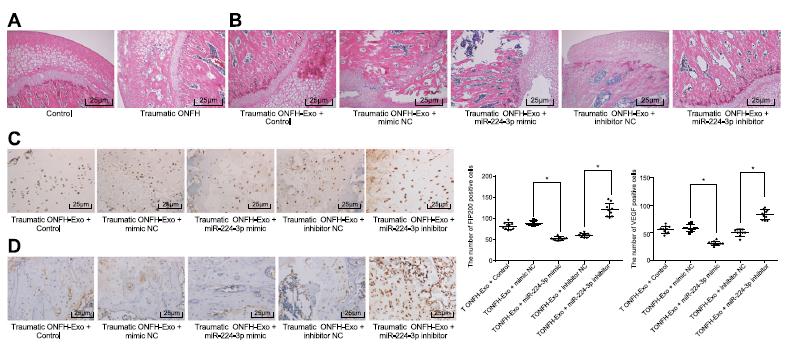
7、下调miR-224-3p可促进体内血管生成
建立了创伤性onfh大鼠模型,模型组股骨头组织内可见大面积坏死骨,空洞集中。对照组可见骨细胞和罕见的空洞。术后1天,从外伤性ONFH患者骨髓间充质干细胞肌注分离的外泌体和miR-224-3p inhibitor或mimic。HE染色显示,外伤性ONFH-Exo+ control组、外伤性ONFH-Exo+ mimicNC组、外伤性ONFH-Exo+抑制剂组中,股骨头以凋亡骨为主,活骨与死骨交替存在。外伤性ONFH-Exo + miR-224-3p模拟组主要表现为死骨和少量骨细胞,而外伤性ONFH-Exo + miR-224-3p抑制剂组主要表现为正常骨细胞,表现为罕见的死骨。外伤性ONFH-Exo +对照组、外伤性ONFH-Exo +模拟NC组和外伤性ONFH-Exo +抑制剂NC组FIP200和VEGF蛋白水平无明显差异(P>0.05)。FIP200的蛋白质含量和VEGF在创伤性显著降低ONFH-Exo + mir - 224 - 3 - P模仿组与创伤ONFH-Exo +模拟数控组相比,而他们是显著增加traumaticONFH-Exo + mir - 224 - 3 - P抑制剂组与创伤ONFH-Exo +抑制剂NC组(P<0.05)。这些研究结果表明,抑制mir - 224 - 3 - P表达ONFH老鼠体内促进血管生成。
总结:
mm - mscs分泌miR-224-3p抑制外泌体,调节外伤性ONFH血管生成。在ONFH中,miR-224-3p在来源于骨髓间充质干细胞的外泌体中的表达被下调,从而促进FIP200的表达,从而促进内皮细胞的血管生成、迁移和侵袭,促进VEGF的表达,进而促进血管生成以预防ONFH。骨髓间充质干细胞的外泌体作用于内皮细胞。外泌体中miR- 224-3p可抑制FIP200的表达,从而抑制内皮细胞的增殖、微血管生成和血管生成。当创伤性ONFH发生时,来自BM-MSCs的外泌体中miR-224-3p的表达下调,从而上调FIP200,促进内皮细胞的增殖、迁移和血管生成。
总之,骨髓间充质干细胞来源的外泌体miR-224-3p的下调,可促进内皮细胞增殖,迁移,侵袭能力,下调miR-224-3p水平通过上调FIP200促进创伤性ONFH的血管生成。此研究结果强烈建议mir - 224 - 3 - p可以作为一种潜在的分子治疗创伤性ONFH的目标,但需要更大的样本量的研究来验证目前的实验结果,以开发临床价值。






