铁死亡与胃癌的获得性耐药有什么关联?
Ferroptosis是一种调节细胞死亡的新形式,涉及铁依赖性脂质过氧化物(脂质-ROS)的积累,并导致细胞的致死性损害。然而,成纤维细胞(CAF)在调节脂类代谢以及癌细胞的铁死亡中的作用仍未被探索,并且仍然是谜。本研究采用质谱法筛选胃癌中与铁死亡相关的基因。通过超速离心分离外泌体,并通过RT-qPCR确定成纤维细胞(CAF)分泌的miRNA。使用Elastin诱导铁死亡,并通过测量脂质ROS,细胞活力和线粒体膜电位来评估铁死亡水平。更重要的是,顺铂和紫杉醇通过激活USP7 / hnRNPA1轴来促进成纤维细胞(CAF)分泌miR-522,从而导致ALOX15抑制并减少脂质-ROS在癌细胞中的蓄积,并最终导致化学敏感性降低。

结果一、GC中与铁死亡相关的关键基因的筛选
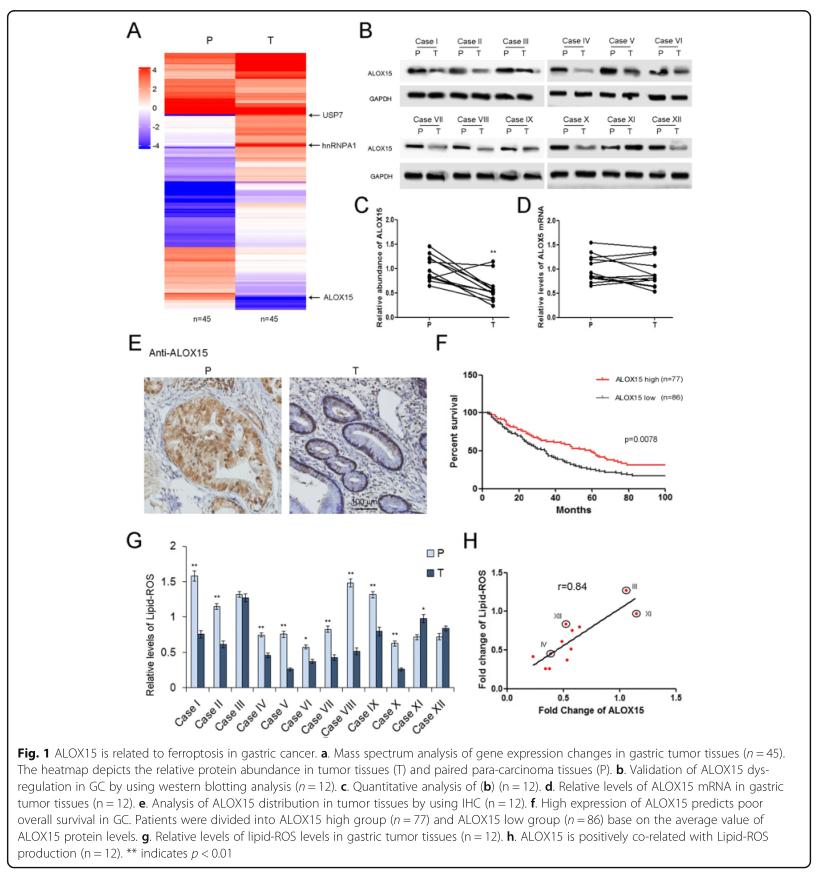
经过质谱比较GC特异性蛋白,与癌旁组织(P)相比,一组蛋白在GC肿瘤组织(T)中明显失调。 ALOX15是导致ferroptosis的关键基因之一,其表达量急剧下降,而肿瘤组织中USP7和hnRNPA1的水平明显升高。 然后,通过IHC分析检查了ALOX15的分布,并且ALOX15主要在癌旁组织的腺细胞中表达,并在腺瘤细胞中少量表达。而且,高水平的ALOX15蛋白还与胃癌患者更好的总体生存率(OS)相关,表明ALOX15在GC中起抗癌作用。这些数据表明,ALOX15在介导胃肿瘤中脂质-ROS产生中起关键作用。
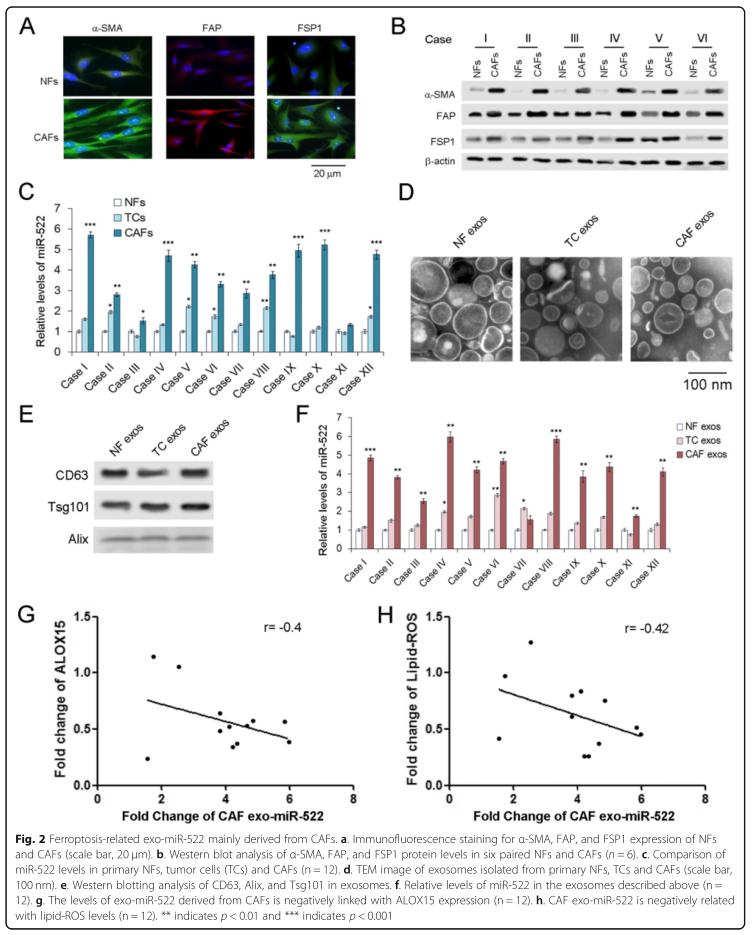
结果二、外泌体miR-522主要来源于肿瘤微环境中的CAF
与NFs相比,CAFs中所有CAFs,α-SMA,FAP和FSP1的标记均明显增加(。与肿瘤细胞和NFs相比,在CAF中发现了最高的miR-522浓度。在CAF外泌体中,miR-522的水平最高,其次是TC外泌体,而在三种外泌体中,CAF外泌体中miR-522的含量绝对占主导地位。源自CAF的外泌体miR-522也与ALOX15和Lipid-ROS呈负相关。这些数据表明,GC肿瘤微环境中的exo-miR-522主要由CAF分泌。
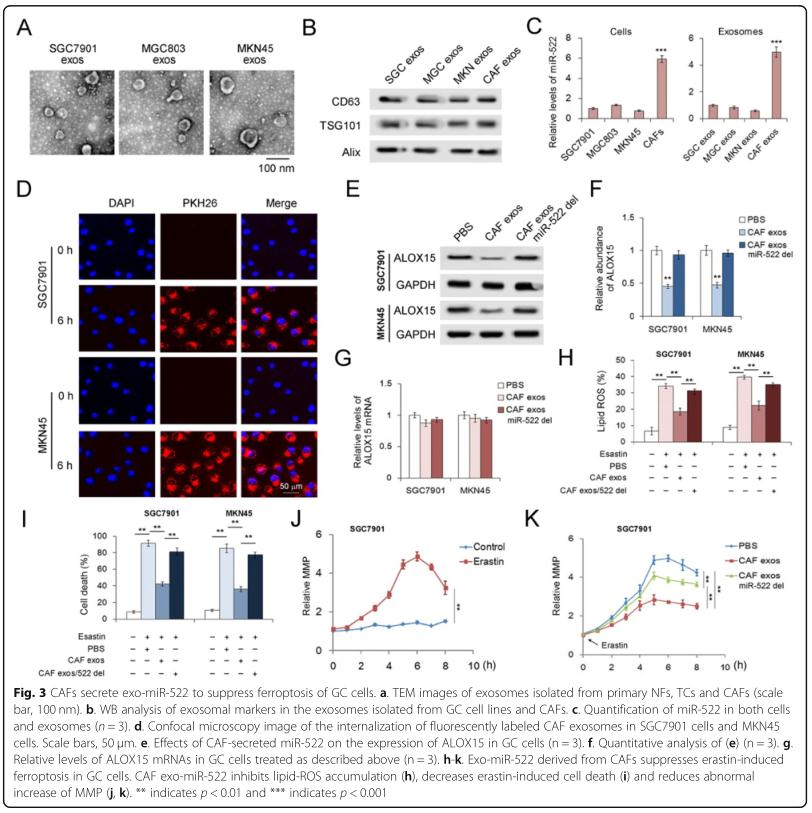
结果三、CAF分泌exo-miR-522抑制GC细胞的肥大化
为了测试源自CAF的exo-miR-522在调节癌细胞的铁死亡中的功能,分离了CAF外泌体并与人胃癌细胞系共培养。 CAF中miR-522的量是GC细胞系的6倍,并且在外泌体中观察到了相同的趋势。将CAF外泌体与GC细胞共培养,并在6h时在SGC7901细胞和MKN45细胞中均检测到PKH-26标记的CAF外泌体,这表明源自CAF的外泌体可以与GC细胞有效融合。 CAF外泌体可显着抑制GC细胞中ALOX15的表达,而不会影响依赖miR-522的ALOX15 mRNA的含量。此外,用抑素处理的SGC7901细胞显示出明显的线粒体膜电位(MMP)升高,CAF外泌体部分逆转了抑素对线粒体的损伤。总而言之,CAF分泌的exo-miR-522抑制了ALOX15的表达并下调了GC细胞中铁死亡的水平。
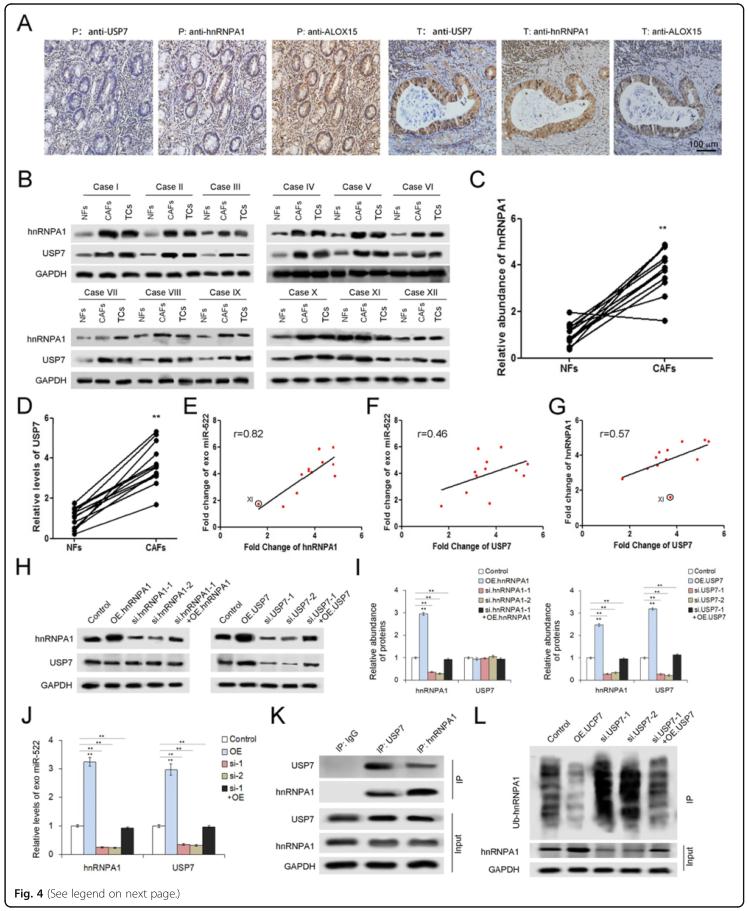
结果四、USP7通过稳定hnRNPA1促进miR-522分泌
据报道,hnRNP家族是将一系列mRNA和非编码RNA包装到外泌体中所必需的。在与成对的NF相比,hnRNPA1和USP7在CAF中高表达。此外,hnRNPA1和USP7的水平均与外泌体miR-522正相关,这表明USP7和hnRNPA1参与了CAFs的miR-522分泌。质粒的转染显着上调了hnRNPA1和USP7的表达,而siRNA的应用导致这两个基因的急剧减少。 hnRNPA1或USP7在CAFs中的过表达促进了miR-522向外泌体的包装。救援实验表明,过表达的hnRNPA1或USP7部分抵消了各自siRNA对exo-miR-522的作用。接下来,可以通过使用抗hnRNPA1抗体在免疫沉淀测定的产物中检测到USP7。此外,USP7还显示与hnRNA1泛素化水平呈负相关。总体而言, USP7通过去泛素化作用使CAF中的hnRNPA1稳定下来,导致外泌体miR-522的分泌增加。
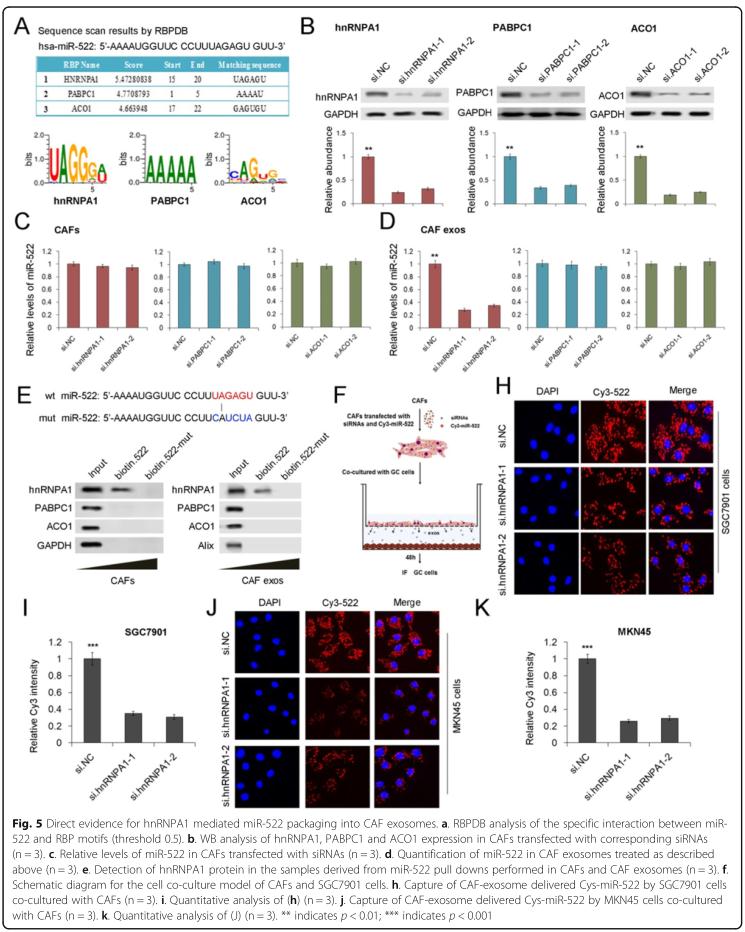
结果五、hnRNPA1直接介导miR-522包装到CAF衍生的外泌体中
为了进一步验证hnRNPA1在将miR-522选择性包装入外泌体中的作用,使用RBPDB(RBP特异性数据库,http://rbpdb.ccbr.utoronto.ca/)预测了潜在的miR-522结合蛋白。结果表明hnRNPA1在介导miR-522到CAF外泌体的包装中起着至关重要的作用。
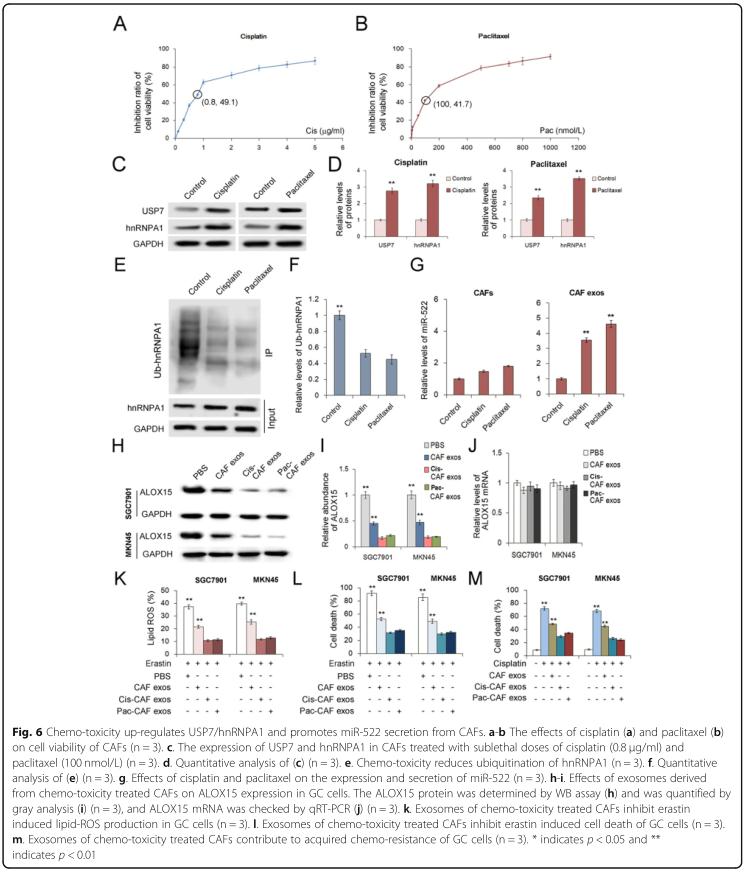
结果六、化学毒性通过激活USP7 / hnRNPA1途径促进CAF分泌miR-522
为了获得CAF中由化学疗法引起的损伤反应,作者检查了用亚致死剂量的顺铂或紫杉醇处理过的GC细胞。体外实验证明CAF外泌体有助于降低化疗期间的药物敏感性。
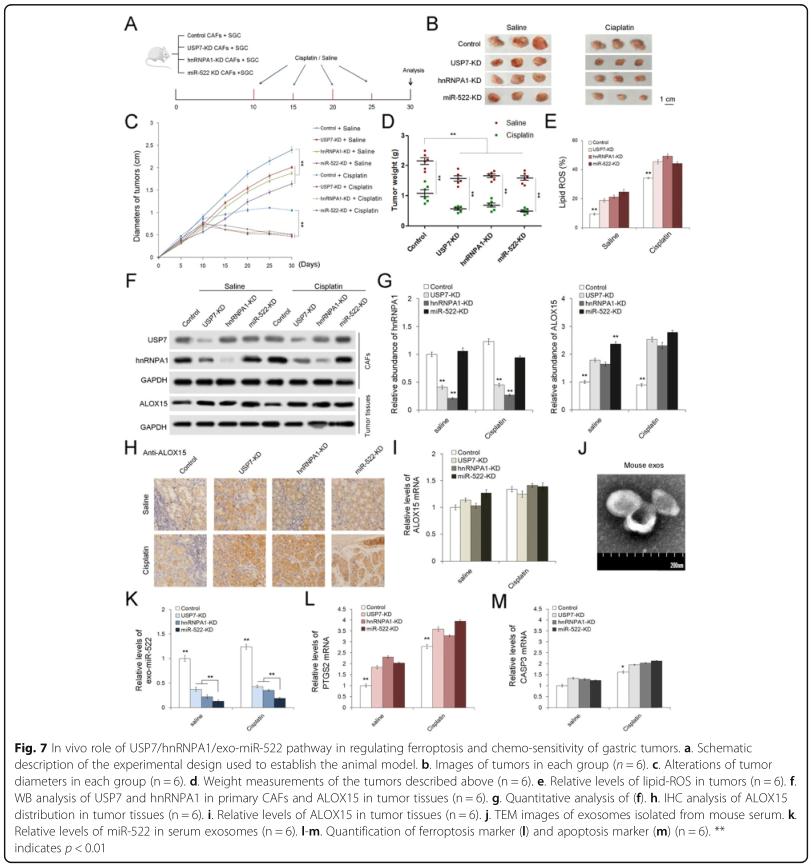
结果七、USP7 / hnRNPA1 / miR-522在调节胃肿瘤生长和化学敏感性中的体内作用
在体内评估了USP7 / hnRNPA1 / miR-522轴在影响肿瘤生长和化学治疗功效中的作用。结果表明USP7 / hnRNPA1促进CAF分泌exo-miR-522,降低肿瘤中的脂质ROS水平并促进肿瘤生长。此外,这些数据还表明,可以通过阻断miR-522的分泌来改善化疗药物的作用。
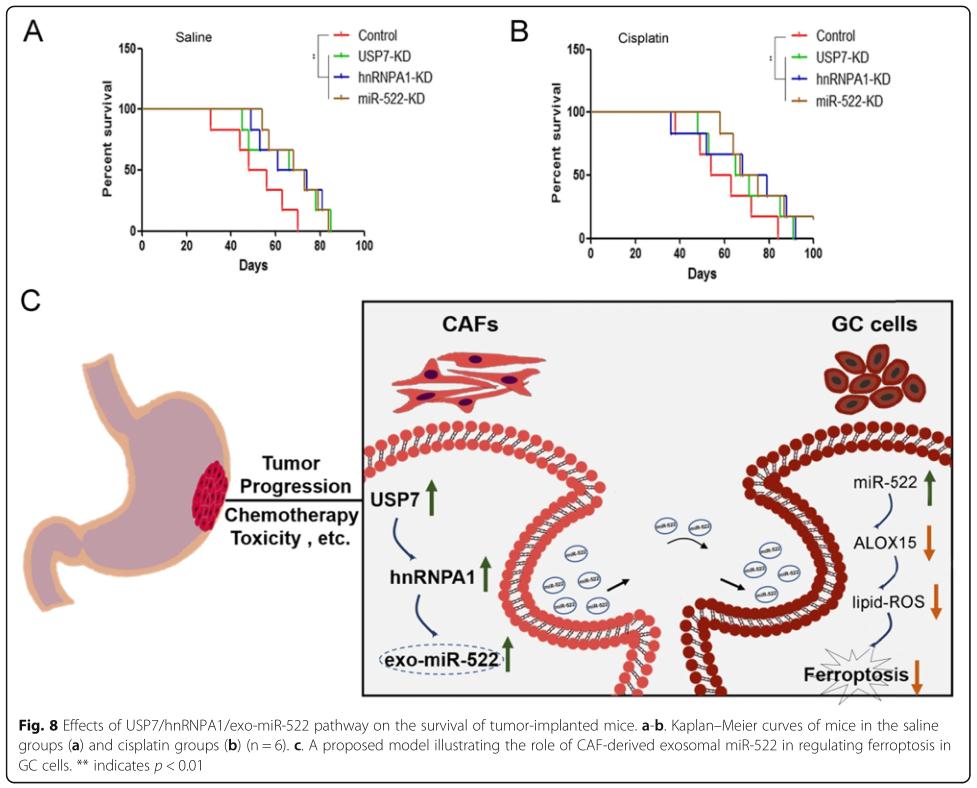
结果八、USP7 / hnRNPA1 / exo-miR-522途径对肿瘤植入小鼠存活的影响
USP7,hnRNPA1和miR-522的表达受抑制延长了荷瘤小鼠的生存期,顺铂组的小鼠比用盐水治疗的小鼠具有更好的生存期。 最后,作者提供了一个示意图来显示包括USP7,hnRNPA1,exo-miR-522和ALOX15在内的跨细胞信号通路在调节GC细胞的肥大作用中的生物学作用。
结论:
该研究阐明了TME衍生的外来体通过转运特殊的信号传递信息在调节癌细胞的铁死亡中的新作用。 这项研究还提供了一种新的想法,即通过阻止特定的miRNA包装到外泌体中来触发肿瘤中的细胞死亡。






