外泌体介导的CD44v6/C1QBP复合物与胰腺癌肝转移

胰管腺癌(PDAC)有明显的肝转移倾向。促癌分泌体通过外泌体传递和运输是转移前微环境形成和转移的关键。2021年4月发表于Gut(IF=19.819)的文章“Exosome-delivered CD44v6/C1QBP complex drives pancreatic cancer liver metastasis by promoting fibrotic liver microenvironment”对此进行了探究。本研究旨在探讨PDAC来源的外泌体(Pex)调控肝脏微环境、促进转移的潜在机制。Pex衍生的CD44v6/C1QBP复合物对于肝纤维化微环境和PDAC肝转移的形成是必不可少的。高表达的外泌体CD44v6和C1QBP是预测PDAC患者预后和肝转移的很有前途的生物标志物。
技术路线
结果
1)Pex诱导肝纤维化微环境,促进PDAC肝转移
从小鼠正常胰腺(Npex)和小鼠PDAC细胞分离的外泌体呈现典型的外泌体结构,大小约为50-150 nm(图1A,B)。进一步的western blot分析证实了分离的外泌体的存在(图1C)。为了确定Pex在PDAC肝转移中的作用,我们首先进行了“教育”程序,并进一步通过脾内注射建立了PDAC肝转移模型(图1D)。在“教育”过程后,STE和原子力显微镜(AFM)显示,与Npex组相比,Pex组小鼠的肝脏刚度显著增加(图1E,F)。此外,肝组织胶原密度增加(图1G),肝ECM明显重构(图1H,I)。同样,PDAC原位植入模型也显示原位肿瘤可增加肝脏胶原沉积。肝转移模型显示,与Npex组相比,Pex组肝转移更多,肝质量更高(图1J)。这些数据表明,Pex可以通过重构肝脏ECM来诱导肝纤维化微环境,促进PDAC肝转移。

2)Pex增强肝卫星细胞(HSCs)的活性
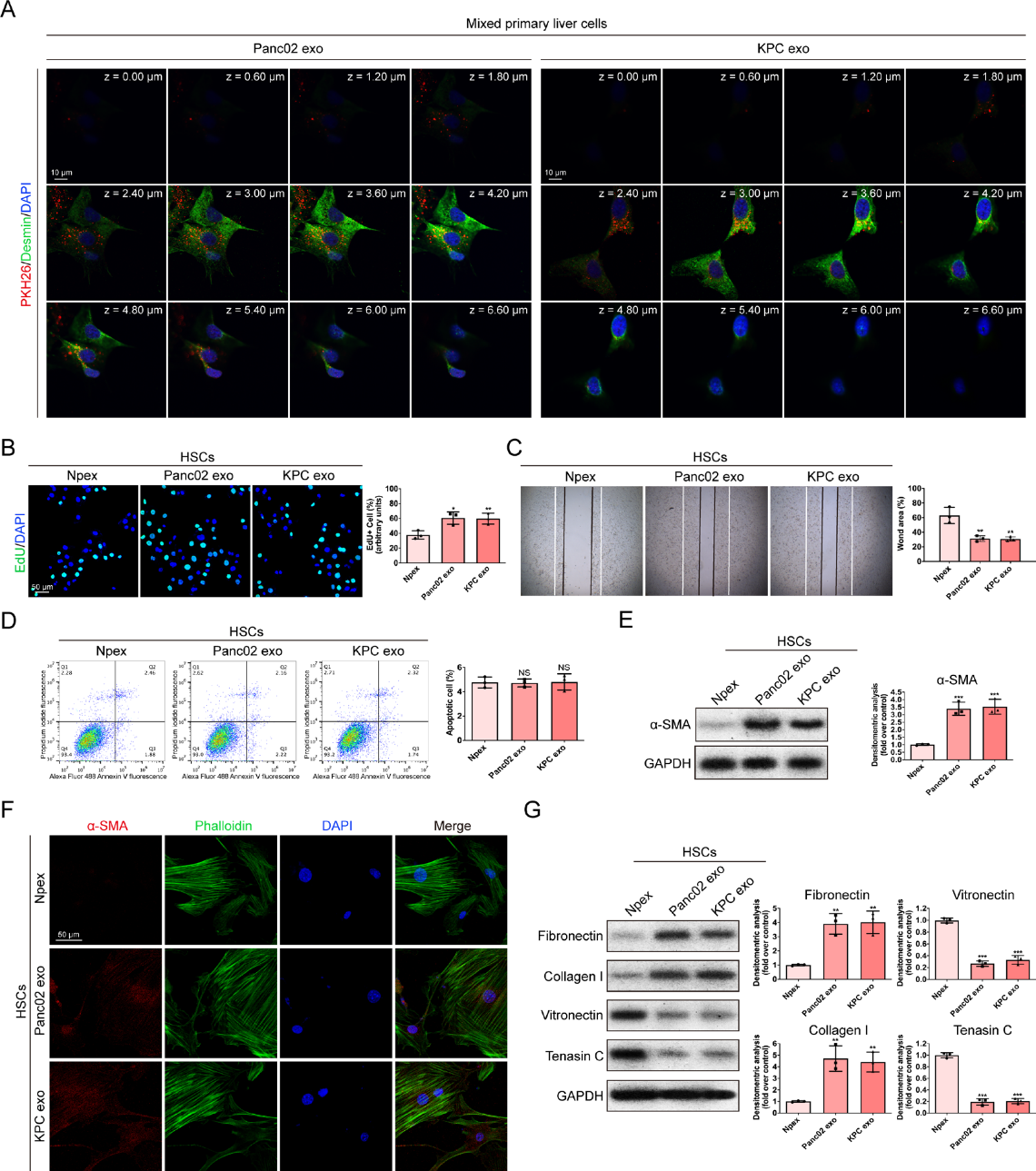
为了证实Pex的生物学功能,将原代小鼠肝细胞与Pex孵育,Pex被受体细胞吸收。然后使用免疫荧光染色对原发性肝细胞的类型进行表征,结果显示,desmin+HSCs和F4/80+Kupffer细胞吸收了Pex(图2A)。我们接下来研究了Pex对HSCs生物学行为的影响,发现Pex显著增强了HSCs的增殖和迁移能力(图2B和C)。Pex与Npex处理的HSCs的凋亡没有显著差异(图2D)。western blot和免疫荧光检测结果显示,Pex显著上调α-SMA的表达,说明Pex能促进HSC的活化(图2E和F)。我们观察到Pex可以通过下调vitronectin和tenascin C的表达,上调collagen I和fibronectin的表达来调节HSCs中的ECM分泌(图2G)。

3) IGF-1信号在Pex诱导的HSC活化和肝纤维化中至关重要
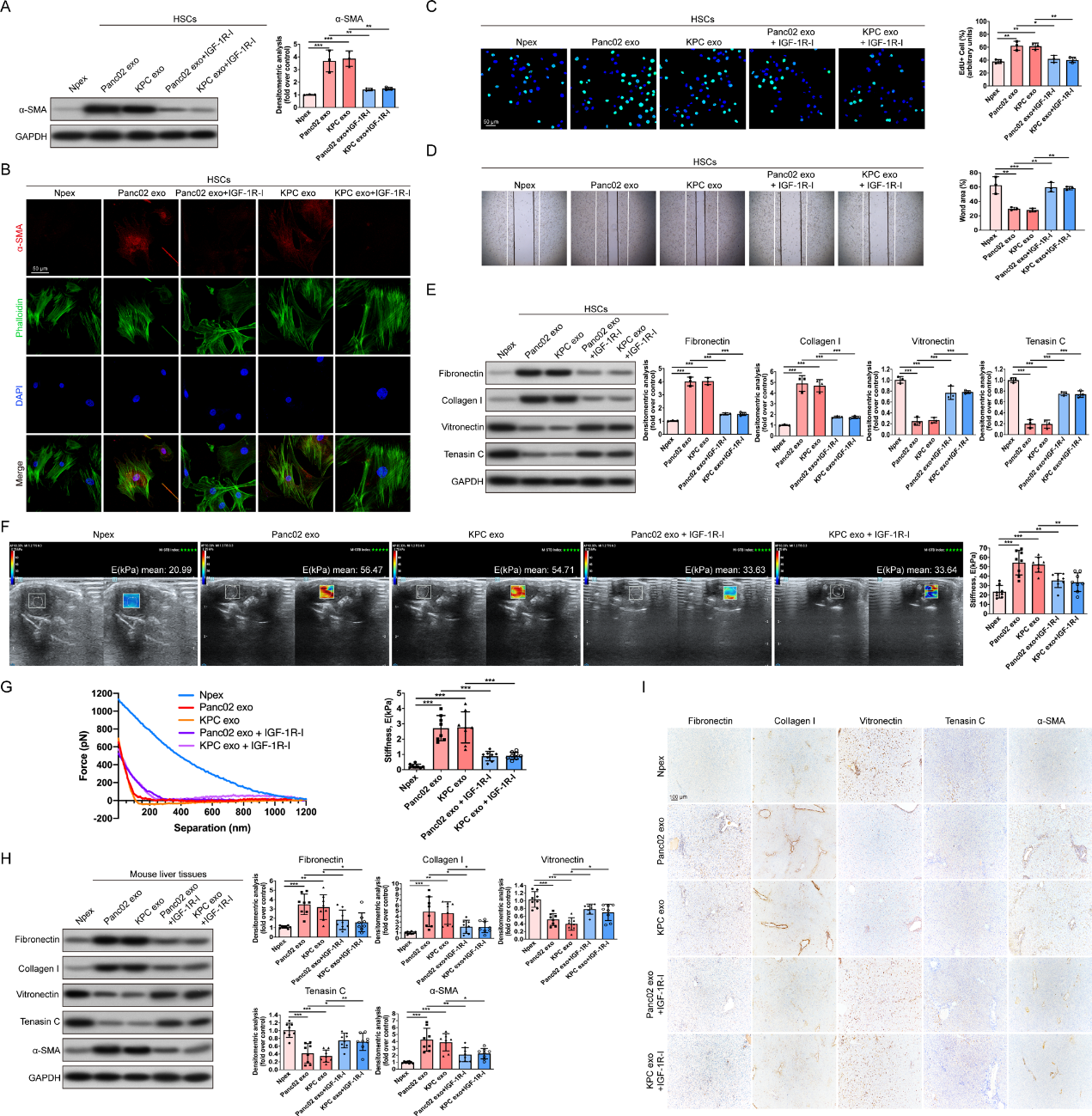
为了进一步探索Pex调控HSC行为的机制,我们比较了Pex和Npex组间的HSC的RNA测序基因表达谱(图3A)。在差异表达基因中,我们观察到41个重叠的上调基因在Pan02 exo组与Npex组和KPC exo组与Npex组之间存在部分交集(图3B)。主要涉及的基因参与细胞外空间、细胞外区域和ECM(图3C),表明Pex调节HSC的ECM分泌。此外,GO和KEGG通路分析显示,IGF-1及其下游PI3K/AKT是受Pex影响的排名最高的信号通路(图3D,E)。western blot分析支持了Pex显著增加HSC中IGF- 1R、IRS-1和AKT磷酸化的发现(图3F)。当使用IGF-1R抑制剂时,Pex诱导的p-IGF-1R、p-IRS-1和p- AKT的上调被阻断(图3G)。基于这些结果,我们推测IGF-1信号可能是介导Pex依赖的HSC活化的关键因素。与预期的一样,IGF-1R抑制剂抑制了Pex诱导的HSC的活化、增殖和迁移(图4A-D)。此外,IGF-1R抑制剂逆转了Pex诱导的HSC中ECM的产生(图4E)。我们的体内实验表明,IGF-1R抑制剂可以阻断Pex诱导的肝纤维化(图4F-I)。这些数据表明IGF-1信号在Pex诱导的肝纤维化中起重要作用。
4)Pex来源的CD44v6对于HSCs的激活是必要的,但不是充分的
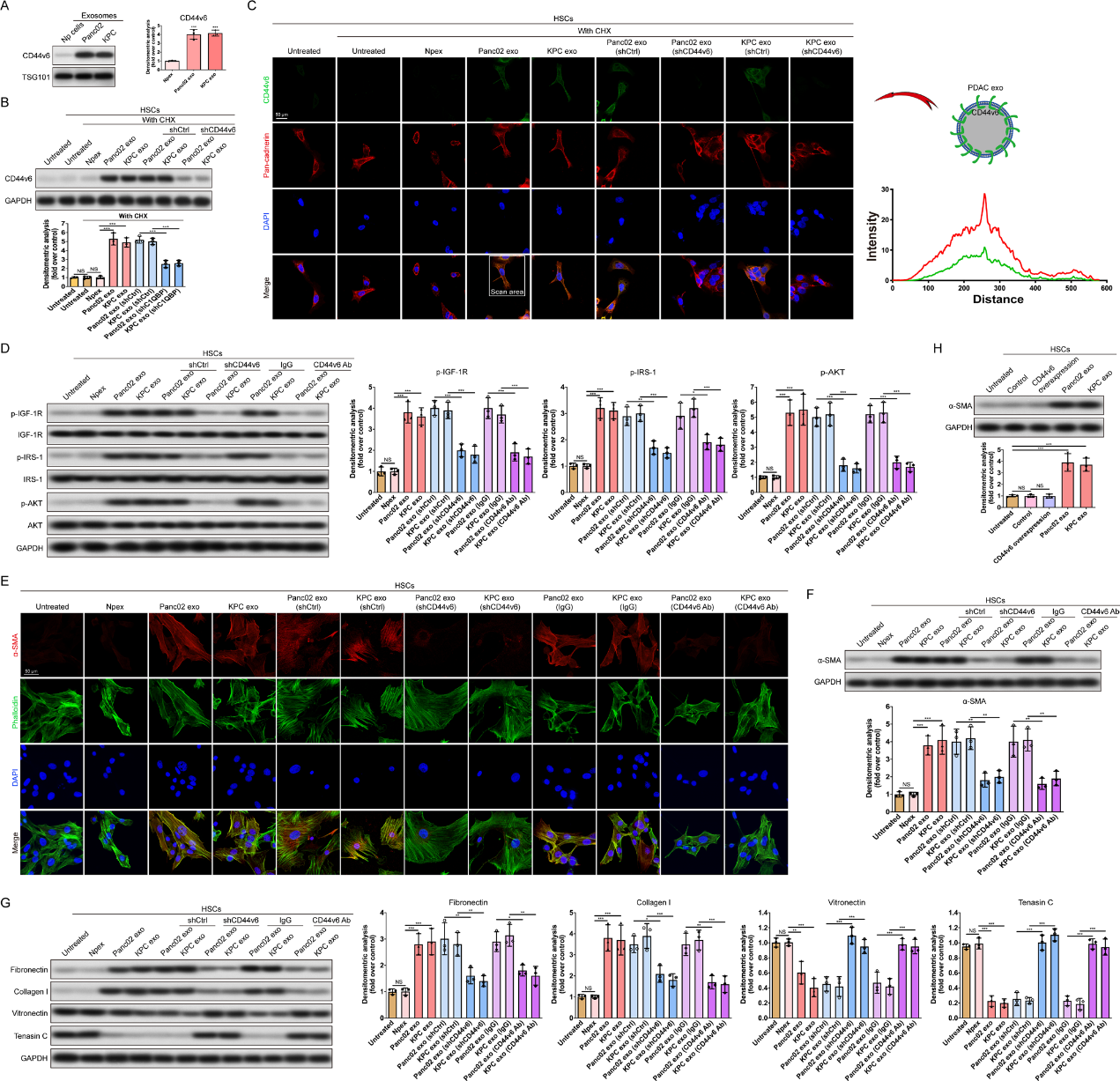
我们之前的研究揭示了CD44v6参与调控PDAC细胞的IGF-1通路。因此,我们首先验证了CD44v6在外泌体中的表达,发现CD44v6在Pex中的表达水平明显高于Npex(图5A)。为了研究CD44v6是否能够被传递到受体细胞中,我们采用蛋白合成抑制剂环己酰亚胺检测加入Pex后CD44v6的蛋白水平。western blot分析显示,加入Pex后,HSCs中CD44v6的表达水平明显增加(图5B)。与Npex-孵育的细胞相比,CD44v6的表达水平保持不变(图5B)。我们还进行了免疫荧光分析,检测出HSC膜中CD44v6与Pan-cadherin共定位(图5C)。这些结果表明,Pex可将CD44v6输送到HSC膜。此外,western blot检测表明,敲除CD44v6或使用抗CD44v6抗体的Pex强烈减弱了Pex诱导的IGF-1信号通路的激活(图5D)。同时,在CD44v6- kd Pex或CD44v6抗体的作用下,Pex诱导的HSC活化(图5E,F)、ECM重塑(图5G)的积极作用显著减少。为了阐明CD44v6在Pex诱导的HSC激活中的作用,我们进一步研究了过表达CD44v6在HSC中是否与Pex具有同样的激活HSC的作用。然而,过表达CD44v6并没有像预期的那样提高α-SMA的表达(图5H)。这些结果表明,CD44v6在Pex诱导的HSC激活中发挥了重要作用。
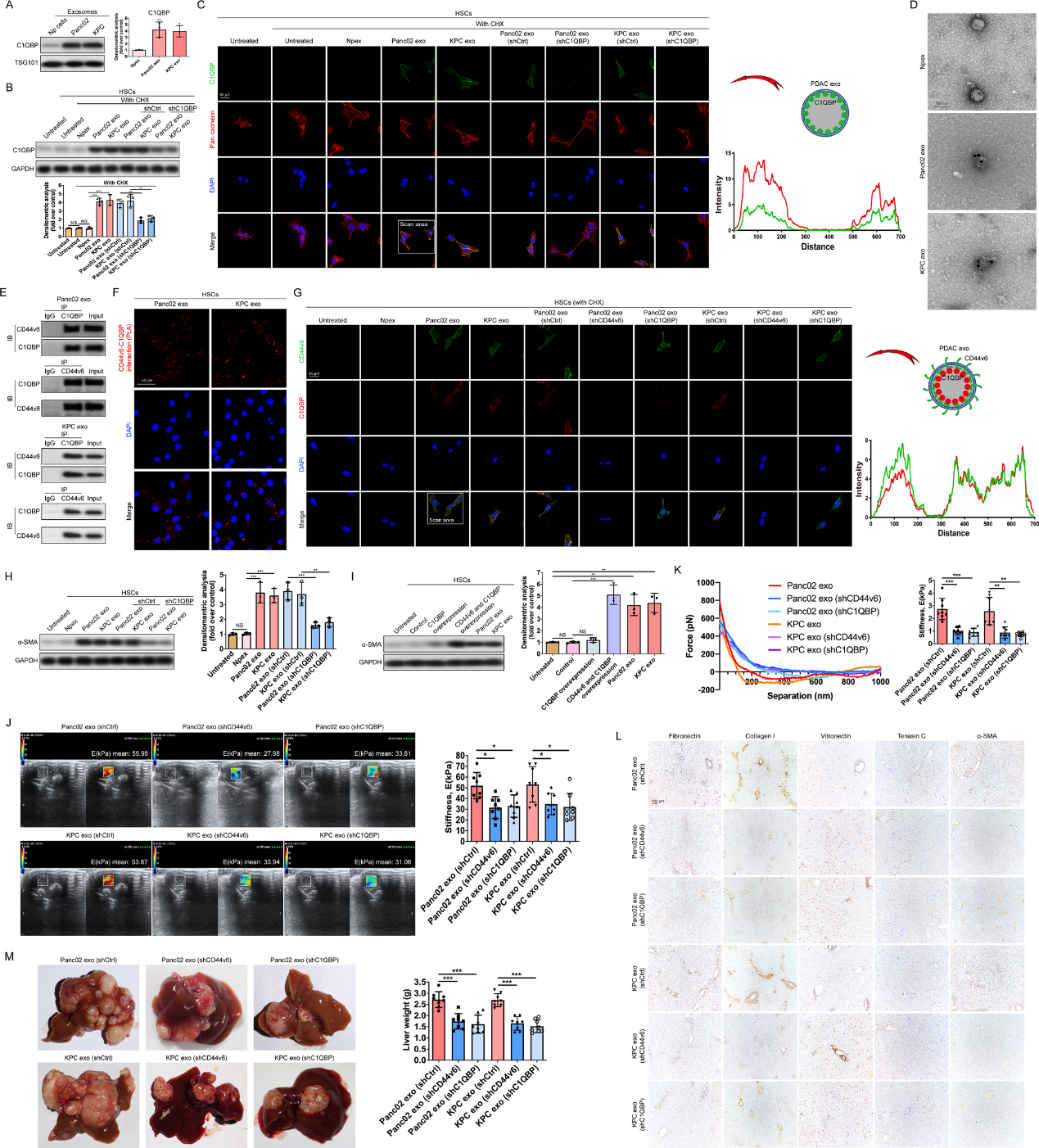
5)Pex衍生的CD44v6/C1QBP复合物介导了Pex对肝纤维化和PDAC肝转移的积极作用
此前,我们发现IGF-1可以通过诱导补体C1q结合蛋白(C1QBP)从细胞质转位到膜上,驱动CD44v6/C1QBP复合物的形成,从而激活IGF-1下游通路。因此,我们很想知道C1QBP是否通过CD44v6相互作用参与Pex诱导的HSC活化。我们的结果表明C1QBP在Pex中的表达明显高于Npex(图6A)。如图6B所示,C1QBP在Pex孵育的HSCs中表达高于Npex组。同时,与Pex处理的细胞相比,C1QBP-kd Pex处理HSCs后C1QBP蛋白水平显著降低(图6B)。与Pex转移的CD44v6在HSCs中的位置一致,膜中也检测到C1QBP,并与Pan-cadherin共定位(图6C)。这些数据表明,C1QBP可以通过Pex传递到HSCs膜。免疫电镜显示CD44v6和C1QBP在Pex中共表达(图6D)。同时过表达CD44v6和C1QBP后,Co- IP检测显示CD44v6和C1QBP在Pex中相互作用(图6E)。此外,通过近距离连接(图6F)和免疫荧光分析(图6G),我们发现了CD44v6和C1QBP在Pex孵化的HSCs膜上的结合。这些发现表明,CD44v6在传递外泌体CD44v6/C1QBP复合物中起重要作用。
与CD44v6敲低实验的结果相似,敲低Pex中的C1QBP在很大程度上抑制了α-SMA表达(图6H)。过表达C1QBP并没有上调α-SMA的表达(图6I)。同时过表达CD44v6和C1QBP显著增加了α-SMA的表达(图6I)。与我们的体外研究一致,敲除Pex中的CD44v6或C1QBP逆转了Pex诱导的HSC激活、肝脏刚度增加和肝脏ECM重塑的作用(图6J-L)。脾内注射肝转移模型(图6M)显示,与Pex组相比,注射了CD44v6- kd或C1QBP- kd的Pex组小鼠的肝转移减少。这些结果表明,Pex衍生的CD44v6/C1QBP复合物介导了Pex对肝纤维化和PDAC肝转移的积极作用。
6)Pex衍生的CD44v6和C1QBP的高表达预示着PDAC患者的肝转移和低生存率
采用免疫组化和western blot检测肝转移灶周围肝组织和正常肝组织的纤维化ECM微环境。与体内实验一致,纤维连接蛋白、I型胶原和α-SMA水平显著升高,而玻连蛋白和固生蛋白C水平下调(图7A,B)。接下来,我们研究了外泌体衍生CD44v6和C1QBP在PDAC患者中的预后价值。外泌体CD44v6和C1QBP在PDAC组织中的表达明显高于正常胰腺组织(图7C)。此外,有肝转移的PDAC患者外泌体CD44v6和C1QBP的表达明显高于无肝转移的PDAC患者(图7C)。免疫电镜显示,CD44v6和C1QBP在PDAC组织来源的EVs中共表达(图7D)。Pex中CD44v6和C1QBP高表达的患者比其他患者更容易发生肝转移 (图7E)。此外,生存分析显示,EV中CD44v6和C1QBP高表达的患者的生存结局明显较差(图7F)。循环外泌体的随访数据也显示了一致的结果。PDAC患者中循环外泌体CD44v6和C1QBP的表达明显高于健康对照组(图7G), PDAC伴有肝转移的患者中循环外泌体CD44v6和C1QBP的表达明显高于无肝转移的患者(图7G)。免疫电子显微镜显示,CD44v6和C1QBP在PDAC患者的循环外泌体中共表达(图7H)。高循环外泌体表达CD44v6和C1QBP的患者比其他患者更容易发生肝转移 (图7I)。然而,高表达循环外泌体CD44v6和C1QBP的患者生存率明显较差(图7J)。总之,我们的研究结果证实了CD44v6和C1QBP在组织源性EV和循环外泌体中的表达可以预测PDAC患者的预后和肝转移。
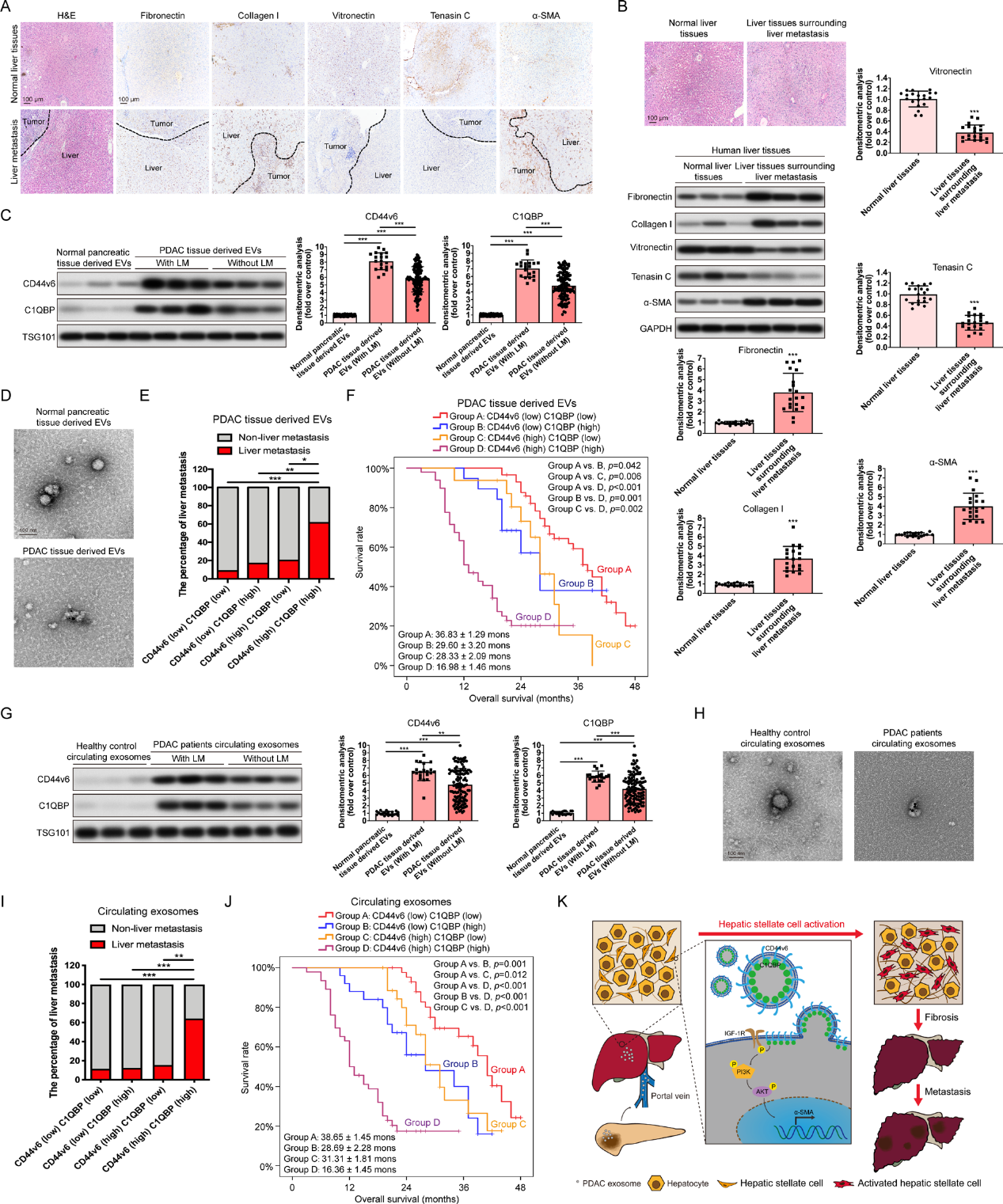
结论:我们揭示了原代PDAC细胞和HSCs之间通过PDAC来源的外泌体进行远距离的细胞通信。此外,Pex通过促进肝纤维化微环境的形成来指示肝特异性转移。更重要的是,我们发现外泌体CD44v6/C1QBP复合物传递到HSC的质膜上诱导IGF-1信号通路的激活。外泌体CD44v6和C1QBP可能是预测PDAC患者预后的有前途的生物标志物,也是治疗PDAC肝转移的潜在靶点。






