癌细胞膜损伤修复机制
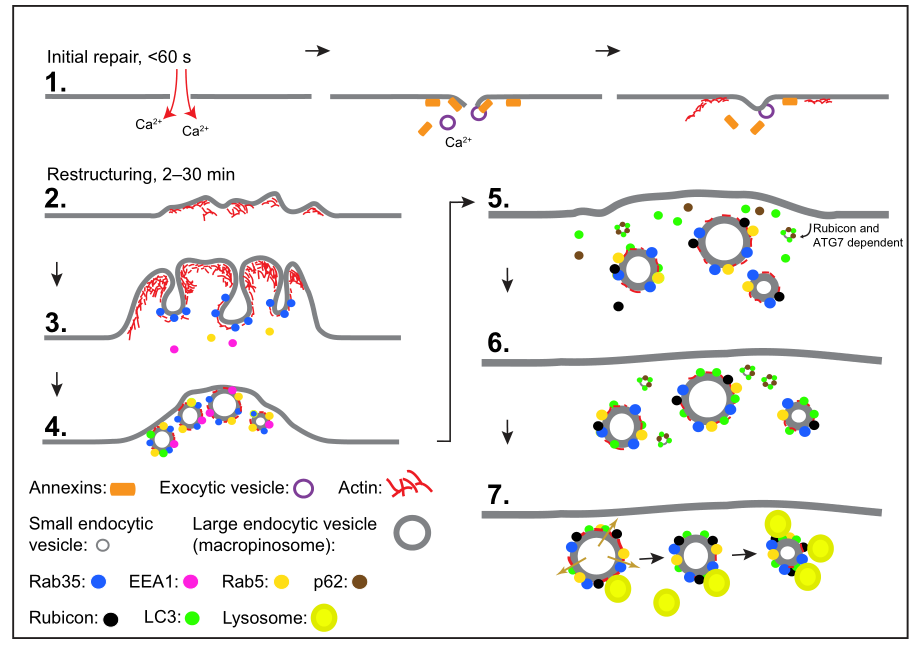
质膜塑造并保护真核细胞免受周围环境的影响,对细胞生命至关重要。尽管重新密封受损膜的初始修复机制已经很好地建立,但关于细胞如何在重建受损膜后恢复体内平衡知之甚少。今年7月发表于《SCIENCE ADVANCES》的一篇研究表明,细胞通过激活与巨胞饮作用相关的蛋白质来响应质膜损伤,特别是在受损的膜上。在膜重新密封之后,细胞形成源自修复部位的、LC3B蛋白阳性的胞吞小体。此过程独立于 ULK1、ATG13 和 WIPI2,但依赖于 ATG7、p62 和 Rubicon。内化的胞吞小体在细胞质中收缩,可能是通过渗透排出,并最终与溶酶体融合。这是一种与非经典自噬相结合的巨胞饮作用,研究者将其称为 LC3 相关巨胞饮作用 (LAM),其功能是从质膜上去除受损物质并在损伤时恢复膜的完整性。接下来我们来看一下具体研究方法及结果:
一、 LC3 阳性囊泡在质膜损伤后在修复部位积聚
用激光照射癌细胞MCF7,致使细胞膜上形成小孔。使用膜不可渗透的 FM1-43 染料测量膜完整性,发现在Ca 2+存在下,细胞能够在 20 到 30s内修复它们的质膜(Fig. 1, A and B, left);在缺乏 Ca 2+ 的培养基中受损的细胞无法修复并继续吸收细胞不可渗透的染料(Fig. 1B,right)。
使用稳定表达融合蛋白增强型绿色荧光蛋白 (eGFP)-LC3的MCF7细胞研究激光照射后自噬是否参与该过程,结果显示, LC3 阳性点在损伤后大约 8 -10 min开始在修复部位形成(Fig. 1C);在未损伤区域中 LC3 阳性点未增加(Fig. 1D);LC3依赖于 ATG7(Fig. 1E-H)。

进一步研究发现,膜损伤后形成了两个不同的囊泡池。较大的囊泡较早从质膜形成, Rab5、EEA1(早期内吞作用)、肌动蛋白、Rab35 呈阳性, LC3 偶尔呈阳性。相比之下,后来形成的囊泡较小且 LC3 呈阳性,最终出现在靠近 Rab5 阳性囊泡的位置。
二、 内化囊泡通过渗透作用在细胞质中收缩,与溶酶体融合
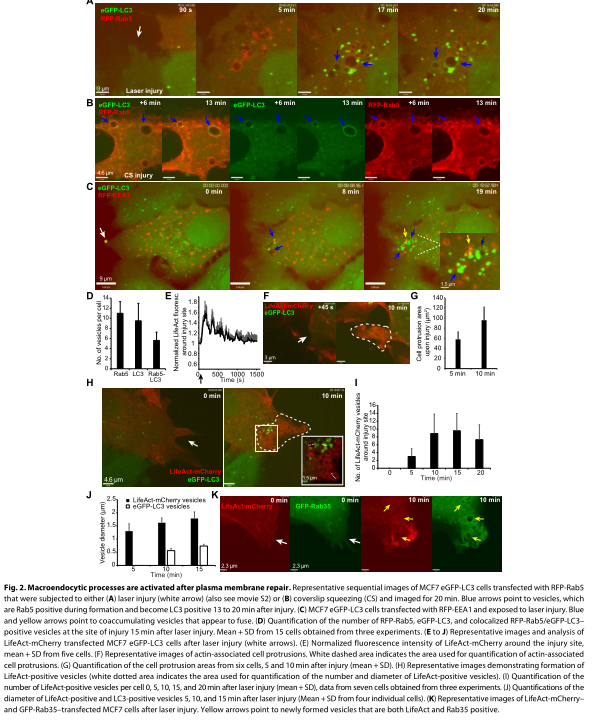
GFP-Rab35 、 RFP-Rab5 转染MCF7,研究胞吞小体的“行动轨迹”。胞吞小体囊泡移动至细胞质,在细胞质中收缩成小囊泡,最后与溶酶体融合。

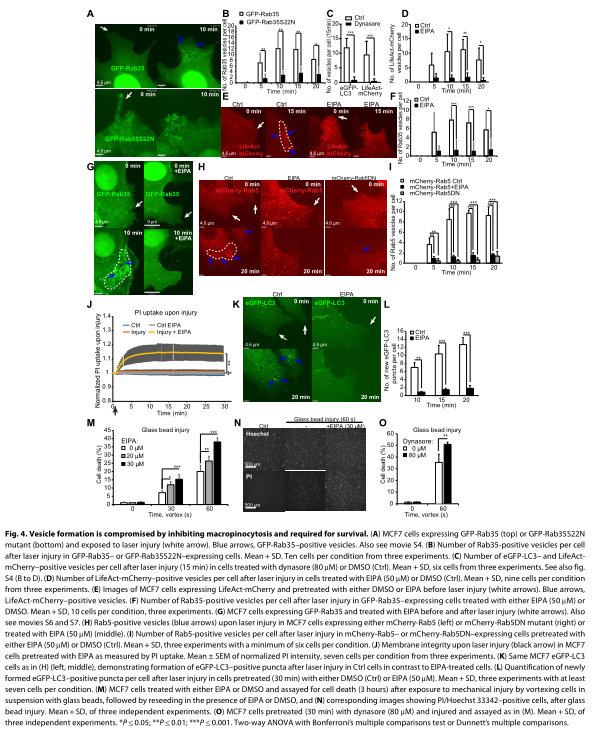
三、 巨胞饮由质膜完整性触发
实验表明巨胞饮作用在损伤后被激活,需要重组,从而保持质膜的完整性。 此外,LC3 囊泡形成是响应囊泡内化而触发。
四、 Rubicon 定位于胞吞小体的界膜,是 LC3 积累所必需的