HIF1A-AS2诱导肺腺癌患者对奥西替尼耐药
虽然表皮生长因子受体酪氨酸激酶抑制剂(TKIs)在肺腺癌(LUAD)患者中显示有效,但TKI耐药性不可避免地发展,限制了长期结果。因此,迫切需要解决LUAD的耐药性问题。lncRNA HIF1A-AS2可能是各种类型肿瘤进展的关键介导因子。我们研究了HIF1A-AS2在改善肺腺癌肿瘤加重和奥希替尼耐药中的作用。在临床样本中,我们发现HIF1A-AS2在LUAD样本中上调,预示着较差的总生存期和无病生存期。HIF1A-AS2沉默抑制LUAD细胞的增殖、迁移和肿瘤发生,以及奥西替尼对体外和体内肿瘤细胞的治疗效果。HIF1A-AS2海绵吸收miR-146b-5p,促进IL-6表达,激活IL-6/STAT3通路,导致LUAD进展。miR-146b-5p和IL-6水平与LUAD患者的预后相关。我们的结果表明,HIF1A-AS2通过靶向miR-146b5p/IL-6/STAT3轴在腺癌细胞中发挥致癌因子的作用,并可能是生存的预后指标。此外,它可以成为一个潜在的治疗靶点,以提高奥西替尼在LUAD患者中的疗效。本文于2021年9月发表在“Molecular Therapy-Nucleic Acids”(IF: 8.886)期刊上。
技术路线
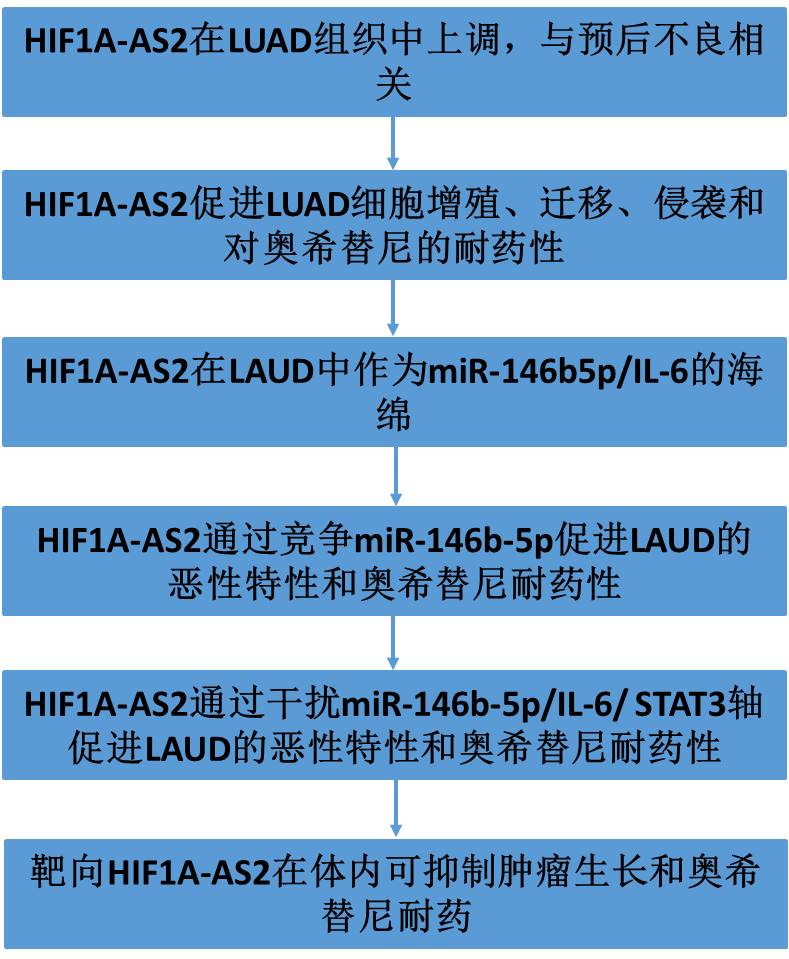
结果
1)HIF1A-AS2在LUAD组织中上调,与预后不良相关
为了研究HIF1A-AS2在LUAD中的作用,我们利用qRT-PCR检测了HIF1A-AS2在56个LUAD组织和匹配的正常瘤周组织中的相对表达。如图1A所示,HIF1A-AS2在LUAD组织中表达显著上调。为了验证HIF1A-AS2在LUAD中的表达,我们研究了TCGA)-LUAD数据库。与正常组织相比,HIF1A-AS2在肿瘤组织中的表达显著上调(图1B)。HIF1A-AS2高表达患者的DFS率和总生存期(OS)率显著低于低表达患者(图1C和1D)。在TCGA-LUAD数据库中,HIF1AAS2水平低的患者OS显著高于HIF1A-AS2水平高的患者(图1E)。在接受EGFR-TKI治疗的晚期LUAD患者的血液样本中,HIF1A-AS2表达分析显示,那些低表达HIF1A-AS2的患者对EGFR-TKI有良好的反应,而高表达HIF1AAS2的患者则表现出较差的反应(图1F)。这些结果提示,HIF1A-AS2的表达显著升高,与LUAD患者预后不良和奥西替尼耐药有关。

2)HIF1A-AS2促进LUAD细胞增殖、迁移、侵袭和对奥希替尼的耐药性
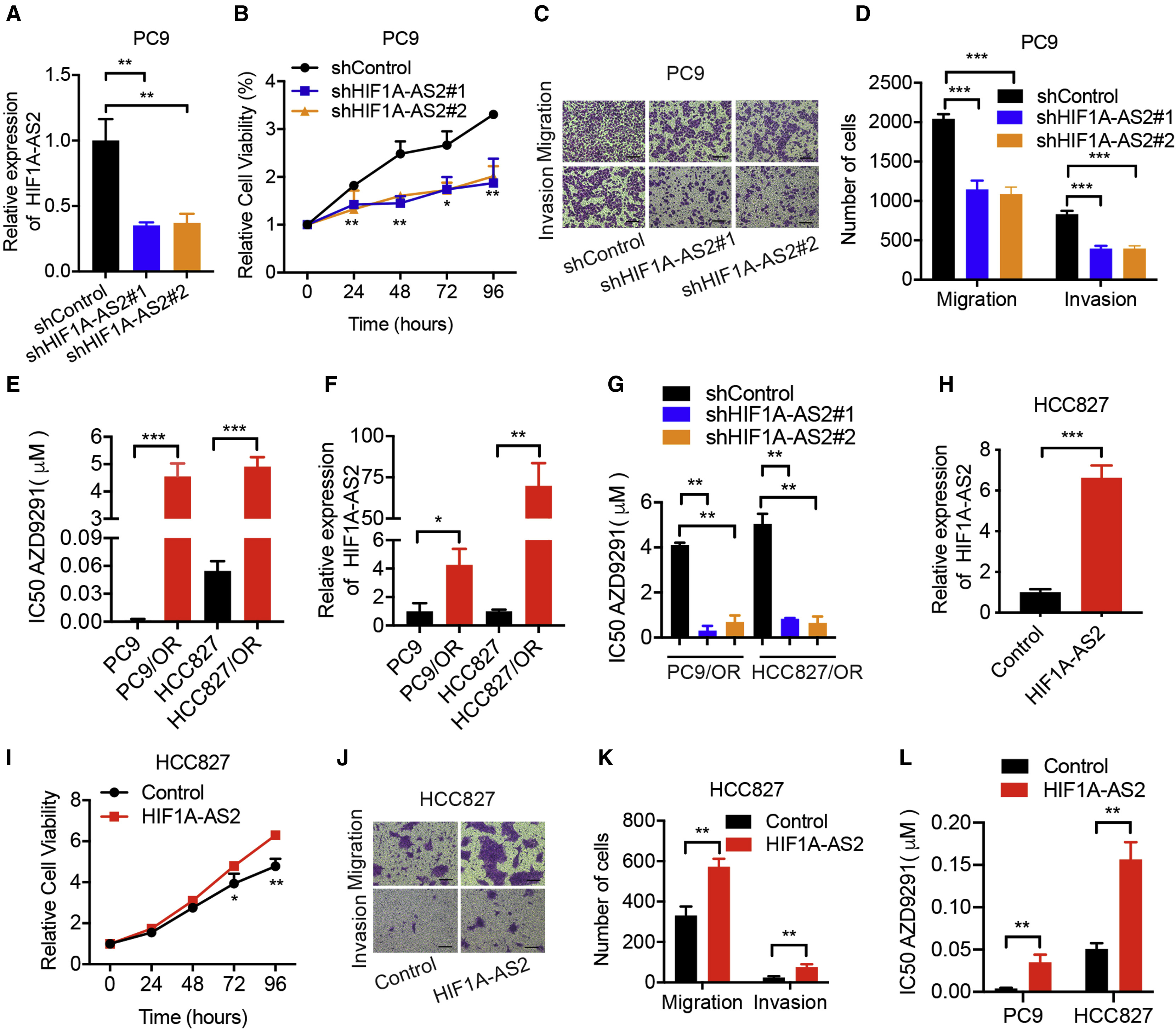
为了探索HIF1A-AS2在LUAD中的潜在生物学功能,我们转染了靶向HIF1A-AS2的shRNA或对照shRNA到PC9细胞。转染后48 h,qRT-PCR证实转染效率(图2A)。HIF1A-AS2的下调降低了PC9细胞的增殖以及迁移和侵袭的细胞数量(图2B-2D)。我们从亲本PC9和HCC827细胞中获得耐奥希替尼的PC9/OR和HCC827/OR细胞,其抑制浓度显著增加(图2 E)。HIF1A-AS2在PC9/OR和HCC827/OR细胞中的相对表达量高于亲代细胞(图2F)。因此,我们确定HIF1A-AS2是否影响了LAUD细胞对奥希替尼的敏感性。如图2G所示,与对照组细胞相比,在HIF1A-AS2缺少的PC9/OR和HCC827/OR细胞中,奥希替尼的IC50显著降低。这些数据表明,HIF1A-AS2基因的下调抑制了LAUD细胞的增殖、转移和对奥希替尼的耐药性。
我们进一步通过在PC9和HCC827细胞中过表达HIF1A-AS2来研究HIF1A-AS2的功能。我们建立了稳定过表达HIF1A-AS2的HCC287细胞(图2H)。与对照组相比,HIF1A-AS2的过表达促进了HCC287细胞的增殖、迁移和侵袭能力(图2I-2K)。此外,我们还检测了HIF1A-AS2上调对LAUD细胞对奥希替尼敏感性的影响。如图2L所示,HIF1A-AS2表达上调导致奥希替尼在PC9和HCC827细胞中的IC50增加。提示HIF1A-AS2促进LUAD细胞增殖、转移和对奥希替尼的耐药。
3)HIF1A-AS2在LAUD中作为miR-146b5p/IL-6的海绵
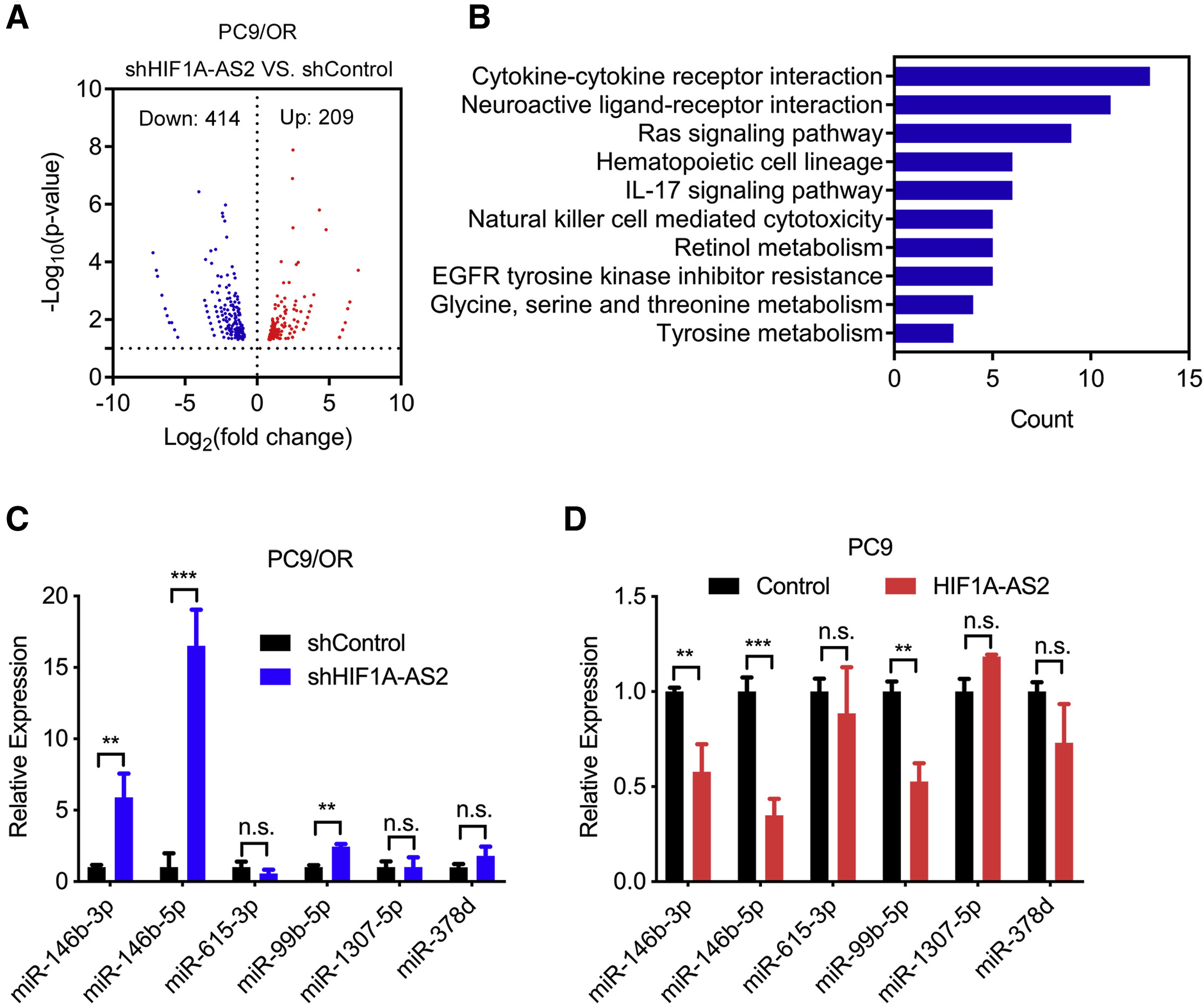
我们进行了RNA-seq来探索在HIF1A-AS2敲低的PC9/OR细胞中HIF1A-AS2的潜在靶结合miRNAs和mRNA。其中上调基因209个,下调基因414个(图3A)。当HIF1A-AS2被抑制时,包括细胞因子-细胞因子受体相互作用、IL-17信号通路和EGFRTKI耐药在内的信号通路发生改变(图3B)。在潜在的候选miRNAs中,miR-146b-3p、miR-146b-5p、miR-615-3p、miR-99b-5p、miR-1307-5p和miR-378d的表达水平与HIF1A-AS2呈负相关。qRT-PCR分析证实,HIF1A-AS2上调后,miR146b-3p、miR146b-5p和miR99b-5p的表达均显著下调。相比之下,沉默HIF1A-AS2增强了miR146b-3p、miR146b-5p和miR99b-5p的表达(图3C和3D)。
4)HIF1A-AS2通过竞争miR-146b-5p促进LAUD的恶性特性和奥希替尼耐药性
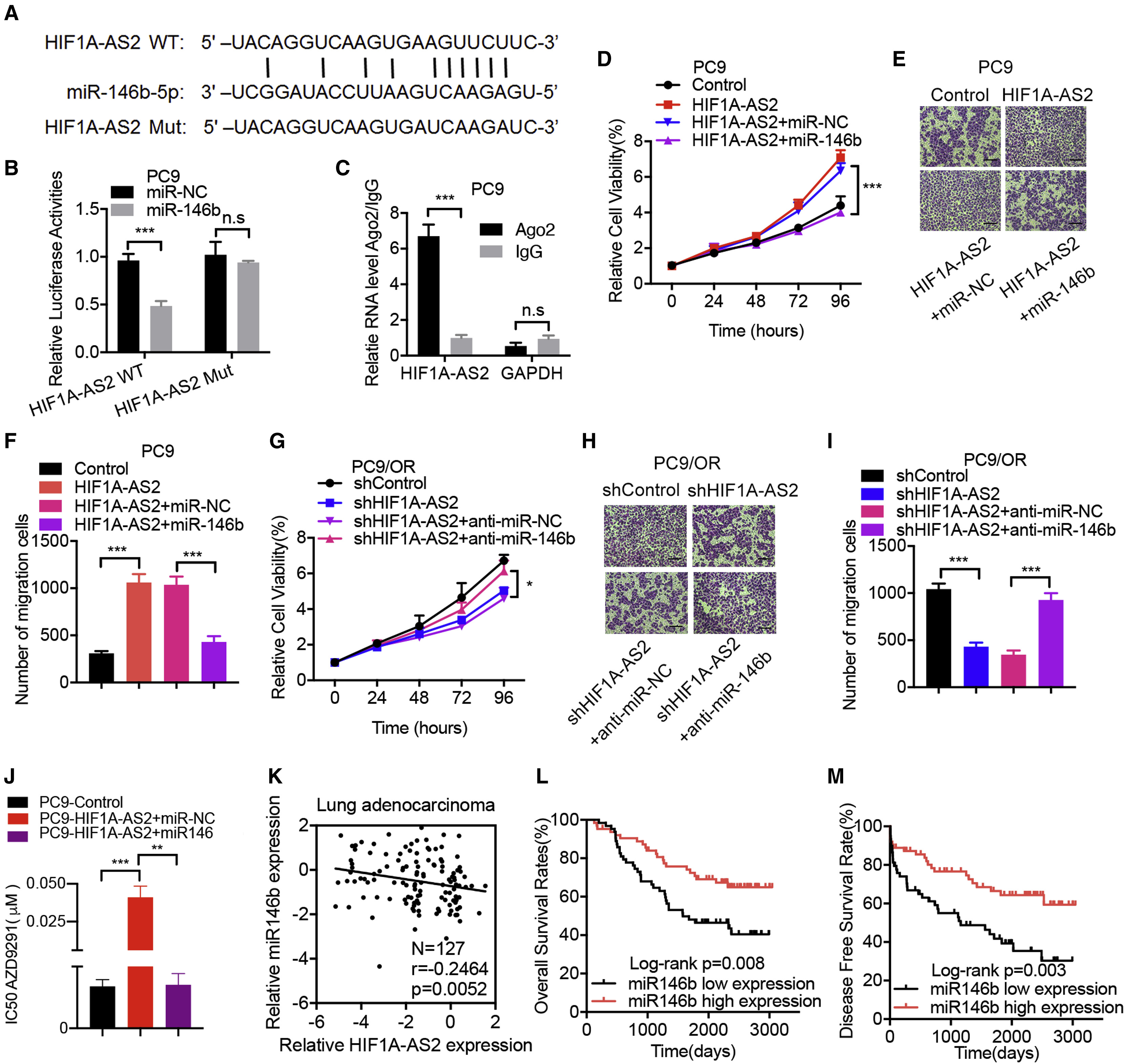
生物信息学分析显示HIF1A-AS2和miR146b-5p之间存在推定的互补序列。为了确定HIF1AAS2是否确实被miR146b-5p、野生型(HIF1AAS2- wt)和miR146b-5p结合位点靶向,我们合成了突变型HIF1A-AS2 (HIF1A-AS2- mut)荧光素酶报告基因(图4A)。结果显示,HIF1A-AS2-WT与miR146b-5p模拟物共转染显著降低了PC9细胞中的荧光素酶活性(图4B)。此外,我们进行了RIP实验,显示HIF1A-AS2和miR146b-5p在LUAD细胞中优先富集于含AGO2的小珠中,从而验证了HIF1A-AS2和miR-146b-5p之间的相互作用(图4C)。为了验证miR146b-5p在HIF1A-AS2调控LUAD进展中的作用,我们进行了拯救实验。用miR146b-5p模拟物处理可阻断PC9细胞中HIF1A-AS2过表达诱导的细胞增殖和迁移(图4D-4F)。相比之下,抗miR-146b -5p治疗减弱了HIF1A-AS2下调对PC9/OR细胞增殖和迁移的抑制作用(图4G-4I)。此外,在HIF1A-AS2上调的PC9细胞中,奥希替尼增加的IC50可被miR146b-5p模拟物部分逆转(图4J)。为了研究miR-146b-5p在LUAD中的临床相关性,我们在127例原发性LUAD组织中使用qRT-PCR检测了miR-146b-5p的表达。HIF1A-AS2和miR-146b-5p表达之间存在负相关(图4K)。miR-146b-5p高表达的患者比低表达的患者预后良好(图4L和4M)。这些结果表明,HIF1A-AS2通过海绵吸附miR146b-5p起到了ceRNA的作用,可以部分克服HIF1A-AS2对LUAD细胞增殖、迁移和奥希替尼敏感性的促进作用。
5)HIF1A-AS2通过干扰miR-146b-5p/IL-6/ STAT3轴促进LAUD的恶性特性和奥希替尼耐药性
生物信息学分析预测IL-6是HIF1A-AS2/miR-146b-5p轴的靶基因。使用生物信息学工具确定了miR-146b-5p与IL-6的3ʹUTR区域之间的潜在结合位点(图5A)。荧光素酶报告基因检测显示IL-6-WT载体的荧光素酶活性低于IL-6-Mut载体(图5B)。为了阐明HIF1A-AS2与IL-6之间的关系,我们采用qRT-PCR检测HIF1A-AS2过表达或敲低表达的LAUD细胞中IL-6的表达情况。结果显示,HIF1A-AS2的上调增强了PC9细胞中IL-6的表达(图5C),而HIF1A-AS2的沉默抑制了PC9/OR细胞中IL-6的表达(图5D),这也通过western blotting得到验证 (图5E)。我们推测HIF1A-AS2可能通过与miR146b-5p相互作用激活IL-6/STAT3通路。接下来,我们探讨了HIF1A-AS2和STAT3通路之间的关联。Western blotting证实过表达HIF1A-AS2的PC9细胞中p-STAT3蛋白水平升高,而HIF1A-AS2敲低的PC9/OR细胞中p-STAT3蛋白水平降低。值得注意的是,STAT3水平保持不变(图5E)。此外,在PC9细胞中,HIF1A-AS2过表达诱导IL-6和p-STAT3上调被miR-146b-5p模拟物阻断(图5F)。一致地,shHIF1A-AS2下调IL-6和pSTAT3的表达,这在PC9/OR细胞中被miR146b-5p抑制剂基本消除(图5G)。在HIF1A-AS2过表达的PC9细胞中,奥希替尼增加的IC50可通过下调IL-6或隐丹参酮的表达部分逆转(图5H和5I)。接下来,我们分析了LUAD样本中HIF1A-AS2、IL-6和miR146b-5p的表达, HIF1A-AS2与IL-6呈正相关,IL-6与miR146b-5p呈负相关(图5J)。此外,IL-6高表达提示LUAD患者DFS和OS低(图5K和5M)。综上所述,HIF1A-AS2可能通过结合miR146b-5p激活IL-6/STAT3通路,促进LUAD的恶性特征。

6)靶向HIF1A-AS2在体内可抑制肿瘤生长和奥希替尼耐药
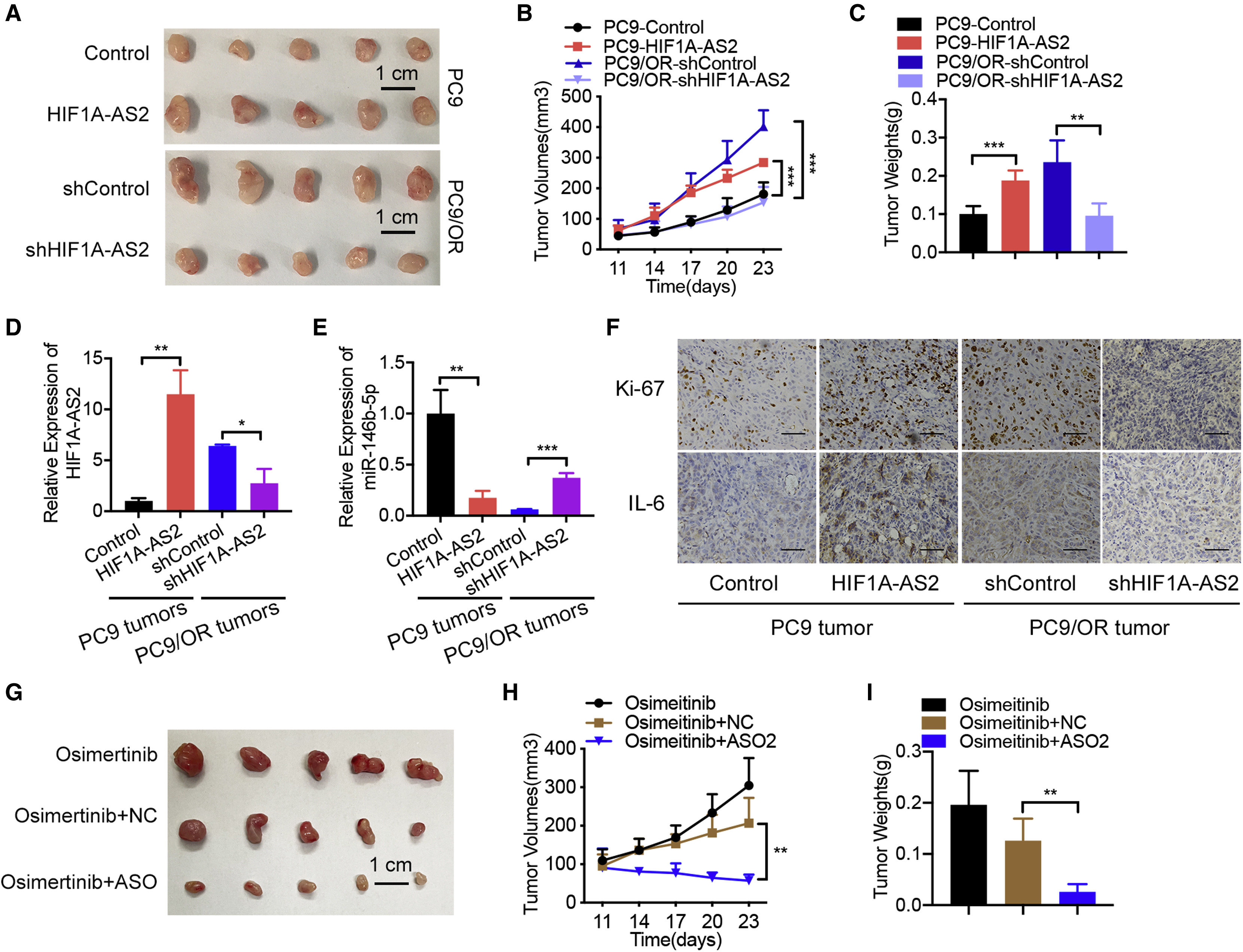
为了探讨HIF1A-AS2在体内肿瘤发生中的作用,我们进行了一项异种移植瘤实验。与对照组相比,上调HIF1A-AS2显著增加肿瘤体积和重量。相比之下,沉默HIF1A-AS2可减少肿瘤体积和重量(图6A-6C)。与对照组相比,PC9-HIF1A-AS2细胞植入小鼠获得的肿瘤组织中HIF1A-AS2表达上调。相比之下,接种PC9/OR-shHIF1A-AS2细胞的小鼠肿瘤组织中HIF1A-AS2的表达减少(图6D)。与对照组相比,接种PC9-HIF1A-AS2细胞的小鼠肿瘤组织中miR-146b-5p的表达水平降低。相反,在接种PC9/OR-shHIF1A-AS2细胞的小鼠肿瘤组织中,miR-146b-5p的表达增加(图6E)。接下来,我们使用IHC方法分析肿瘤组织中Ki-67、IL-6和p-STAT3的表达。与PC9-Control小鼠相比,PC9-HIF1A-AS2小鼠肿瘤中Ki-67、IL-6和p-STAT3的表达显著增强。相反,与PC9/OR-shHIF1A-AS2小鼠相比,PC9/ OR-shControl小鼠肿瘤中Ki-67、IL-6和p-STAT3的表达下降(图6F)。接着,为了探讨体内靶向HIF1A-AS2对耐奥希替尼的LUAD细胞肿瘤生长的影响,我们设计并使用了一种靶向HIF1A-AS2的ASO作为拮抗剂来抑制内源性HIF1A-AS2的表达。与奥希替尼加NC组相比,奥希替尼联合ASO治疗显著抑制肿瘤生长,肿瘤生长抑制率为72.4%(图6G和6H)。与NC组相比,奥希替尼+ ASO联合治疗也显著降低了肿瘤重量(图6I)。总的来说,HIF1A-AS2抑制可能是对奥希替尼耐药的LUAD患者的一种有效的治疗策略,它受miR-146b-5p/IL-6/STAT3轴的调控(图7)。

结论:HIF1A-AS2通过海绵miR-146b-5p作为ceRNA上调IL-6的表达,激活STAT3信号通路,诱导奥希替尼耐药和体内肿瘤生长。因此,我们的结果为HIF1A-AS2是LUAD潜在的治疗靶点提供了实验证据。
参考文献:
Si J, Ma Y, Lv C, Hong Y, Tan H, Yang Y. HIF1A-AS2 induces osimertinib resistance in lung adenocarcinoma patients by regulating the miR-146b-5p/IL-6/STAT3 axis. Mol Ther Nucleic Acids. 2021 Sep 14;26:613-624. doi: 10.1016/j.omtn.2021.09.003. PMID: 34703647; PMCID: PMC8517096.






