膜蛋白联动——TREM2/CD36促进泡沫细胞形成加速AS进展
动脉壁上的脂质堆积异常是动脉粥样硬化(AS)的一个标志。以前研究发现,在小鼠AS的主动脉斑块中,骨髓细胞上的触发受体2(TREM2)(一种免疫球蛋白家族的跨膜受体)的表达增加。然而,TREM2是否在AS中起作用仍未知。本研究利用ApoE knockout (ApoE−/−) 小鼠模型,原代血管平滑肌细胞(SMCs)和骨髓来源巨噬细胞(BMDMs)探究得知TREM2通过CD36表达促进SMC和巨噬细胞来源的泡沫细胞形成加速AS进展。本研究于2023年5月发表在《Cell and Molecular Life Sciences》IF:8期刊上。
技术路线

主要实验结果
1、TREM3的表达在AS斑块中增加
此前研究表明TREM2参与脂质代谢,并且在AS中TREM表达增加。作者分析了GSE43292数据集发现TREM2的表达相比于正常组织,在硬化斑块中增加(Fig. 1a)。鉴于该结果,作者检测了小鼠斑块进展时TREM2的表达,发现其在ApoE−/−小鼠主动脉中的表达随着时间增加(Fig. 1b)。此外,作者使用硬化因子oxLDL (50 µg/mL)处理RAW264.7细胞和mSMCs细胞,发现TREM2的表达也随着时间增加(Fig. 1c)。共聚焦荧光建伟就证实了TREM2的表达在Trem2+/+/ApoE−/−小鼠斑块中的表达趋势(Fig. 1d, e)。以上结果表明TREM3的表达在AS斑块中增加。
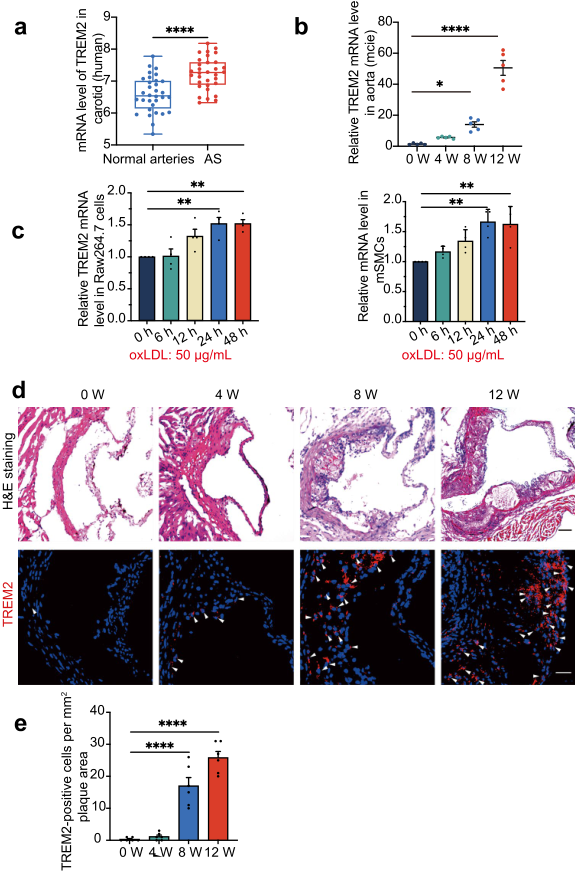
图1 TREM3的表达在AS斑块中增加
2、敲低TREM2缓解斑块形成和脂质沉积
为确定TREM2在AS中因果关系,作者在ApoE−/−小鼠中敲低TREM2构建了Trem2−/−/ApoE−/−小鼠,高脂饮食喂养12周诱导AS发生。ORO染色显示,相比对照组,Trem2−/−/ApoE−/−小鼠的整个主动脉病变区域减少(Fig. 2a)。此外,主动脉弓病变面积减小,主动脉组织坏死核减小,纤维帽厚度增加(Fig. 2a–c)。类似的,脂质染色也在Trem2−/−/ApoE−/−小鼠主动脉窦水平下降(Fig. 2b, c)。这些结果表明敲低TREM2降低斑块进展和脂质沉积。
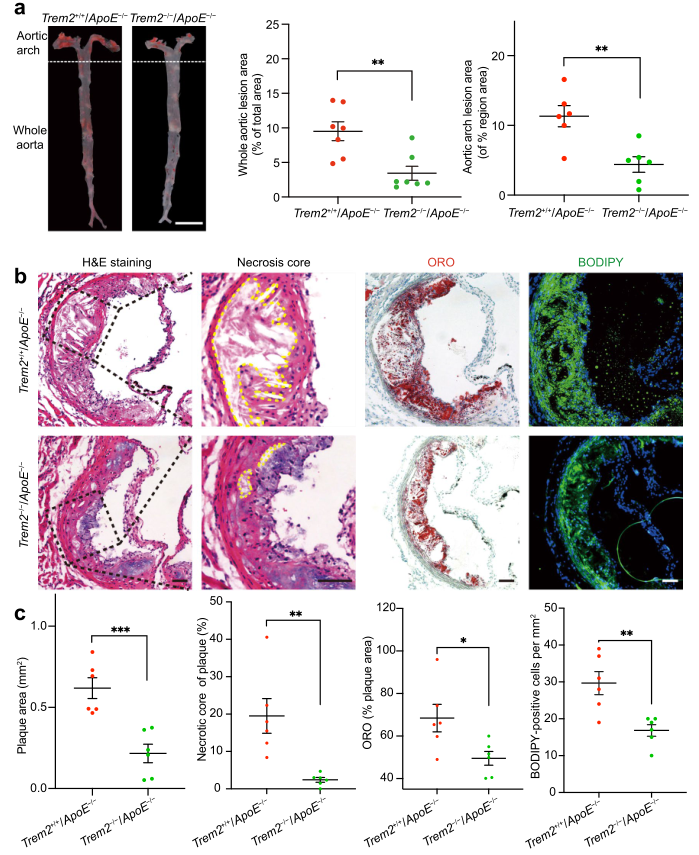
图2 敲低TREM2缓解斑块形成和脂质沉积
3、TREM2在斑块中的巨噬细胞和SMCs衍生的泡沫细胞中表达
脂质沉积是AS的标志,有助于斑块的进展和不稳定。作者研究了TREM2是否直接参与AS的脂质代谢功能障碍。将TREM2特异性抗体与斑块中的BODIPY共免疫染色。结果显示,BODIPY阳性细胞与TREM2在斑块中共定位(图3)。随着AS的进展,BODIPY/TREM2阳性细胞的数量逐渐增加(Fig. 3a, d)。这些结果与前面在体内的观察结果一致,即TREM2缺乏会降低主动脉根部的脂质负担。
由于泡沫细胞的主要来源是SMCs和巨噬细胞,所以作者研究了TREM2在这两种细胞的泡沫过程中的作用。用细胞SMC标记物(α-SMA)和巨噬细胞标记物(CD68)对不同时期饲喂HFD小鼠主动脉窦的TREM2抗体进行免疫荧光共染色。结果表明,TREM2在斑块中与α-SMA和CD68共定位,并且TREM2/α- SMA阳性和TREM2/ CD68阳性细胞的数量随着动脉粥样硬化的进展而增加(Fig. 3b, c, e, f),表明TREM2在动脉粥样硬化病变中上调,并在SMCs和巨噬细胞中富集,即TREM2参与动脉粥样硬化过程中SMCs和巨噬细胞的泡化。

图3TREM2在斑块中的巨噬细胞和SMCs衍生的泡沫细胞中表达
4、TREM2通过CD36受体促进泡沫细胞的形成
为探究TREM2是否促进巨噬细胞和SMCs细胞形成泡沫细胞,作者利用慢病毒在Raw264.7和mSMCs细胞中过表达TREM2。ORO染色显示,用50 μg/mL oxLDL处理24小时后,TREM2过表达组的ORO阳性细胞显著增多(Fig. 4a, b)。此前研究表明TREM2促进小胶质细胞的脂质摄取。为阐明TREM2促进泡沫细胞形成的机制,作者进一步检测了动脉粥样硬化中参与脂质代谢的主要脂质摄取受体(CD36, MSR1和OLR1)和外排受体(ABCG1和ABCA1)的蛋白水平变化。结果表明,TREM2对脂质摄取受体MSR1和OLR1的表达无显著影响,同样,脂质外排受体ABCG1和ABCA1的表达也不受TREM2表达的影响,然而,与LV-GFP组相比,LV-TREM2组Raw264.7细胞和mSMCs中CD36蛋白水平显著升高(Fig. 4c, d)。此外,TREM2增加了CD36的mRNA水平,但没有增加其他受体的转录(Fig. 4e, f)。在原代BMDMs和mSMC中,敲除TREM2导致CD36的表达降低(Fig. 4g)。
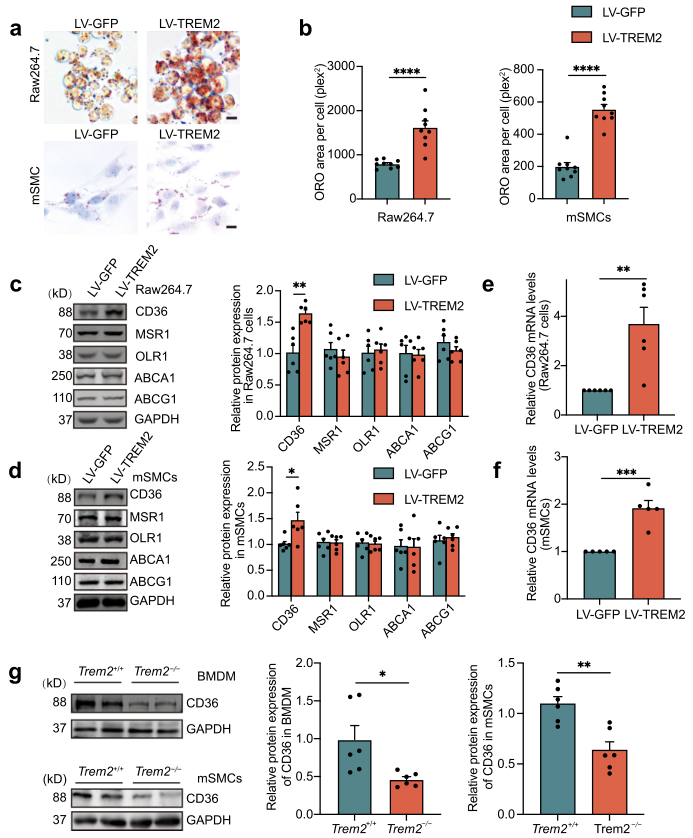
图4 在体外TREM2促进泡沫细胞的形成
CD36是动脉粥样硬化中影响脂质摄取的主要受体,因此使用DiI-oxLDL来评估脂质摄取水平。免疫荧光分析和流式细胞术显示,TREM2促进了Raw264.7细胞和mSMCs对DiI-oxLDL的摄取(图5a, b),这与先前在小胶质细胞中的研究一致。为进一步评估TREM2对CD36表达的影响,在过表达TREM2的细胞中使用siRNA抑制CD36的表达。结果显示CD36沉默抑制TREM2诱导的Raw264.7细胞和mSMCs中脂质积累和摄取的增加(Fig. 5c–f)。
以上数据表明TREM2通过CD36促进脂质摄取进而促进泡沫细胞的形成。
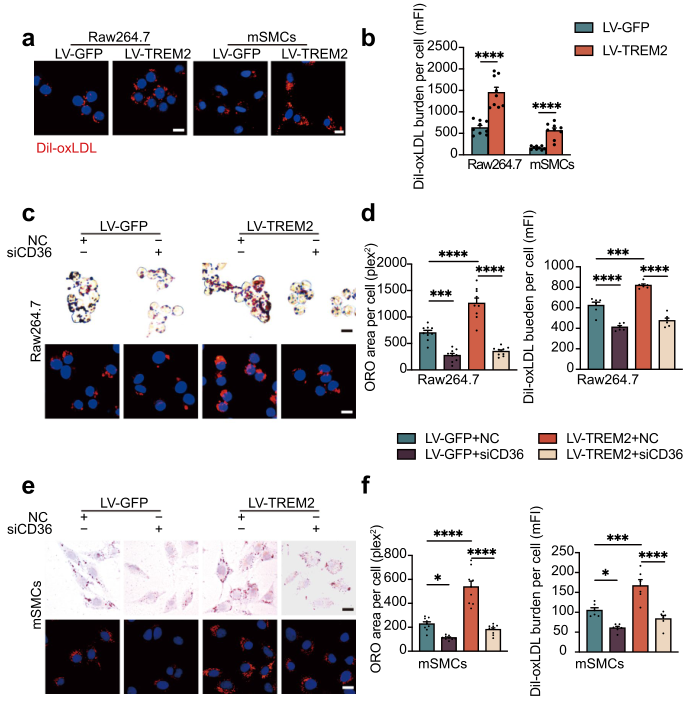
图5 TREM2通过调节CD36刺激胆固醇摄取
5、TREM2通过调节MAPK-p38和PPARγ的磷酸化调控CD36的表达
转录因子PPARγ是调控CD36转录的最重要因子。WB结果显示TREM2不改变oxLDL刺激下的PPARγ的蛋白表达,但显著抑制PPARγ的磷酸化活性(Fig. 6a–d)。这些结果表明,TREM2通过调控PPARγ的磷酸化水平调控CD36的转录水平,进而调控动脉粥样硬化过程中脂质积累和泡沫细胞的形成。
MAPK信号通路调控AS和肥胖期间的多种转录印制的激活,其参与TREM2和PPARγ信号通路,因此,作者检测了TREM2过表达后的MAPK信号通路,包括p38,JNK1/2,ERK1/2。结果显示,过表达TREM2显著降低两株细胞中p36的磷酸化,而不影响JNK1/2,ERK1/2的磷酸化和表达(Fig. 6a–d)。这些结果表明p38参与了PPARγ的磷酸化。接下来,利用p38磷酸化激动剂Deh探究p38的作用。发现Deh刺激后,TREM2诱导的脂质摄取和积累增加受到抑制(Fig. 6e, f)。WB结果也显示p38磷酸化激动剂处理后PPARγ活性降低,CD36表达降低(Fig. 6g, h)。这些数据表明,TREM2通过抑制p-p38的磷酸化水平来调节PPARγ的活性,从而促进CD36的表达和脂质摄取。
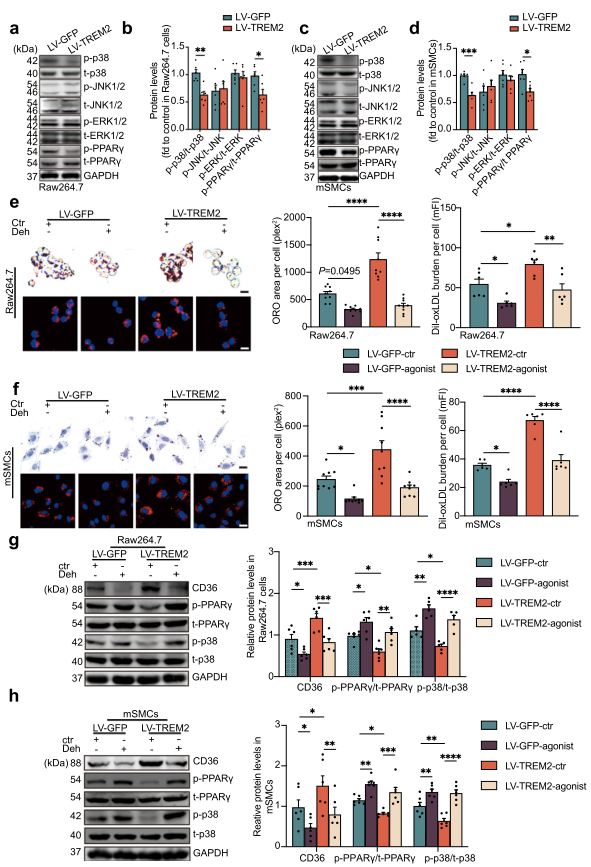
图6 TREM2调节MAPK-p38和PPARγ的磷酸化
作者检测了上述蛋白在小鼠体内的表达变化。结果进一步证实,TREM2通过p38/PPARγ信号传导和下调CD36的表达来影响动脉粥样硬化的进展(图7a,b)。此外,与Trem2+/+/ApoE-/-小鼠相比,Trem2-/-/ApoE-/-小鼠的CD36有所下降。通过CD68-BODIPY和α-SMA-BODIPY双染色,主动脉窦内的脂质负荷和泡沫细胞也明显减少(图7c-e)。总之,这些数据表明,TREM2的缺失通过调节CD36的表达来抑制动脉粥样硬化中泡沫细胞的形成。
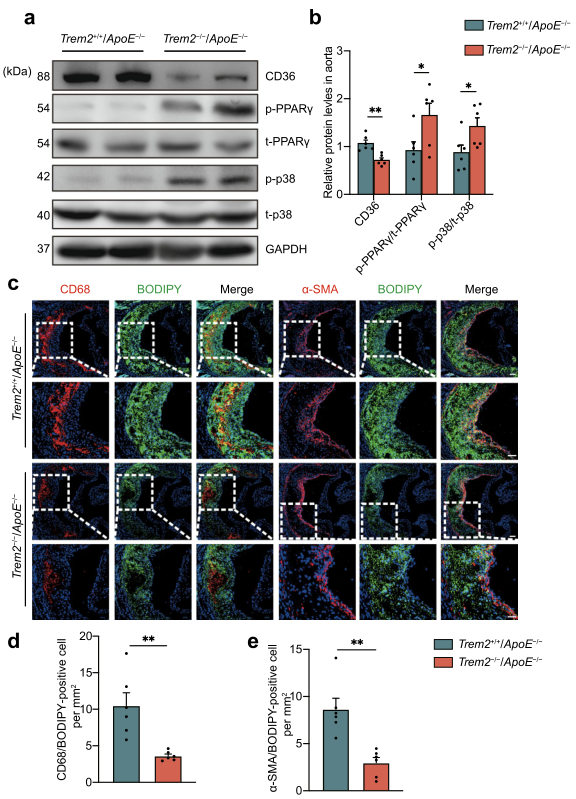
图7 在体内TREM2缺失降低泡沫细胞的形成
总之,这项研究发现,TREM2在动脉粥样硬化斑块中增加,而且TREM2的缺失会减弱ApoE-/-小鼠的动脉粥样硬化进展。在体外,TREM2的过度表达通过调节CD36的表达促进脂质吸收,加剧巨噬细胞和mSMCs中泡沫细胞的形成。因此,TREM2是治疗动脉粥样硬化的一个潜在目标。

图形摘要
实验方法
GEO芯片数据分析,TREM2-knockout mice (Trem2−/−)构建,AS斑块分析,免疫荧光(IF)染色,细胞培养和诱导,DiI-oxLDL摄取实验,ORO染色,BODIPY染色,WB实验,qRT-PCR
参考文献
Guo X, Li B, Wen C, Zhang F, Xiang X, Nie L, Chen J, Mao L. TREM2 promotes cholesterol uptake and foam cell formation in atherosclerosis. Cell Mol Life Sci. 2023 May 3;80(5):137. doi: 10.1007/s00018-023-04786-9. PMID: 37133566.






