国自然热点追踪——m7G甲基化近期文献摘要汇总
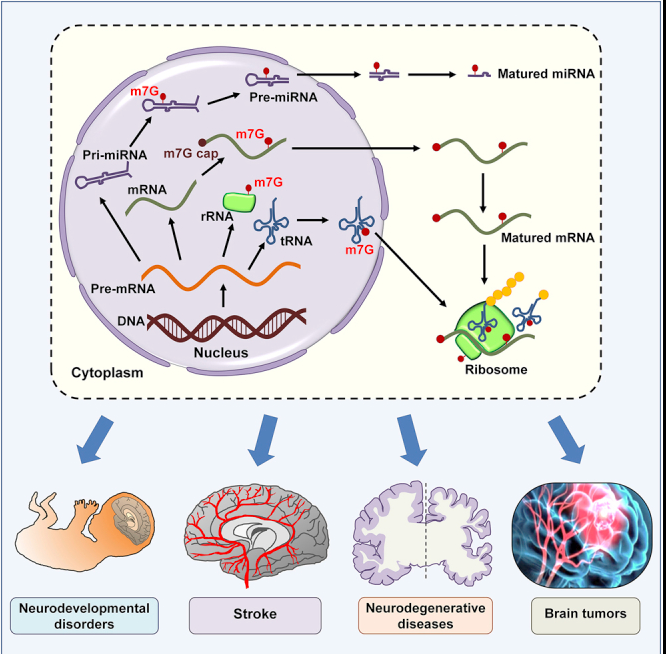
N7 -甲基鸟苷(m7G)是一种最常见的RNA表观修饰,也是一种进化上保守的RNA修饰,最初是在信使RNA(mRNA)的5‘端发现的。大多数真核细胞mRNAs在其5′端的末端鸟苷的N7位置有一个甲基和一个正电荷。这种修饰稳定了转录物免受核外降解,并介导相关生物功能,包括转录延伸、pre mRNA剪接、核输出和翻译。m7G甲基化还被发现在转移RNA(tRNA)和核糖体RNA(rRNA)的内部位置。
m7G tRNA修饰由异二聚体蛋白复合物催化,该复合物在哺乳动物中包括甲基转移酶样-1蛋白(METTL1)和WD重复结构域4(WDR4), METTL1/WDR4复合体可以将m7G安装在mRNA上,这会影响mRNA的翻译效率,也可以催化tRNA中m7G的修饰。 m7G在tRNA核苷酸位置46(m7G46)是最普遍的tRNA修饰之一。m7G46 存在于 tRNA 亚群的可变环区,tRNA-Phe 结构显示 C13–G22-m7G46碱基三重相互作用,有助于稳定三级结构。在rRNA中,WBSCR22/TRMT112 复合物作为甲基转移酶参与了18S rRNA前体的加工, 这对于 40S 核糖体亚基之前的核输出是必需的。
1. METTL1-WDR4甲基化tRNA的结构和机制
RNA 的调控修饰对于正确的基因表达非常重要。 tRNA 富含各种影响其稳定性和功能的化学修饰。 tRNA 46 位的 7-甲基鸟苷 (m7G) 是一种保守修饰,可调节稳态 tRNA 水平以影响细胞生长。 METTL1-WDR4 复合物在人类中生成 m7G46,METTL1-WDR4 的失调与脑畸形和多种癌症有关。 在这里,我们展示了 METTL1 和 WDR4 如何合作识别 RNA 底物并催化甲基化。 METTL1-WDR4的晶体结构和METTL1-WDR4-tRNA的冷冻电镜结构表明,复合蛋白表面通过形状互补性识别tRNA弯头。 METTL1-WDR4-tRNA 与 S-腺苷甲硫氨酸或 S-腺苷高半胱氨酸的冷冻电子显微镜结构以及 METTL1 晶体结构通过揭示多种状态的活性位点,为催化机制提供了额外的见解。 METTL1 N 末端将辅因子与 tRNA、催化环和 WDR4 C 末端的构象变化结合起来,充当激活 m7G 甲基化的开关。 因此,我们的结构模型解释了 METTL1 N 末端的翻译后修饰如何调节甲基化。 我们的工作共同阐明了 METTL1 修饰 m7G 的核心和调控机制,为理解其对生物学和疾病的贡献提供了框架。

2. METTL1-WDR4 调节 m7G tRNA 修饰的结构基础
RNA 的化学修饰在许多生物过程中发挥着关键作用。 N7-甲基鸟苷 (m7G) 是 大量tRNAs维持 完整性和稳定性所必需的。 含有甲基转移酶 1-WD 重复序列的蛋白 4 (METTL1-WDR4) 复合物是一种甲基转移酶,可修饰某些 tRNA 可变环中的 G46,其失调会导致多种癌症类型的肿瘤发生。 WDR4 突变会导致人类发育表型改变,包括小头畸形。 METTL1-WDR4 如何修饰 tRNA 底物并受到调节仍然难以捉摸。 在这里,我们通过对人类 METTL1-WDR4 的结构、生化和细胞研究表明,WDR4 可作为 METTL1 和 tRNA T 臂的支架。 tRNA 结合后,METTL1 的 αC 区域转变为螺旋,与 α6 螺旋一起固定 tRNA 可变环的两端。 出乎意料的是,我们发现 METTL1 预测的无序 N 端区域是催化口袋的一部分,并且对于甲基转移酶活性至关重要。 此外,我们发现 METTL1 N 末端区域的 S27 磷酸化通过局部破坏催化中心来抑制甲基转移酶活性。 我们的结果提供了对 METTL1-WDR4 tRNA 底物识别和磷酸化介导的调节的分子理解,并揭示了 METTL1 假定的无序 N 端区域作为甲基转移酶活性的联系。

3. TMEM11 通过 METTL1 介导的 ATF5 mRNA m7G 甲基化调节心肌细胞增殖和心脏修复
线粒体跨膜(TMEM)蛋白家族具有多种重要的生理功能。然而,其在心肌细胞增殖和心脏再生中的作用尚不清楚。在这里,我们检测到TMEM11在体外抑制心肌细胞增殖和心脏再生。TMEM11缺失增强了心肌细胞增殖,恢复了心肌损伤后的心脏功能。相反,TMEM11过表达抑制了小鼠心脏中新生心肌细胞的增殖和再生。TMEM11直接与METTL1相互作用,增强了Atf5 mRNA的m7G甲基化,从而增加ATF5的表达。ATF5的TMEM11依赖性增加促进了Inca1的转录,Inca1是一种细胞周期蛋白依赖性激酶的抑制剂,通过与细胞周期蛋白A1相互作用,抑制心肌细胞增殖。因此,我们的研究结果表明,TMEM11介导的m7G甲基化参与心肌细胞增殖的调节,靶向TMEM11-METTL1-ATF5-INCA1轴可能作为促进心脏修复和再生的新治疗策略。

4. METTL1/WDR4介导的tRNA m7G修饰和mRNA翻译控制促进肿瘤发生和阿霉素耐药性
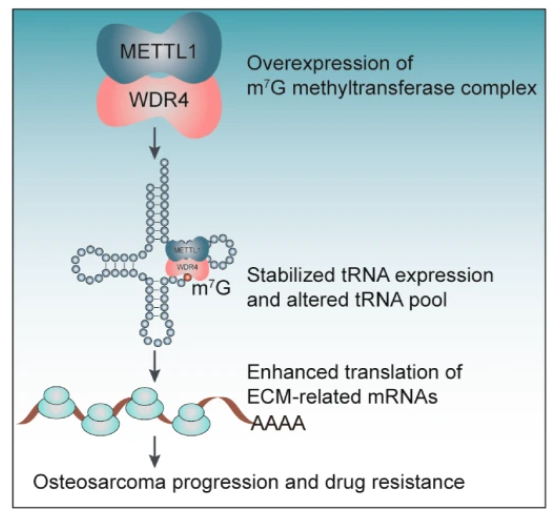
骨肉瘤是导致青少年和儿童高死亡率的最常见骨肿瘤。tRNA m7G甲基转移酶METTL1位于染色体12q14.1中,该区域在骨肉瘤患者中经常扩增,而其在骨肉瘤调节中的功能和潜在机制仍然未知。本文表明,METTL1和WDR4在骨肉瘤中过表达,与患者预后不良有关。敲低 METTL1 或 WDR4 导致 tRNA m7G修饰水平降低并阻碍体外和体内骨肉瘤的进展。METTL1/WDR4 过表达可促进骨肉瘤的增殖、迁移和侵袭。tRNA甲基化和mRNA翻译分析表明,METTL1/WDR4 修饰的 tRNA 可通过更多 m7G tRNA 解码密码子增强 mRNA 的翻译,包括细胞外基质 (ECM) 重塑效应子,从而促进骨肉瘤进展和对阿霉素的化疗耐药。研究表明METTL1/WDR4介导的tRNA m7G修饰通过改变致癌mRNA翻译来增强骨肉瘤进展和对阿霉素的耐药,具有关键的致癌功能,表明METTL1抑制联合化疗是治疗骨肉瘤患者的有希望的策略。
5. QKI将m7G修饰的内部转录物穿梭到应激颗粒中并调节mRNA代谢
N7甲基鸟苷(m7G)修饰通常发生在mRNA 5‘端或tRNA/rRNA内,也存在于mRNA内部。尽管m7G 5‘端对于pre mRNA加工和蛋白质合成至关重要,但mRNA内部m7G修饰的确切作用仍然难以捉摸。在这里,我们报道了mRNA内部m7G被震动蛋白( Quaking proteins ,QKIs)选择性识别。通过对m7G甲基组和QKI结合位点的转录组全谱分析/定位,我们鉴定了1000多个具有保守“GANGAN(N=a/C/U/G)”基序的m7G修饰和QKI-结合的高置信度mRNA靶标。 QKI7与应激颗粒(SG)核心蛋白G3BP1相互作用(通过C末端),并将m7G修饰的内部转录物穿梭到SG中,以调节mRNA在应激条件下的稳定性和翻译。具体而言,QKI7减弱河马信号通路中基本基因的翻译效率,从而使癌症细胞对化疗敏感。总之,我们将QKIs表征为调节靶mRNA代谢和细胞耐药性的mRNA内部m7G结合蛋白。







