泛癌tRNA 衍生片段CAT1协调RBPMS稳定NOTCH2 mRNA促进肿瘤发生

转运核糖核酸衍生片段(tRFs)是一类小非编码调控RNAs,与许多疾病的病理生理学有关。然而,tRFs 在癌症进展中的作用在很大程度上仍然难以捉摸。本研究证明泛癌症3′-tRF CAT1(癌症相关tRF 1)在肿瘤中普遍上调,并与包括肺癌在内的多种癌症的不良预后相关。机制上,癌细胞中上调的CAT1与具有多重剪接功能的 RNA 结合蛋白(RBPMS)结合,取代NOTCH2与RBPMS 的联系,从而抑制随后由CCR4-NOT脱腺苷化复合物介导的NOTCH2 mRNA衰减。该研究于2023年8月发表在《Cell Reports》,IF:8.8。
技术路线
主要研究结果
1. 泛癌CAT1上调促进肿瘤细胞增殖和侵袭,与癌症患者预后不良相关
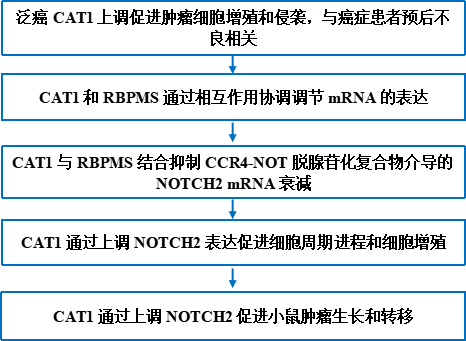
为确定CAT1在肿瘤发病机制中的确切作用,分析小RNA测序(RNA-seq)数据,结果表明CAT1是一个18-nt的3′-tRF,它是由携带对应于氨基酸L-丙氨酸的反密码子AGC(即tRNA-Ala-AGC-1-1)的only tRNA isodecoder的TψC环切割产生的(图1A,右)。dumbbell-聚合酶链反应(Db-PCR)产物的Sanger测序验证肿瘤标本中CAT1的18-nt序列(图1A,左),Db-PCR是一种改良的TaqMan实时qPCR方法,可以单碱基分辨率对RNA片段的5ʹ和3ʹ端变异体进行特异性定量(图1A,左)。对TCGA数据集的分析表明,CAT1在许多类型的肿瘤组织中显著上调(图1B)。值得注意的是,其高表达强烈预测各种癌症类型患者的短生存期(图1C)。与此一致,对一组独立的癌症标本进行的Db-PCR分析证实,与健康标本相比,CAT1在大多数癌症类型中高度丰富,且表达上调(图1D)。鉴于非小细胞肺癌(NSCLC)是全球癌症相关死亡率的主要原因,因此选择肺癌细胞系(A549和Calu1)作为评估CAT1在癌症中的功能的主要模型。正如预期的那样,CAT1不仅在肺癌组织中上调(图1B和1D),而且其高表达还与较差的预后相关。值得注意的是,对30例NSCLC患者和25例健康对照者血浆标本的Db-PCR分析表明,CAT1在肺癌患者血浆中的表达显著且持续高于健康对照者(图1E)。综上所述,这些结果表明CAT1在癌组织和NSCLC患者血浆中高表达,并与不良预后相关。CAT1敲低降低肺癌细胞的增殖(图1F)、迁移(图1G)和侵袭(图1G)。此外,CAT1敲除诱导G1期阻滞(图1H)。
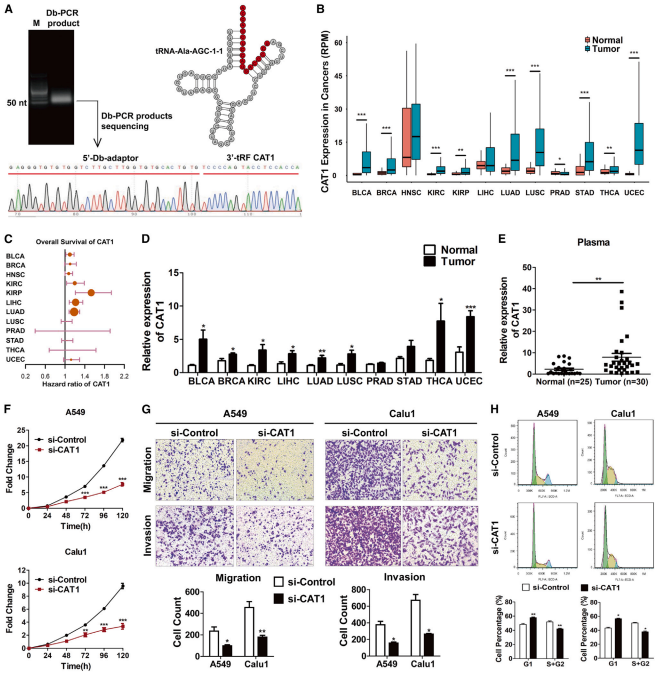
图1. 泛癌CAT1上调促进肿瘤细胞增殖和侵袭,与癌症患者预后不良相关
2. CAT1和RBPMS通过相互作用协调调节mRNA的表达
为阐明CAT1调控癌细胞的机制,使用合成的3′-生物素化CAT1在A549细胞中进行RNA pull-down实验。免疫印迹分析表明RBPMS是一种相关蛋白,而CAT1反义链未与RBPMS结合(图2A)。同样,在A549细胞中使用抗RBPMS抗体进行的RNA免疫沉淀(RIP)检测证实,RBPMS与CAT1结合,但未与其他tRFs结合,如5′-IleAAT-8-1-L20 (Ile-20,阴性对照)(图2B)。CAT1在3′末端含有CAC RRE,RNA下拉实验表明,含有GGG取代CAC的CAT1突变体降低CAT1与RBPMS的结合(图2C)。与这一发现一致,缺失RRM结构域的RBPMS突变体失去与CAT1的关联(图2D)。这些结果表明CAT1与RBPMS蛋白的相互结合依赖于CAT1中的CAC RRE被RBPMS的RRM结构域识别。利用RNA-seq对CAT1敲低(图2E)和RBPMS敲除细胞进行无偏转录组分析(图2F)。这项分析显示,5,873个基因在CAT1敲低时发生改变,3,777个基因在RBPMS敲低时发生改变,其中1,321个基因在RBPMS敲低细胞和CAT1敲低细胞中同时发生改变(图2G)。观察到的1,321个改变基因的数量显著高于在RBPMS敲除和CAT1敲除细胞中偶然同时发生的改变基因的数量(p=1.06E71),表明CAT1和RBPMS协同调节一些改变基因的表达。此外,RBPMS-RIP-seq显示,1,741个包含CAC RREs的基因与RBPMS结合,其中176个与RBPMS和CAT1可能共同调节的1,321个基因重叠(图2G)。然后对这176个基因进行GO富集分析,发现其中25个基因与细胞周期调控相关,这与CAT1对肿瘤细胞周期进程的强调控(图1H)很好地吻合。对这些验证基因的FLAG-RBPMS-RIP分析显示,除LIG4外,其他8个基因与RBPMS相关,但与RRM截短突变体无关,其中相对富集度最高的是NOTCH2(图2H)。这些结果表明,CAT1和RBPMS通过相互作用协同调节包括NOTCH2在内的mRNA的表达。
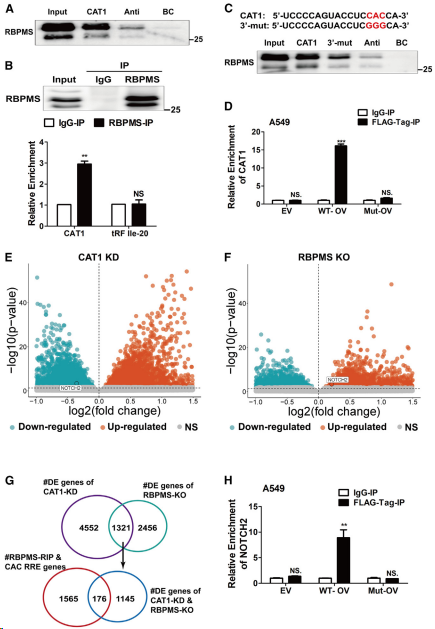
图2. CAT1和RBPMS通过相互作用协调调节mRNA的表达
3. CAT1与RBPMS结合抑制CCR4-NOT脱腺苷化复合物介导的NOTCH2 mRNA衰减
NOTCH2在肿瘤中常被过度表达或突变,可上调CCND1的表达并调节细胞周期在G0/G1期和细胞增殖。使用抗RBPMS抗体对A549细胞进行RIP分析,结果表明,CAT1的过表达(与RBPMS呈剂量依赖性结合)(图3A)以CAT1表达依赖性的方式降低RBPMS相关NOTCH2 mRNA的富集(图3B),同时细胞NOTCH2 mRNA总表达相应增加(图3C)。此外,对转录的Notch胞内结构域(NICD) RNA进行的电泳迁移率变化分析(EMSA)表明,纯化的RBPMS与合成的3′-生物素化CAT1结合,并且这种结合以依赖于NICD RNA剂量的方式减少(图3D)。这些结果表明CAT1和NOTCH2 mRNA竞争性结合RBPMS,并且CAT1与RBPMS的结合取代NOTCH2 mRNA与RBPMS的结合。值得注意的是,在用Dactinomycin处理的肺癌细胞中敲低CAT1,抑制重新转录,从而消除转录调控的作用,使NOTCH2 mRNA的半衰期缩短(图3E),而过表达CAT1(图3F)或去除RBPMS(图3G)则延长NOTCH2 mRNA的半衰期。重要的是,CNOT1敲低挽救了CAT1敲低引起的NOTCH2半衰期缩短(图3H、3I)。与这些发现一致,通过siRNA(图3J和3K)敲除CAT1降低NOTCH2的mRNA和蛋白水平,而这种降低可通过敲除RBPMS(图3L和3M)或CNOT1(图3N和3I)来消除。相反,CAT1过表达(图3C)或RBPMS敲低(图3O和3P)增加NOTCH2 mRNA和蛋白的表达。接下来研究CAT1和RBPMS对notch2介导的CCND1、CDK4和EMT标志物表达的调节作用,结果表明,敲除RBPMS(图3P)增加了这些蛋白的表达,并且敲除RBPMS可消除CAT1诱导的减少(图3M)。总之,这些结果表明,CAT1与RBPMS的结合减弱了RBPMS与NOTCH2 mRNA关联,并抑制随后CCR4-NOT脱腺苷化复合物介导的NOTCH2 mRNA衰变,从而上调NOTCH2的表达
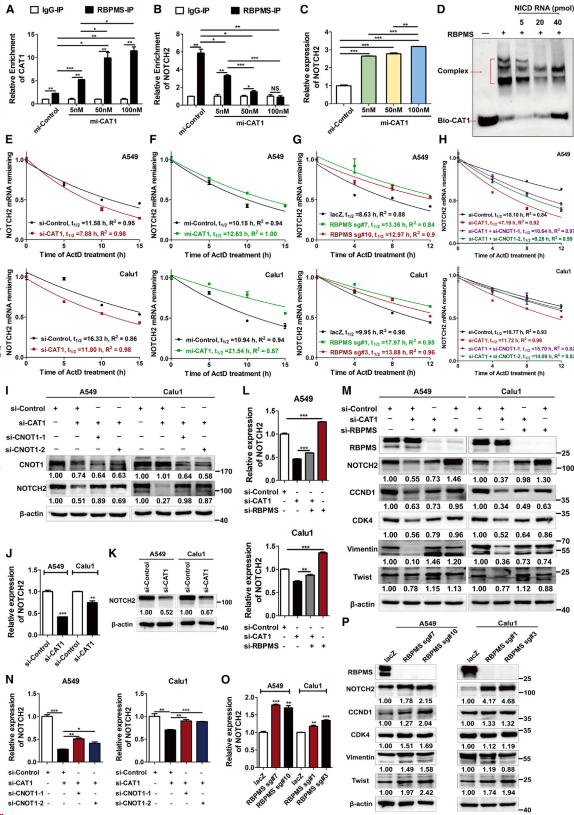
图3. CAT1与RBPMS结合抑制CCR4-NOT脱腺苷化复合物介导的NOTCH2 mRNA衰减
4. CAT1通过上调NOTCH2表达促进细胞周期进程和细胞增殖
接下来检测CAT1介导的和RBPMS以及CNOT1依赖的NOTCH2上调对细胞增殖和侵袭的影响。发现,NOTCH2过表达恢复CAT1缺失诱导的G1期阻滞(图4A)以及肺癌细胞增殖(图4B)、迁移和侵袭(图4C)的减少。通过过表达NOTCH2, CAT1敲低抑制的CCND1和CDK4以及EMT标志物的相应表达水平也中度恢复(图4D)。相反,CAT1过表达促进从G1期向S期(G1/S)的转变(图4E)、细胞增殖(图4F)、迁移和侵袭(图4G)。同样,NOTCH2敲低后,CAT1过表达引起的CCND1和CDK4以及EMT标志物水平升高有所降低(图4H)。这些数据表明CAT1通过抑制RBPMS/ CCR4-NOTCH2介导的NOTCH2 mRNA的衰减促进肺癌细胞周期进程以及增殖和侵袭。
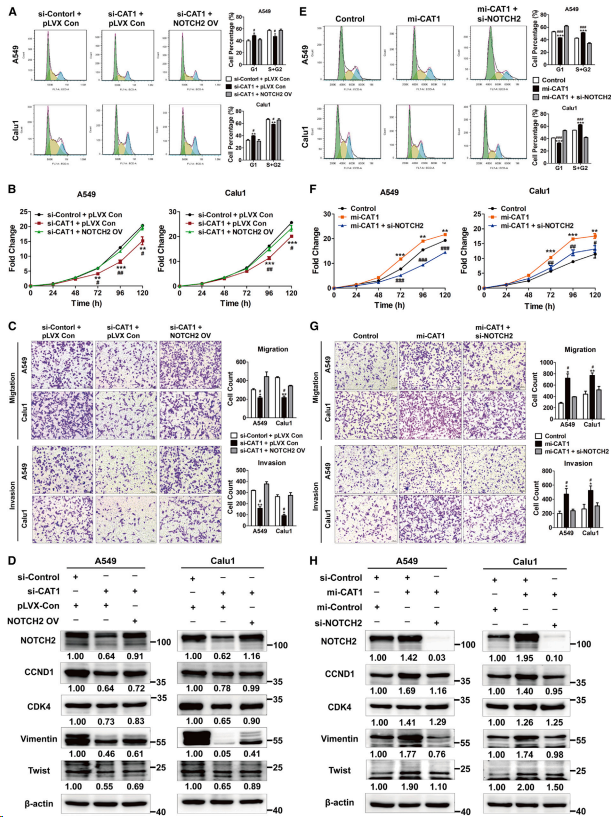
图4. CAT1通过上调NOTCH2表达促进细胞周期进程和细胞增殖
5. CAT1通过上调NOTCH2促进小鼠肿瘤生长和转移
将敲除CAT1的A549细胞接种于BALB/c裸鼠皮下,观察CAT1在A549细胞成瘤中的作用。CAT1缺失显著减小肿瘤大小(图5A)、体积(图5B)和重量(图5C)。将CAT1敲除后表达荧光素酶报告基因的Calu1细胞尾静脉注射至裸鼠体内。生物发光成像显示,CAT1敲除大大降低小鼠转移性肺肿瘤的生长(图5D)和肺转移结节的数量(图5E)。Calu1细胞中CAT1过表达显著增加肿瘤大小(图5F)、体积(图5G)、重量(图5H),而这种增加被NOTCH2敲除抑制(图5F - 5H)。对肿瘤组织的实时qPCR和免疫组化分析表明,CAT1敲除降低NOTCH2 mRNA表达(图5I),相应降低NOTCH2蛋白水平(图5J)。相反,CAT1过表达增强肿瘤组织中NOTCH2 mRNA表达(图5K),相应增加NOTCH2蛋白水平(图5L),而这种增加被NOTCH2敲除消除(图5K和5L)。这些数据表明CAT1通过上调NOTCH2促进小鼠肿瘤的生长和转移。
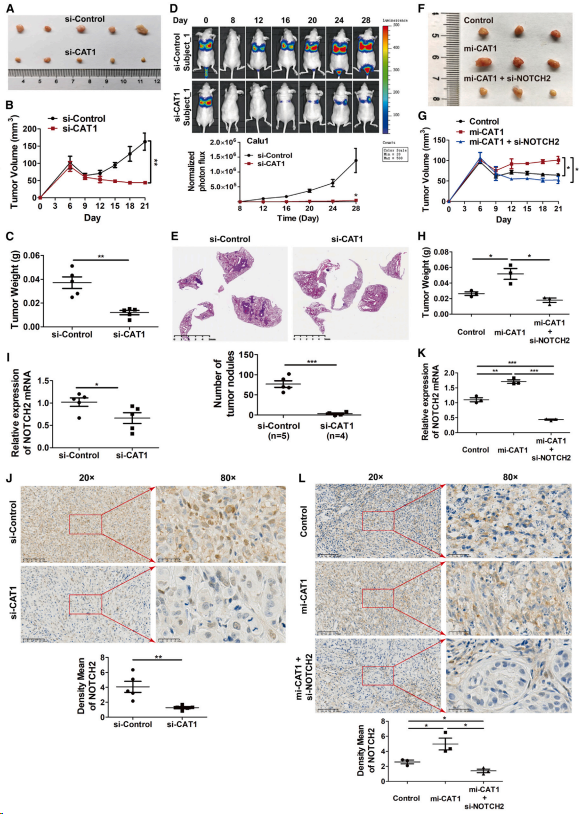
图5. CAT1通过上调NOTCH2促进小鼠肿瘤生长和转移
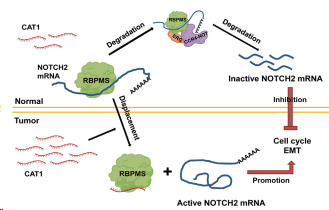
图6. CAT1介导的肿瘤生长和进展调节示意图
结论
综上所述,本研究证明泛癌3′-tRF,CAT1,在肿瘤中普遍上调,并与包括肺癌在内的多种癌症的不良预后相关。揭示了癌症特异性CAT1上调与癌症进展之间的内在联系,显示了3′-tRF对癌症中NOTCH信号转导的调控,并凸显了其巨大的临床潜力。
实验方法
细胞转染,用CRISPR/Cas9生成基因敲除细胞系,细胞增殖实验,体外迁移及侵袭试验,细胞周期分析,RNA提取及实时荧光定量PCR分析,血浆RNA提取,tRF的Dumbbell-PCR,四叶草RT-qPCR检测成熟tRNA,WB,Northern blot,RNA pull-down,RIP,Co-IP,体外转录实验,EMSA,RNA稳定性实验,双荧光素酶报告实验,基因过表达,免疫组化,RNA-seq和数据分析,动物实验
参考文献
Yu M, Yi J, Qiu Q, Yao D, Li J, Yang J, Mi C, Zhou L, Lu B, Lu W, Ying K, Chen W, Chen E, Zhang H, Lu Z, Lu Y, Liu P. Pan-cancer tRNA-derived fragment CAT1 coordinates RBPMS to stabilize NOTCH2 mRNA to promote tumorigenesis. Cell Rep. 2023 Nov 8;42(11):113408. doi: 10.1016/j.celrep.2023.113408. Epub ahead of print. PMID: 37943661.






